Содержание
Ошибка 404 | Областной перинатальный центр
АКТУАЛЬНЫЕ НОВОСТИ!
⚡⚡⚡ График работы ГБУЗ ЯО «Областной перинатальный центр» в новогодние праздники.
с 31.12.2022 по 08.01.2023 Администрация и амбулаторно-поликлинические отделения не работают.
04.01.2023 – рабочий день в консультационно-диагностическом отделении (прием у врача-акушера-гинеколога и пренатальный скрининг — по предварительной записи).
Стационарная и экстренная помощь пациентам будет оказываться в полном объёме.
В Перинатальном центре сформированы дежурные бригады, утверждены графики дежурства врачей, среднего медперсонала и администрации.
09.01.2023 – рабочий день.
⚡⚡⚡
В связи с завершением финансового года, банковские карты 30.12.2022 в качестве средства платежа не принимаются. Предлагаем осуществлять оплату наличными денежными средствами.
⚡⚡⚡ Партнерские роды временно приостановлены
В соответствии с письмом Департамента здравоохранения и фармации Ярославской области от 15.
Исходя из вышеизложенного, присутствие родственников при родоразрешении беременной (партнерские роды) приравнивается к посещению пациентов структурных подразделений стационарного типа.
Снятие ограничений будет возможно при улучшении эпидемиологической обстановки по гриппу и ОРВИ в Ярославской области.

⚡⚡⚡
Памятка для медицинских работников по проведению дифференциальной диагностики COVID-19 с гриппом и ОРВИ, определению тактики ведения больных, включая детей, лиц пожилого возраста и беременных с алгоритмом действий медицинских работников, оказывающих медицинскую помощь в амбулаторных условиях, в том числе на дому, пациентам с ОРВИ и Памятка для населения (ссылка) по профилактике и лечению сезонного гриппа, COVID-19, РС-инфекции и других острых респираторных вирусных инфекций (письмо Министерство здравоохранения Российской Федерации от 28.11.2022 №30-4/И/1-20344)
—————————————————————————————————————————————————————
⚡⚡⚡
С учетом эпидемиологической ситуации, в настоящее время продолжает действовать ограничение на посещения пациентов стационарных отделений Перинатального центра.
⚡⚡⚡ Информация для сопровождающих лиц
В связи с повышенным риском распространения COVID-19 нахождение лиц, сопровождающих пациентов амбулаторных отделений, в здании Перинатального центра не допускается. Вход в здание Перинатального центра разрешен только сопровождающим недееспособных пациентов и пациентов с ограниченными возможностями.
Вход в здание Перинатального центра разрешен только сопровождающим недееспособных пациентов и пациентов с ограниченными возможностями.
⚡⚡⚡ Информация для пациентов с бесплодием, нуждающихся в проведении ВРТ
В соответствие с приказом Минздрава РФ от 31.07.2020 №803н «О порядке использования вспомогательных репродуктивных технологий, противопоказаниях и ограничениях к их применению», который вступил в силу 01.01.2021, наличие показаний к проведению программ ВРТ осуществляет лечащий врач. Он же оформляет направление на проведение лечение бесплодия методом ЭКО.
Для получения направления необходимо обратиться на консультацию к врачу-репродуктологу отделения охраны репродуктивного здоровья ГБУЗ ЯО «Областной перинатальный центр», который принимает решение о направлении на программу ЭКО. Запись по телефону регистратуры (4852) 78-81-96.
⚡⚡⚡ Памятка для граждан о действиях в случае бессимптомного или легкого течения новой коронавирусной инфекции и острой респираторной вирусной инфекции (Скачать полную памятку, скачать короткую памятку)
Причина бесплодия — иммунитет — Вспомогательные репродуктивные технологии — Отделения
Статья была опубликована в журнале 9 месяцев №12 2004г.
Автор: Божедомов Владимир Александрович, Доктор медицинских наук, профессор, врач уролог-андролог высшей квалификационной категории.
Иммунной системе в обеспечении нормального репродуктивного процесса принадлежит важная роль. Нарушения в ее работе становятся причиной различных заболеваний: бесплодия, привычного выкидыша, патологии развития плода.
Функция иммунной системы — основные сведения.
Существование сложных многоклеточных организмов, в том числе человека, невозможно без нормальной работы иммунной системы. Иммунная система защищает от микроорганизмов, охотно паразитирующих внутри нашего тела, и собственных клеток, которые перестали выполнять свои функции и стали бесконтрольно размножаться. Такие клетки называют раковыми. Чтобы обеспечить эти задачи существуют специальные иммунокомпетентные клетки. Их делят на несколько классов: нейтрофильные гранулоциты, эозинофилы, макрофаги, Т-, В-, НК-лимфоциты и др. Они способны распознавать «чужаков» и убивать их. В борьбе с инфекциями участвуют так же иммуноглобулины (антитела). Они образуются после контакта иммунных клеток с микроорганизмом-паразитом и являются строго специфичными. Против каждого типа возбудителя образуются «свои» антитела, причем обычно нескольких видов. Они связываются с поверхностью проникших в организм паразитов, препятствуют их прикреплению к нашим клеткам и способствуют их быстрому уничтожению клетками-фагоцитами (пожирателями).
В борьбе с инфекциями участвуют так же иммуноглобулины (антитела). Они образуются после контакта иммунных клеток с микроорганизмом-паразитом и являются строго специфичными. Против каждого типа возбудителя образуются «свои» антитела, причем обычно нескольких видов. Они связываются с поверхностью проникших в организм паразитов, препятствуют их прикреплению к нашим клеткам и способствуют их быстрому уничтожению клетками-фагоцитами (пожирателями).
Чтобы уничтожить «чужих» иммунные клетки должны уметь отличать их от «своих». В основе такого распознавания лежат различия в структуре антигенов1 клеток. Наиболее важным для такого распознавания являются антигены т.н. главного комплекса гистосовместимости, которые у человека названы лейкоцитарными или HLA. Каждый человек имеет уникальный набор HLA–антигенов. Все типы клеток организма, которые имеются у младенца на момент рождения, считаются «своими», иммунные клетки на них в норме не реагируют. Все, что отличается – чужим. «Чужими» являются проникшие в организм бактерии и глисты, «чужими» становятся и свои клетки, если в них проник вирус или бактерия с внутриклеточным циклом развития (например, хламидия), или произошла их злокачестванная трансформация. «Чужими» для мужчин иногда оказываются их собственные сперматозоиды, для женщин – сперматозоиды, проникшие в половые пути, и даже развивающийся внутри материнского организма плод. Почему так происходит?
«Чужими» для мужчин иногда оказываются их собственные сперматозоиды, для женщин – сперматозоиды, проникшие в половые пути, и даже развивающийся внутри материнского организма плод. Почему так происходит?
Иммунологический контроль репродуктивной функции
Не все клетки организма доступны иммунным клеткам, циркулирующим в крови. Некоторые отделены специальными барьерами, например нейроны головного мозга – гемато-энцефалическим, клетки сперматогенеза в яичках – гемато-тестикулярным. Это связано с тем, что в процессе развития у некоторых клеток появляются белковые структуры (антигены), отсутствовавшие на момент рождения и в первые дни жизни. Например, сперматозоиды появляются у мальчиков в 11-13 лет и содержат элементы, необходимые для оплодотворения и ранее не контактировавшие с иммунными клетками. Поэтому на них может развиться иммунный ответ. Чтобы этого избежать, сперматозоиды развиваются в специальных трубочках – сперматогенных канальцах, — стенки которых пропускают кислород, гормоны, питательные вещества, но не позволяют контактировать с циркулирующими в крови иммунными клетками. На развивающихся сперматогенных клетках и зрелых сперматозоидах отсутствуют антигены HLA-комплекса. Кроме того, специальные клетки яичка вырабатывают особое вещество – Fas — которое вызывает быструю смерть (апоптоз)2 лимфоцитов, проникших в паренхиму яичка. В обеспечении иммуносупрессии[3] участвуют и клетки яичка, продуцирующие мужской половой гормон тестостерон – известно, что андрогены, как и другие стероидные гормоны, способны ослаблять иммунный ответ.
На развивающихся сперматогенных клетках и зрелых сперматозоидах отсутствуют антигены HLA-комплекса. Кроме того, специальные клетки яичка вырабатывают особое вещество – Fas — которое вызывает быструю смерть (апоптоз)2 лимфоцитов, проникших в паренхиму яичка. В обеспечении иммуносупрессии[3] участвуют и клетки яичка, продуцирующие мужской половой гормон тестостерон – известно, что андрогены, как и другие стероидные гормоны, способны ослаблять иммунный ответ.
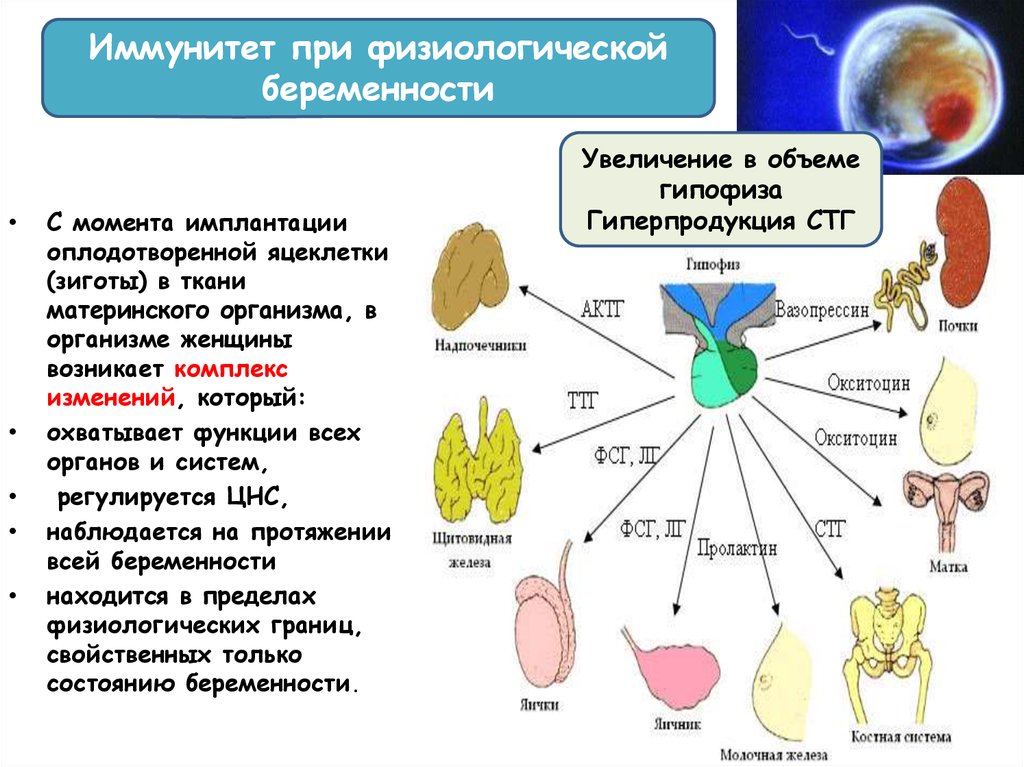
Иммунная система регулирует и течение физиологической беременности.
Беременность на первый взгляд напоминает в иммунологическом плане ситуацию, возникающую при трансплантации, поскольку плод содержит как антигены матери, так и «чужие» антигены отца. Известно, что после пересадки (трансплантации) одному человеку органов другого развивается иммунологический ответ против донорского органа. В основе конфликта – несовпадение HLA-антигенов донора и реципиента (получателя органа). Чтобы сохранить функцию трансплантата приходится пожизненно применять препараты, подавляющие иммунитет. Однако наблюдения и многочисленные эксперименты показывают, что иммунологическое распознавание чужеродного плода при физиологической беременности, в отличие от трансплантации органа, обычно не приводит к его отторжению.
Однако наблюдения и многочисленные эксперименты показывают, что иммунологическое распознавание чужеродного плода при физиологической беременности, в отличие от трансплантации органа, обычно не приводит к его отторжению.
В чем причины иммунологической привилегированности плода?
Во-первых, эмбрион и образующийся после внедрения в матку трофобласт[4] не имеет на своей поверхности высокоиммуногенных антигенов HLA. Кроме того, поверхность зародыша покрыта специальным слоем из сиаломуцина, защищающим от иммунного распознавания. Во-вторых, в организме женщины происходят сложные перестройки, в результате которых иммунная система вырабатывает меньше тех клеток, которые способны убивать «чужие» клетки, в т.ч. клетки плода, и вырабатывает больше антител. Многие из этих антител не только не повреждают развивающийся зародыш, но даже являются «блокирующими или защитными факторами», предотвращающими распознавание клетками-киллерами тканей плода.
Особый интерес вызывает иммунокоррегирующая функция плаценты. Многоядерный слой плаценты традиционно считают своеобразным «щитом» для плода. Одной из особенностей трофобласта является то, что клетки его наружной части на ранних сроках беременности не имеют на своей поверхности HLA-антигенов, а внутренний слой содержит нетрадиционный HLA-G. Предполагают, что данная форм HLA выполняет функцию «универсальной карты идентичности», позволяя клетке плода быть распознанной как не чужеродная, и избежать атаки специальных НК-лимфоцитов, которые убивают клетки, лишенные HLA. Кроме того, большие гранулярные лимфоциты в присутствии HLA-G продуцируют существенно меньшее количество различных провоспалительных цитокинов[5] (ФНО-a, ИФН-g и др.). Одновременно трофобласт секретирует b-2-микроглобулин, человеческий плацентарный белок-14, лактоген, а печень плода – a-фетопротеин, так же угнетающие пролиферативную активность Т-клеток. Как и клетки яичка, клетки плаценты продуцируют Fas, приводящий к локальной гибели лейкоцитов. Большие гранулярные лимфоциты материнской части трофобласта вырабатывают трансформирующий фактор роста-b, подавляющий активацию и пролиферацию цитотоксических клеток.
Многоядерный слой плаценты традиционно считают своеобразным «щитом» для плода. Одной из особенностей трофобласта является то, что клетки его наружной части на ранних сроках беременности не имеют на своей поверхности HLA-антигенов, а внутренний слой содержит нетрадиционный HLA-G. Предполагают, что данная форм HLA выполняет функцию «универсальной карты идентичности», позволяя клетке плода быть распознанной как не чужеродная, и избежать атаки специальных НК-лимфоцитов, которые убивают клетки, лишенные HLA. Кроме того, большие гранулярные лимфоциты в присутствии HLA-G продуцируют существенно меньшее количество различных провоспалительных цитокинов[5] (ФНО-a, ИФН-g и др.). Одновременно трофобласт секретирует b-2-микроглобулин, человеческий плацентарный белок-14, лактоген, а печень плода – a-фетопротеин, так же угнетающие пролиферативную активность Т-клеток. Как и клетки яичка, клетки плаценты продуцируют Fas, приводящий к локальной гибели лейкоцитов. Большие гранулярные лимфоциты материнской части трофобласта вырабатывают трансформирующий фактор роста-b, подавляющий активацию и пролиферацию цитотоксических клеток. Эти и ряд других механизмов обеспечивают подавление иммунологической реактивности материнского организма по отношению к развивающемуся плоду. Система антибактериального иммунитета, наоборот, активируется: увеличивается количество клеток-пожирателей (гранулоцитов и моноцитов) в периферической крови матери, наблюдаются признаки их активации. Это обеспечивает надежную защиту от микроорганизмов-паразитов в условиях снижения активности специфического клеточного иммунитета.
Эти и ряд других механизмов обеспечивают подавление иммунологической реактивности материнского организма по отношению к развивающемуся плоду. Система антибактериального иммунитета, наоборот, активируется: увеличивается количество клеток-пожирателей (гранулоцитов и моноцитов) в периферической крови матери, наблюдаются признаки их активации. Это обеспечивает надежную защиту от микроорганизмов-паразитов в условиях снижения активности специфического клеточного иммунитета.
Важную роль выполняют стероидные гормоны. Более полувека назад описано увеличение содержания в крови беременных женщин надпочечникового гормона кортизола, который способствует переключению клеточного цитотоксического иммунитета, способного уничтожать клетки плода, на гуморальный, при котором вырабатываются антитела. Повышение содержания гормона желтого тела прогестерона так же не только подготавливает матку к прикреплению зародыша, но и создает необходимую для этого иммуносупрессию, в частности, препятствуя синтезу простогландинов[6].
Иммунопатология созревания половых клеток, оплодотворения и беременности
Несмотря на надежную защиту развивающихся половых клеток иногда возникают ситуации, когда они подвергаются иммунной атаке. У мужчин наиболее частой причиной этого являются острые и тупые травмы яичек, сопровождающиеся разрывом семенных канальцев и капилляров. При этом антигены попадают в кровь и вызывают иммунный ответ. Если травма была сильной, аутоиммунный воспалительный процесс в яичке – орхит, — обычно захватывает весь орган и заканчивается его соединительно-тканным перерождением. Если повреждение было субклиническим, то за счет естественных регенераторных процессов целостность гемато-тестикулярного барьера восстанавливается и сперматогенез продолжается. Но специфические антиспермальные антитела (АСАТ), которые начали образовываться после травмы, продолжают циркулировать в сперме и крови и нарушают функцию мужских половых клеток. При этом объектом иммунной атаки оказываются все сперматозоиды, образовавшиеся как в травмированном, так и в здоровом яичке. В присутствии АСАТ снижается подвижность, происходит их агглютинация, оказывается практически невозможным прохождение через цервикальный канал в матку, нарушается акросомальная реакция[7], без чего невозможно оплодотворение яйцеклетки даже «в пробирке». Такая ситуация получила название «аутоиммунное мужское бесплодие». По различным данным, от 5 до 40% мужчин из бесплодных пар имеют АСАТ; по результатам наших исследований более чем у 20% мужчин причиной бесплодия являются аутоиммунные реакции против сперматозоидов. При этом нами было показано, что некоторые врожденные особенности строения половых органов, например варикоцеле[8], в несколько раз повышают риск развития иммунного бесплодия и орхита после субклинической травмы мошонки.
В присутствии АСАТ снижается подвижность, происходит их агглютинация, оказывается практически невозможным прохождение через цервикальный канал в матку, нарушается акросомальная реакция[7], без чего невозможно оплодотворение яйцеклетки даже «в пробирке». Такая ситуация получила название «аутоиммунное мужское бесплодие». По различным данным, от 5 до 40% мужчин из бесплодных пар имеют АСАТ; по результатам наших исследований более чем у 20% мужчин причиной бесплодия являются аутоиммунные реакции против сперматозоидов. При этом нами было показано, что некоторые врожденные особенности строения половых органов, например варикоцеле[8], в несколько раз повышают риск развития иммунного бесплодия и орхита после субклинической травмы мошонки.
Другой причиной развития антиспермального иммунитета являются урогенитальные инфекции. Принято считать, что одним из механизмов образования АСАТ на фоне инфекций является способность многих бактериальных, вирусных и грибковых организмов прикрепляться к мембране сперматозоидов и вызывать перекрестные реакции. Среди наиболее значимых следует назвать хламидии, микоплазмы, вирусы герпеса и папилломавируса. При диагностике вирусных инфекций прогностически наиболее важным является обнаружение возбудителя непосредственно в сперматозоидах, в меньшей степени — в мазке и специфических антител в крови.
Среди наиболее значимых следует назвать хламидии, микоплазмы, вирусы герпеса и папилломавируса. При диагностике вирусных инфекций прогностически наиболее важным является обнаружение возбудителя непосредственно в сперматозоидах, в меньшей степени — в мазке и специфических антител в крови.
Следует подчеркнуть, что не все антитела, вырабатывающиеся против антигенов сперматозоидов, представляют угрозу для их функции. Из более чем 40 антигенов сперматозоидов и семенной плазмы лишь для нескольких установлена связь с нарушением оплодотворяющей способности. Имеет значение, какие классы АСАТ имеются в сперме. Показано, что сперматозоиды утрачивают подвижность, когда АСАТ имеются на их хвостах, проникновение сперматозоидов в цервикальную слизь (ЦС) нарушено в присутствии АСАТ класса IgА, а степень нарушения оплодотворения яйцеклетки «в пробирке» пропорциональна проценту сперматозоидов, головки которых покрыты IgG. Поэтому остро стоит вопрос об адекватности результатов различных методов определения АСАТ в прогнозе фертильности.
АСАТ в цервикальной слизи у женщин встречаются в несколько раз чаще (30-40%), чем у мужчин. Имеются некоторые количества АСАТ и у фертильных женщин. Возможно, они участвуют в устранении неполноценных сперматозоидов. Когда АСАТ у женщин становится слишком много, они мешают оплодотворению. В половине случаев выработка у женщины собственных АСАТ является реакцией на попадание в половые пути спермы партнера, содержащей антитела, что делает сперму более иммуногенной. Кроме присутствия мужских АСАТ, антитела против сперматозоидов могут вырабатываться у женщин под действием различных факторов, например, при наличии урогенитальных инфекций, таких как грибы, хламидии или др., при увеличенном содержании лейкоцитов в сперме мужчин с неспецифическим бактериальным простатитом, при повышенном количестве сперматозоидов в сперме и т.д. Но в случае наличия АСАТ в сперме у постоянного партнера, особенно класса IgA, антиспермальные антитела в ЦС у женщин вырабатываются практически всегда, и это резко ухудшает прогноз на беременность.
Клиническим проявлением действия женских АСАТ является неспособность сперматозоидов проникать в ЦС. Это можно обнаружить при специальных лабораторных тестах, оценивающих взаимодействие сперматозоидов с ЦС.
Имеются многочисленные данные о снижении успеха программы ЭКО и ПЭ[9] когда АСАТ имеются не только в ЦС, но и в сыворотке крови женщин. При этом показано, что нарушение взаимодействия гамет в присутствии АСАТ зависит не столько от количества АСАТ (что важно в процессе проникновения через ЦС), сколько от разнообразия антител, взаимодействующих со специфическим антигеном (-ми). По некоторым данным АСАТ у женщин могут также оказывать вредное влияние на раннее развитие эмбриона, имплантацию и течение беременности. Статистически значимую корреляция между присутствием АСАТ IgG и хронологией привычного выкидыша показали многие исследователи. Была высказана точка зрения, что повышение чувствительности к антигенам сперматозоидов может активировать материнскую иммунную систему против отцовских антигенов, представленных на эмбрионе.
К активации иммунопатологических процессов, повышенному синтезу провоспалительных цитокинов может приводить длительное присутствие в матке условно-патогенных микроорганизмов и вирусов. Это служит препятствием для создания в предимплантационный период локальной иммуносупрессии, которая необходима для формирования защитного барьера. Поэтому инфекцию рассматривают как один из основных факторов развития привычного выкидыша: у женщин, страдающих невынашиванием, диагноз хронического воспаления эндометрия имеет место в 60-75% случаев.
Антифосфолипидный синдром (АФС) так же является одной из причин привычного выкидыша. Фосфолипиды являются важной составляющей всех биологических мембран, поэтому появление антифосфолипидных антител может расстроить функцию клеток, стать причиной развития воспалительной реакции, вызвать нарушения свертывания крови, следствием чего являются недостаточность кровообращения в плаценте, тромбозы кровеносных сосудов, инфаркты в плаценте. АФС обнаруживают у 27-31% женщин с привычным выкидышем. Полагают, что у женщин с АФС образование тромбов в плаценте обусловливает потерю плода в основном после 10 нед беременности. Частота АФС повышается на 15% с каждым следующим выкидышем. Таким образом, АФС является не только причиной, но и осложнением привычного невынашивания беременности.
Полагают, что у женщин с АФС образование тромбов в плаценте обусловливает потерю плода в основном после 10 нед беременности. Частота АФС повышается на 15% с каждым следующим выкидышем. Таким образом, АФС является не только причиной, но и осложнением привычного невынашивания беременности.
Предметом обсуждения являются аутоантитела к гормонам. Наиболее изученным является гормон ХГЧ[10]. Отечественными гинекологами показано. что у женщин с высоким уровнем антител к ХГЧ отмечается раннее (3-8 нед беременности) развитие хронической формы ДВС[11], что по-видимому, является одной из основных причин внутриутробной гибели эмбриона и плода.
Повышенные титры антител против ДНК обнаруживают у 22% женщин с привычным невынашиванием беременности и у 50% женщин с бесплодием. Аутоантитела к ДНК могут вызывать воспалительные изменения в плаценте и запускать реакцию отторжения плода. Обнаружение повышенного титра анти-ДНК-антител требует проведения полного скрининга по другим аутоантителам, поскольку это может быть связано с наличием других сопутствующих аутоиммунных заболеваний. Умеренно повышенные уровни анти-ДНК-антител в большинстве случаев не вызывают клинических проявлений вне беременности, и привычный выкидыш может быть единственным клиническим проявлением аутоиммунного процесса в организме.
Умеренно повышенные уровни анти-ДНК-антител в большинстве случаев не вызывают клинических проявлений вне беременности, и привычный выкидыш может быть единственным клиническим проявлением аутоиммунного процесса в организме.
Проявлением иммунологического конфликта матери и плода является гемолитическая болезнь плода. Она возникает, когда на эритроцитах плода имеется специфический антиген, полученный от отца и называемый резус-фактором, а у матери такой белок отсутствует (резус-отрицательная кровь). В результате у женщины могут начать вырабатываться антитела против эритроцитов плода, которые приводят к разрушению его эритроцитов. Поскольку в норме плод достаточно эффективно изолирован от иммунных клеток матери, такая реакция обычно развивается уже перед самыми родами или в момент родов, и плод не успевает пострадать. Опасность эти антитела будут представлять уже следующему резус-положительному плоду.
Еще одним иммунологическим осложнением является тромбоцитопения – повреждение под действием материнских антител тромбоцитов плода. Обычно при этом снижены вес плода, содержание в крови лейкоцитов и лимфоцитов. Установлено, что в 3 из 4 случаев это сопровождается наличием антител против отцовских HLA-антигенов плода.
Обычно при этом снижены вес плода, содержание в крови лейкоцитов и лимфоцитов. Установлено, что в 3 из 4 случаев это сопровождается наличием антител против отцовских HLA-антигенов плода.
Все описанные синдромы являются отражением гипериммунных состояний. Но последние годы появились данные, что причиной патологии беременности может явиться и отсутствие иммунологического распознавания матерью плода. Было показано, что женщины, близкие с мужем по HLA-антигенам, например родственники, страдают привычным выкидышем. Исследования HLA антигенов матери и плода при невынашивании беременности показали, что совпадающие с матерью по НLА антигенам II класса плоды отторгаются чаще всего. Оказалось, что развитие «терпимости» иммунной системы матери к плоду при беременности является разновидностью активного иммунного ответа, предполагающего на начальном этапе распознавание и активную переработку чужеродных антигенов. Сочетание уникальных качеств трофобласта с уникальными условиями иммунного микроокружения, в дальнейшем приводит к тому, что распознавание беременности организмом матери в норме включает не реакцию отторжения, а реакцию наибольшего иммунологического благоприятствования.
Бесплодный брак и неразвивающаяся беременность: что нужно сделать?
Диагностика иммунологических нарушений репродуктивной функции должна быть комплексной, к специалистам андрологу и гинекологу должны обращаться обязательно оба супруга. Обследование должно опираться на подробный анализ истории болезни, данные объективного осмотра и результаты современных лабораторных исследований. Лечение иммунологических нарушений репродуктивной функции должны проводить врачи, имеющие специализацию по иммунологии и достаточный опыт ведения таких больных.
Мужчинам: первым и обязательным этапом обследования является комплексное исследование спермы. Обнаружение АСАТ любым из лабораторных методов (MAR-тест, IBT-тест, ИФА/ELISA и др.) позволяет установить существование аутоиммунных реакций против сперматозоидов. Если АСАТ покрыты более 50% подвижных сперматозоидов ставится диагноз «мужское иммунное бесплодие». Дальнейшее обследование будет направлено на уточнение классов АСАТ, количества антител в сыворотке крови и на каждом сперматозоиде, прочности их связи с клетками, выраженности воспалительных реакций, существовании гормональных нарушений, сопутствующих нарушениях функции сперматозоидов (акросомальная реакция), степени нарушения проникновения в ЦС и т. д. Поскольку нередко причиной развития антиспермального иммунитета являются урогенитальные инфекции обязательно обследование на хламидии, микоплазмы, герпес и другие возбудители. При этом нужно помнить, что выявляемость этих микроорганизмов у мужчин даже при использовании современных методов диагностики, таких как ПЦР12, далеко не 100%.
д. Поскольку нередко причиной развития антиспермального иммунитета являются урогенитальные инфекции обязательно обследование на хламидии, микоплазмы, герпес и другие возбудители. При этом нужно помнить, что выявляемость этих микроорганизмов у мужчин даже при использовании современных методов диагностики, таких как ПЦР12, далеко не 100%.
Лечение мужского иммунного бесплодия базируется на данных об установленных причинах формирования данного состояния и может включать оперативные вмешательства, направленные на устранение непроходимости семявыносящего тракта и нарушений кровообращения, назначение различных гормональных и негормональных лекарственных препаратов, применения методов отмывки спермы для удаления антител с поверхности сперматозоидов с сохранением их функции. В данной области у нас имеется большой собственный опыт, отраженный в более чем в 10-и оригинальных Патентах на изобретения и 2-х Учебных пособиях для врачей. Нужно быть готовым к тому, что лечение может быть длительным. При отсутствии эффекта лечения в течение года может быть рекомендовано ЭКО и ПЭ с применением интроцитоплазматической инъекции сперматозоидов (ИКСИ).
При отсутствии эффекта лечения в течение года может быть рекомендовано ЭКО и ПЭ с применением интроцитоплазматической инъекции сперматозоидов (ИКСИ).
Женщинам: к развитию иммунологических нарушений так же часто приводят хронические воспалительные заболевания и генитальные инфекции, нередкой находкой является эндометриоз.
Для обнаружения АСАТ у женщин применяются пост-коитальный тест (ПКТ) и тест взаимодействия сперматозоидов с ЦС «на стекле» (проба Курцрока-Мюллера), непосредственное определение АСАТ методом непрямого MAR-теста, проточной цитофлуорометрии и др.
Привычный выкидыш, определяемый как 2 и более клинически обнаруженных потерь беременности на сроке до 20 недель, требует кариотипирования13 трофобраста: в основе 60-70% ранних самопроизвольных выкидышей лежит элиминация генетически неполноценного эмбриона; полезно так же определение динамики b-ХГЧ и прогестерона.
При обследовании пациенток с невынашиванием беременности в обязательном порядке должно проводиться исследование крови на аутоантитела. Как минимум должно проводиться определение антител к фосфолипидам, к ДНК и к факторам щитовидной железы. Важно отметить, что при привычном невынашивании беременности дополнительных симптомов аутоиммунных заболеваний может и не быть, а повышение уровня аутоантител в среднем бывает меньше, чем при манифестном течении аутоиммунных заболеваний.
Как минимум должно проводиться определение антител к фосфолипидам, к ДНК и к факторам щитовидной железы. Важно отметить, что при привычном невынашивании беременности дополнительных симптомов аутоиммунных заболеваний может и не быть, а повышение уровня аутоантител в среднем бывает меньше, чем при манифестном течении аутоиммунных заболеваний.
Важное диагностическое значение для диагностики иммунных форм невынашивания беременности имеет определение генотипа супругов по HLA-антигенам II класса. Желательно проведение фенотипирования по HLA-DR и -DQ антигенам. В современных условиях такое типирование проводится методом ДНК-диагностики. Для оценки степени распознавания аллоантигенов отцовского происхождения используется смешанная культура лимфоцитов (СКЛ).
Методы лечебных воздействий при иммунологических нарушениях репродуктивной функции у женщин зависят от характера нарушений, степени нарушений и общего состояния пациентки. Обычно лечения включает три этапа:
· общая иммунокоррекция и лечение сопутствующих заболеваний;
· подготовка к беременности;
· лечение во время беременности.
Обнаружение АСАТ в цервикальной слизи требует регулярного применения презервативов для исключения попадания спермы в половые пути и уточнения причин иммунных реакций против сперматозоидов: АСАТ у мужа, инфекции, гормональные нарушения и др. Лечение включает меры специфического и неспецифического характера, в качестве дополнительного способа лечения может быть рекомендована внутриматочная инсеминация отмытой спермой мужа. При обнаружении значимых количеств АСАТ в сыворотке крови лечение может потребовать продолжительно периода, инсеминации и ЭКО до нормализации количества АСАТ не рекомендуются.
Общая иммунокоррекция и лечение сопутствующих заболеваний направлено на устранение иммунодефицитного состояния, выявленного при обследовании пациентки, лечение воспалительных заболеваний половых органов и генитальных инфекций, устранение дисбактериоза кишечника и влагалища, проведение общеукрепляющего лечения и психологической реабилитации. При этом нужно иметь в виду, что в настоящее время несмотря на довольно значительное количество препаратов, обладающих иммуномодулирующими свойствами, их применение у беременных резко ограничено. По-прежнему активно применяется иммуноцитотерапия – введение беременной лимфоцитов мужа или донора. В развитие этого метода большой вклад внесли отечественные ученые В.И.Говалло и В.М.Сидельникова. Метод может успешно применяться как при избыточных реакциях иммунной системы матери против плода, так и при совпадении генотипа супругов по HLA.
По-прежнему активно применяется иммуноцитотерапия – введение беременной лимфоцитов мужа или донора. В развитие этого метода большой вклад внесли отечественные ученые В.И.Говалло и В.М.Сидельникова. Метод может успешно применяться как при избыточных реакциях иммунной системы матери против плода, так и при совпадении генотипа супругов по HLA.
Наиболее успешным лечение невынашивания беременности бывает тогда, когда иммунологическая подготовка к беременности начинается как минимум за месяц до прекращения предохранения. Конкретные лечебные мероприятия определяет врач-гинеколог. Независимо от исходных нарушений, после наступления беременности большое значение имеет периодическое исследование показателей гемостаза и анализа крови на аутоантитела с проведением адекватной коррекции в случае обнаружения отклонений.
Собственный опыт и данные научной литературы свидетельствуют, что бесплодие и осложнения беременности, связанные с нарушением регулирующей функции иммунной системы, в настоящее время в большинстве случаев излечимы.
Что происходит с иммунной системой во время беременности?
Исследования показывают, что иммунная система занимает центральное место в контроле над беременностью. Однако вирусы и бактерии могут его перехитрить, что иногда приводит к плачевным последствиям.
Поделиться на PinterestСчиталось, что подавление иммунной системы необходимо для беременности.Во время беременности иммунная система матери находится в постоянном движении.
Хотя в настоящее время широко признано, что существует точно настроенное взаимодействие между клетками матери и плода для поддержания здоровой беременности, во многих исследованиях для изучения этого использовались мышиные модели, но мыши — это не люди.
Новое исследование, опубликованное на этой неделе в журнале Science Immunology , проливает новый свет на то, как иммунная система человека меняется по мере развития беременности.
В ходе исследования д-р Брис Годильер, доцент кафедры анестезиологии, периоперационной и обезболивающей медицины в Исследовательском центре недоношенности March of Dimes Стэнфордского университета в Калифорнии, вместе с коллегами построили комплексную модель поведения иммунных клеток человека во время операции. нормальная беременность. Тем не менее, их долгосрочные амбиции заключаются в том, чтобы исследовать это еще глубже.
нормальная беременность. Тем не менее, их долгосрочные амбиции заключаются в том, чтобы исследовать это еще глубже.
Д-р Gaudilliere планирует провести аналогичное исследование с женщинами, перенесшими преждевременные роды, чтобы выяснить, сможет ли команда определить конкретные изменения, которые могут действовать как ранние предупреждающие признаки.
По данным Всемирной организации здравоохранения (ВОЗ), преждевременные роды, которые определяются как рождение до 37 недель беременности, являются основной причиной смерти детей в возрасте до 5 лет. В 2015 году это привело к почти 1 миллиону смертей во всем мире.
В Соединенных Штатах частота преждевременных родов составляет 10 процентов. И во всем мире число преждевременных родов растет. Те, кто выживает, могут столкнуться с осложнениями на всю жизнь.
Но почему иммунная система играет такую большую роль во время беременности? И как это связано с преждевременными родами?
В течение многих лет процесс беременности сравнивали с трансплантацией органов, как объясняет доктор Гил Мор, профессор акушерства, гинекологии и репродуктивных наук в Йельской школе медицины в Нью-Хейвене, штат Коннектикут, и его коллеги. недавняя статья опубликована в журнале Nature Reviews Immunology .
недавняя статья опубликована в журнале Nature Reviews Immunology .
Ученые считали, что материнская иммунная система должна подавляться на протяжении всей беременности, чтобы предотвратить отторжение плода. В качестве доказательства этой теории было принято присутствие множества иммунных клеток в месте имплантации эмбриона.
Предполагается, что эти клетки борются с чужеродными эмбриональными клетками, которые, в свою очередь, пытаются подавить этот иммунный ответ. Если бы эмбриональные клетки одержали верх, имплантация могла бы продолжаться. Но борьба продолжалась на протяжении всей беременности.
Если этот процесс не был успешным, считалось, что это может привести к выкидышу или преждевременным родам.
Однако исследования, проведенные впоследствии, показали, что присутствие или рекрутирование иммунных клеток не является реакцией на инородное тело, а является необходимым условием для успешной имплантации.
И это еще не все; в настоящее время считается, что взаимодействие между клетками плода и иммунным ответом матери является критическим компонентом на протяжении всей беременности.
Чтобы позволить развивающемуся эмбриону имплантироваться, некоторые из его клеток активно внедряются в слизистую оболочку матки. Это приводит к воспалительному каскаду, подобному тому, что происходит при заживлении ран.
Если предотвратить возникновение воспаления, имплантация не может продолжаться, что подчеркивает важность воспалительных молекул и клеток в этом процессе.
Эта провоспалительная среда преобладает в течение первых 12 недель беременности. В течение следующих 15 недель развивающийся плод находится в состоянии быстрого роста и развития. Преобладают противовоспалительные клетки и молекулы.
Некоторые клетки плода экспрессируют маркеры клеточной поверхности или антигены, происходящие от отца. В нормальных условиях иммунная система матери распознает их как чужеродные и атакует клетки.
Регуляторные Т-клетки (Treg), представляющие собой особую форму лейкоцитов, которые способствуют противовоспалительной среде, активно защищают такие клетки плода.
Низкий уровень Treg связывают с невынашиванием беременности.
На последней стадии беременности иммунная система снова переходит в провоспалительное состояние. Без этого мать не может начать роды. Преждевременные роды, в свою очередь, могут быть связаны с аномальными иммунными реакциями.
На поведение иммунной системы во время беременности влияет множество факторов, и ученые все чаще полагают, что микробиом матери играет определенную роль.
В течение многих лет считалось, что первую дозу микробов ребенок получает при рождении. Однако недавние исследования обнаружили микроорганизмы в первом стуле ребенка, а это означает, что некоторая передача микробных видов от матери к плоду произошла до рождения ребенка.
Однако не только живые микробы могут играть роль в развитии плода; фрагменты микробов и продукты микробного пищеварения могут переноситься через плаценту.
Доктор Эндрю Макферсон, профессор медицины и заведующий отделением гастроэнтерологии в университетской больнице Берна в Швейцарии, и его коллеги объясняют в недавней статье, опубликованной в журнале Nature Reviews Immunology , что этот процесс может иметь решающее значение для иммунной системы. системы новорожденного.
системы новорожденного.
Поделиться на PinterestГенетически модифицированные мыши и бактерии позволяют исследователям обратить внимание на роль микробиома в иммунитете.
Мыши, содержащиеся в стерильных условиях, не имеют иммунной системы. Используя хитроумную генную инженерию, доктор Макферсон и его команда смогли подвергнуть беременных мышей воздействию бактерий Escherichia coli в течение ограниченного периода времени.
К тому времени, когда мыши родили, они снова были обеззаражены, и, следовательно, они не передавали никаких E. coli своему потомству.
Мыши, рожденные таким образом, имеют повышенный уровень антибактериальных молекул в кишечнике, более развитые иммунные клетки и более зрелый метаболизм.
Однако не все так радужно; В некоторых случаях микробы могут нанести вред здоровью плода.
У доктора Мор есть теория о вирусах. Он считает, что они сводят на нет полезные эффекты, которые обеспечивает нормальный микробиом, подвергая риску и мать, и плод.
Согласно этой «гипотезе двойного удара», вирусы деактивируют иммунные сигнальные процессы, которые имеют решающее значение для взаимодействия между иммунной системой и бактериями. Это подвергает мать риску бактериальной инфекции в дополнение к вирусу, уже находящемуся в организме.
Используя модель мыши, его команда показала, что воздействие обычного бактериального токсина в дополнение к вирусной инфекции приводит к преждевременным родам.
Фактически, 40 процентов преждевременных родов у людей связаны с той или иной формой инфекции.
Доктор Мор также указывает на доказательства связи вирусных и бактериальных инфекций во время беременности с повышенным риском развития у ребенка шизофрении, расстройств аутистического спектра и аллергии в более позднем возрасте.
В чем может быть причина? Ученые считают, что в необратимом повреждении плода виноват высокий уровень активации иммунной системы матери в ответ на инфекцию.
Доктор Мор и его команда показали, что даже если инфекция не передается напрямую от матери, в таких случаях уровень воспалительных маркеров у плода резко возрастает. В исследованиях на мышах это сопровождается аномалиями развития.
В исследованиях на мышах это сопровождается аномалиями развития.
Своим новым исследованием доктор Годильер и его коллеги дополняют существующую совокупность знаний о том, какие из различных популяций иммунных клеток присутствуют во время беременности.
В исследовании приняли участие 18 женщин, имевших нормальное течение беременности и сдавших образцы крови в течение каждого из триместров, а также через 6 недель после родов.
Поделиться на PinterestНовый анализ крови может помочь выявить тех, кто подвергается наибольшему риску преждевременных родов.
Используя технику, называемую масс-цитометрией, исследователи смогли получить из этих образцов множество информации, в том числе, какие клетки присутствовали в крови, как они реагировали на соединения, подобные вирусам и бактериям, и какие сигнальные пути были наиболее активными. активный.
Включив эту информацию в расширенную статистическую модель, команда смогла построить сложную карту того, как иммунная система адаптируется во время беременности.
Следующим в списке следует сравнительное исследование с использованием образцов крови женщин, родивших преждевременно, чтобы увидеть, сопровождаются ли это последовательными изменениями в иммунной системе.
Команда надеется использовать эти знания для разработки анализа крови, который может указывать на риск преждевременных родов у матери.
«Мы особенно заинтересованы в более точном понимании того, что происходит на очень ранних и очень поздних сроках беременности», — объясняет д-р Годильер. «Мы хотели бы увидеть, действительно ли есть переключатель, который мы можем поймать, золотую середину, где отклонение от нормы будет максимальным с патологией».
«Иммунная система не действует изолированно, и сейчас мы очень заинтересованы в анализе ее взаимодействия с другими аспектами биологии матерей, такими как их генетика, метаболизм и микробные сообщества организма, чтобы получить целостную картину. биологические часы беременности».
Ведущий автор исследования Нима Агаипур, доктор философии.
Существует множество доказательств того, что западная диета и современный образ жизни пагубно влияют на микробных пассажиров, которые неразрывно связаны с нашим здоровьем.
Уменьшение микробного разнообразия связано с целым рядом заболеваний. Остается один вопрос: влияет ли это на иммунную систему во время беременности.
Повышает ли низкое микробное разнообразие риск выкидыша или преждевременных родов?
Только время покажет. Однако ясно, что исследователи используют новые и инновационные инструменты, чтобы пролить свет на связь между нашей иммунной системой, теми факторами, которые на нее влияют, и здоровьем матери и ребенка во время и после беременности.
Как беременность влияет на вашу иммунную систему? Объяснение экспертов
Беременность
EmirMemedovski/E+/Getty Images
Да, есть причина, по которой вам так противно.
на Эшли Джонс
Если вы когда-либо болели во время беременности, вы хорошо знаете, как подхватив любой небольшой вирус, вы можете почувствовать, что вас буквально запустили на грузовике. Вялость, ломота, боль и прямая неприязнь всего этого просто сокрушают душу. Затем ваш малыш вырывает кишки, но ваше тело пропускает именно эти микробы. Что дает? Как именно беременность влияет на вашу иммунную систему? Как оказалось, есть причина, по которой простая простуда может заставить вас чувствовать себя так, будто на вас напало стадо антилоп, но в другие дни вы чувствуете себя совсем как Суперженщина.
«Во время беременности иммунная система меняется, чтобы обеспечить защиту как матери, так и ребенка от болезней», — говорит акушер-гинеколог Нили Элиша из Inspira Medical Group. «Одни части иммунной системы усиливаются, а другие подавляются. Этот баланс может предотвратить заражение ребенка без ущерба для здоровья матери».
По сути, ваше тело находится в центре гигантской ситуации, когда ваша иммунная система обеспокоена на протяжении всей беременности. «В частности, иммунная система матери подавляется, поэтому ее организм не идентифицирует плод как чужеродное существо и не пытается отвергнуть ребенка», — объясняет Элиша.
Как меняется ваша иммунная система во время беременности
Поскольку беременность влияет на все ваше тело, изменения, которые вы испытываете, широко распространены и будут меняться на протяжении всей беременности. То же самое касается реакции вашей иммунной системы на беременность. «Широко признано, что иммунная система подавляется на одних фазах, но на других фазах перегружается очень специфическими способами», — говорит доула и эксперт по родам Сара Лайон. «Помимо физиологии беременности, существуют анатомические изменения, которые делают беременных женщин более восприимчивыми к некоторым вирусным инфекциям, таким как ИМП и пневмония, как из-за повышенного структурного давления, так и из-за снижения емкости — ребенок и окружающие его органы занимают много места!»
На ранних сроках беременности ослабленная иммунная система может сделать вас более восприимчивыми к некоторым вирусным заболеваниям. «Во время беременности уровни эстрогена и прогестерона меняются», — говорит Элиша Ромпер. «В первом триместре изменения в этих гормонах делают беременную женщину более восприимчивой к таким инфекциям, как грипп и простуда».
«Во время беременности уровни эстрогена и прогестерона меняются», — говорит Элиша Ромпер. «В первом триместре изменения в этих гормонах делают беременную женщину более восприимчивой к таким инфекциям, как грипп и простуда».
Подобно остальному телу во время беременности, эксперты могут с уверенностью сказать, что ваша иммунная система претерпевает множество изменений во время беременности. Но Лайон объясняет, что «как и во многих перинатальных переживаниях, у нас есть нечеткое представление об иммунной системе во время беременности». Вот почему во время беременности трудно определить, как вы будете себя чувствовать день ото дня.
«Иммунная система — это не монолит — это сложная система химических и физических структур, которые постоянно адаптируются к нашим обстоятельствам», — объясняет Лайон Ромпер. «Имея это в виду, думайте об иммунной системе как о распределительном щите. Во время беременности и во время беременности существует постоянно меняющийся баланс подавления и усиления, который делает иммунную систему каждой женщины более уязвимой для одних патогенов и менее уязвимой для других».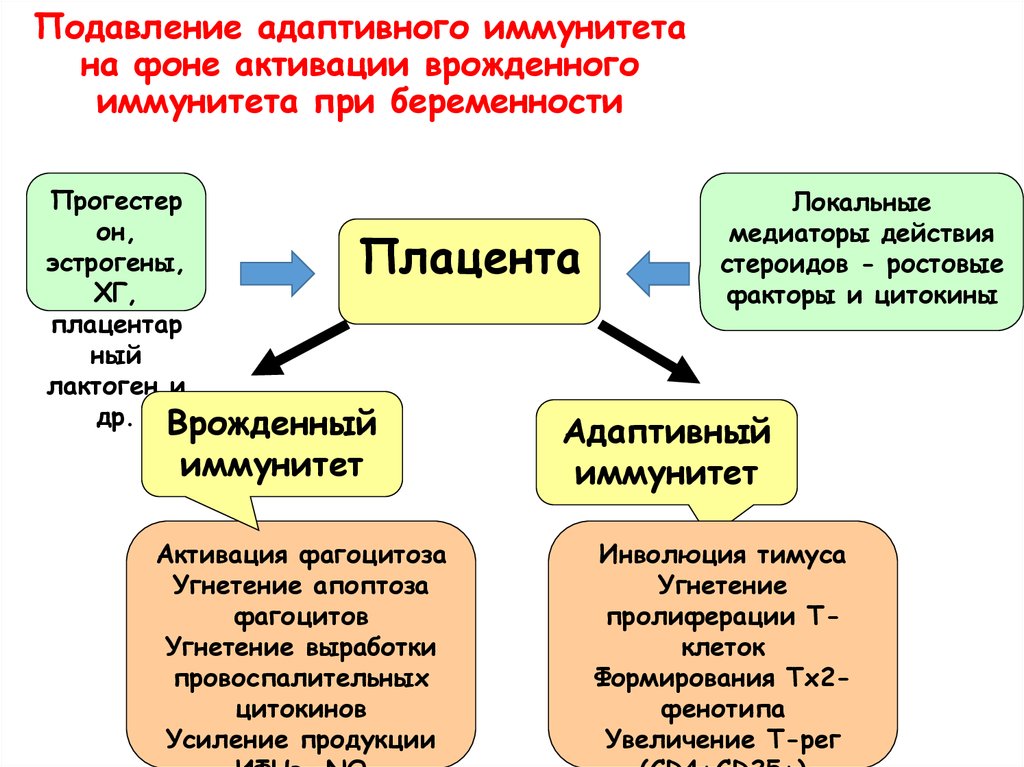
Как поддержать иммунную систему во время беременности
Чтобы обеспечить безопасность и здоровье вас и вашего ребенка на протяжении всей беременности, Элиша говорит, что важно поддерживать свою иммунную систему большим количеством отдыха, сбалансированной диетой и витаминами для беременных. «Мы также рекомендуем сделать прививку надлежащим образом, чтобы сделать себя менее восприимчивым к инфекции», — продолжает она. «Мы рекомендуем делать прививку от гриппа в сезон гриппа — с декабря по март — и прививку Tdap — от столбняка, дифтерии, коклюша — в течение третьего триместра. Кроме того, вакцина против коронавируса безопасна для будущих мам и может помочь передать иммунитет ребенку».
Мытье рук, держитесь подальше от больных людей и не пользуйтесь общими вещами, такими как посуда и стаканы для питья, также может помочь предотвратить болезнь и защитить вашу иммунную систему от более серьезного удара во время беременности. Если вы начинаете замечать признаки ослабления иммунной системы во время беременности, такие как чрезмерная вялость, заложенность носа, головокружение или обезвоживание, обратитесь к своему лечащему врачу.