Содержание
Причины и симптомы неразвивающейся беременности
Неразвивающаяся беременность (замершая беременность) – это патологическое состояние, при котором плод прекращает свое развитие и погибает, но при этом отсутствуют клинические симптомы выкидыша. Согласно статистике, неразвивающаяся беременность встречается в 20% случаев. Стоит отметить, что неразвивающаяся беременность на ранних сроках – одна из причин самопроизвольных выкидышей в первом триместре (45-88%). Стоит отметить, что первые недели являются кризисными периодами, поэтому неразвивающаяся беременность на ранних сроках встречается чаще всего.
Причины неразвивающейся беременности
Причины неразвивающейся беременности разнообразны. В гинекологической практике в большинстве случаев невозможно выделить конкретный фактор, который может привести к подобной патологии. Специалисты выделяют следующие причины неразвивающейся беременности, которые имеют ведущее значение:
- Инфекции;
- Хромосомные аномалии;
- Расстройства иммунитета;
- Гормональные нарушения.

Инфекционный фактор – ведущая причина неразвивающейся беременности. Длительное нахождение микроорганизмов в полости матки может вызвать формирование или усиление патологических состояний половых органов, привести к нарушениям гемодинамики и обмена веществ, что может стать причиной прекращения развития и роста плода. Ученые доказали, что инфекция становится в 1-2% причиной неразвивающейся беременности, последствиями которой становятся врожденные аномалии плода, несовместимые с жизнью.
Стоит отметить, что не каждая беременность, развивающаяся на фоне инфекции, заканчивается трагически, к тому же степень повреждения эмбриона может быть разной. Все зависит от пути проникновения микробов, вовлечения в процесс околоплодных вод и плаценты, вида и количества организмов, длительности заболевания и других факторов. Выделяют следующие группы микроорганизмов, которые с большей степенью вероятности становятся
- Условно-патогенные микробы: стрептококки, стафилококки, кишечная палочка, клебсиелла и другие;
- Вирусы: вирусы краснухи и Коксаки, ЦМВ, ВПЧ, аденовирус;
- Патогенные микробы: микоплазма, хламидия, бледная трепонема;
- Простейшие: токсоплазмы, грибы и другие.

Восходящий путь инфицирования эмбриона является частой причиной неразвивающейся беременности на ранних сроках, которая может привести к частичному разрыву плодных оболочек, заражению околоплодных вод. В результате эмбрион заглатывает инфицированную жидкость, поражающую легкие, пищеварительную систему, мочевыделительные органы, кожные покровы, что в результате приводит к гибели плода. Нисходящий путь инфицирования также может стать причиной неразвивающейся беременности, последствиями такого процесса становятся патология плаценты, поражение околоплодных вод и органов плода и, как результат, его гибель.
Инфекционные агенты, как причины неразвивающейся беременности, могут оказывать не только прямое влияние на ткани плода и плаценту, но и вызывать неадекватный иммунный ответ. Это может стать причиной неразвивающейся беременности, последствия которой будут заключаться в гибели эмбриона.
Научно доказанная причина неразвивающейся беременности – хромосомные аномалии. Гибель плода может быть вызвана неправильным развитием зиготы, структурными изменениями плаценты, генетическими аномалиями органов и систем.
Генетические аномалии — причины неразвивающейся беременности, последствия которых связаны не только с интенсивностью мутации хромосом, но и эффективностью их отбора. Чем выше возраст родителей, тем хуже процесс отбора, поэтому аномалии и пороки развития — частые явления.
Неблагоприятные внешние факторы также могут вызвать генетические нарушения. В 60% случаев ведущей причиной неразвивающейся беременности в ранние сроки являются бластопатии. В 15% случаев грубые хромосомные аномалии — причины неразвивающейся беременности, последствия которых — пустые зародышевые мешки.
Эндокринная патология – это одна из причин неразвивающейся беременности, последствия которой основаны на недостаточной имплантации эмбриона, неполноценности плаценты, расстройствах маточно-плацентраного кровообращения, недостаточности прогестерона и других нарушениях.
Аутоиммунные причины неразвивающейся беременности, последствия которых связаны с тяжелыми нарушениями кровотока, дефектами имплантации плода, усиленной атакой клеток эмбриона, в 90-95% случаев заканчиваются гибелью плода на ранних сроках.
Также в группу риска с возможным формированием неразвивающейся беременности, входят женщины:
- с множественными абортами в прошлом;
- с внематочными беременностями;
- старше 30 лет при первой беременности;
- с анатомически особенным строением матки (двурогая, седловидная и т.п.).
Патогенез неразвивающейся беременности
Неразвивающаяся беременность в первые дни протекает как нормальная, вначале происходит имплантация эмбриона, иногда даже успевает сформироваться плацента, но после этого под воздействием неблагоприятных внешних и внутренних факторов плод погибает. Но, несмотря на неразвивающуюся беременность, матка продолжает расти и выкидыша не происходит, хотя со временем происходит отслойка плаценты и отторжение плода.
Основным механизмом формирования неразвивающейся беременности на ранних сроках является остановка фето-плацентраного кровообращения на фоне сохранения маточно-плацентраного. Также неразвивающаяся беременность может образоваться в результате обратного развития эндометрия, так как желтое тело полностью распадается, формируются новые фолликулы, которые, воздействуя на внутреннюю оболочку полости матки, видоизменяют ее, и она приобретает признаки эндометрия в фазе пролиферации.
Симптомы неразвивающейся беременности
Клинические признаки неразвивающееся беременности, к сожалению, появляются уже после гибели плода, когда нельзя изменить ситуацию, хотя патологическое состояние можно предупредить, если тщательно спланировать свою беременность и прислушиваться к своему организму. В принципе, женщина при данной патологии чувствует себя беременной, но при этом может отмечать некоторые нарушения. Некоторые и вовсе не замечают признаки неразвивающейся беременности, так как не следят за своим здоровьем и ведут неправильный образ жизни.
У некоторых женщин признаки неразвивающейся беременности на ранних сроках могут быть яркими и отчетливыми, у других субъективные признаки неразвивающейся беременности на ранних сроках могут полностью отсутствовать, и патология регистрируется на основании различных методов обследования.
Чтобы вовремя распознать подобное состояние, необходимо знать основные симптомы неразвивающейся беременности:
- изменение уровня ХГЧ при неразвивающейся беременности: ХГЧ – это гормон, продуцирующийся за счет эмбриона, динамика этого вещества может многое сказать о состоянии плода и течении беременности. ХГЧ в первые дни увеличивает свою концентрацию в 2-4 раза каждый день, достигая максимума на 10-12 неделе, затем постепенно снижается. Концентрация ХГЧ при неразвивающейся беременности меняется по-другому. ХГЧ при неразвивающейся беременности, как правило, медленно понижается;
- отсутствие роста матки – частый признак неразвивающейся беременности: этот симптом неразвивающейся беременности может отметить только ваш лечащий врач во время осмотра, иногда отмечается несоответствие размеров матки сроку беременности.
 Признак неразвивающейся беременности на поздних сроках – низкое расположение дна матки;
Признак неразвивающейся беременности на поздних сроках – низкое расположение дна матки; - исчезновение неприятных симптомов (токсикоза и т.п.): если у женщины был ярко выражен токсикоз на первых неделях, то основным признаком неразвивающейся беременности на ранних сроках является резкое исчезновение тошноты и рвоты, улучшение общего состояния, связанное с гибелью плода;
- Мягкие и безболезненные молочные железы – еще один ранний симптом неразвивающейся беременности;
- Кровяные выделения: не всегда кровянистые и мажущие выделения могут быть признаком неразвивающейся беременности на ранних сроках, этот симптом должен всегда настораживать женщину, поэтому при его появлении следует обратиться к врачу как можно раньше;
- Болезненные ощущения внизу живота – это тревожный признак и один из симптомов неразвивающейся беременности;
- Уменьшение базальной температуры: раньше гинекологи придавали огромное значение уровню базальной температуры, сегодня этот метод не является точным, хотя её снижение может быть косвенным признаком неразвивающейся беременности на ранних сроках;
- УЗ признаки неразвивающейся беременности: наиболее информативный лабораторный признак неразвивающейся беременности – отсутствие сердцебиения плода.
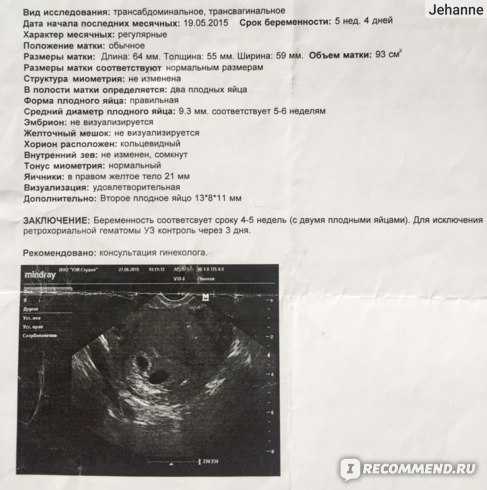
- Отсутствие шевелений плода – с 18-20 недели женщина может ощутить движения эмбриона, если их нет, то это может быть признаком неразвивающейся беременности.
Диагностика неразвивающейся беременности
Заподозрить наличие патологии можно при наличии признаков неразвивающейся беременности. Косвенные признаки неразвивающейся беременности на ранних сроках — болезненные ощущения, мажущие кровяные выделения. Поэтому если вы определили у себя подобные симптомы, незамедлительно обратитесь к врачу.
Первоначально врач проводит гинекологический осмотр с целью определения размеров матки, если они не совпадают со сроком, то есть риски формирования неразвивающейся беременности. Для того, чтобы уточнить признаки неразвивающейся беременности на ранних сроках, гинеколог назначает дополнительные методы исследования: УЗИ и доплерографию.
По УЗИ можно выделить несколько симптомов неразвивающейся беременности, которые определяют на ранних этапах после гибели эмбриона: отсутствие плодного яйца (анэмбриония), плод очень маленького размера и без признаков сердцебиения, иногда определяется плод обыкновенных размеров, но без признаков жизнедеятельности, нередко определяют аномалии и пороки развития эмбриона, повреждения, несовместимые с жизнью.
Поздние УЗ симптомы неразвивающейся беременности, которые определяют после длительного нахождения погибшего плода в полости матки: строение плодного яйца сильно изменено, возможно появление множественных перетяжек и эхоструктур, очагов некроза, маловодие или многоплодие.
Последствия неразвивающейся беременности
Последствия неразвивающейся беременности могут быть разными. Часто на фоне патологии наблюдается ареактивность матки, когда она не отторгает погибший плод, при этом он задерживается в ней на долгое время.
Частым последствием неразвивающейся беременности является постепенное отторжение плодного яйца, что ведет к появлению мажущих выделений и исчезновению симптомов беременности. Грозное последствие неразвивающейся беременности при длительном нахождении погибшего эмбриона (более 4 недель) – аутолиз и формирование ДВС-синдрома, что может привести к тяжелым нарушениям кровообращения. К тому же длительное присутствие погибшего плода может закончиться серьезными воспалительными реакциями со стороны матки и ее придатков, что может отразиться на дальнейшем здоровье женщины и стать серьезным последствием неразвивающейся беременности. Стоит отметить, что гибель плода на поздних сроках нередко заканчивается сепсисом, перитонитом, поэтому последствия неразвивающейся беременности нельзя недооценивать. Также одним из последствий неразвивающейся беременности могут стать трудности во время хирургических манипуляций по удалению погибшего эмбриона.
Стоит отметить, что гибель плода на поздних сроках нередко заканчивается сепсисом, перитонитом, поэтому последствия неразвивающейся беременности нельзя недооценивать. Также одним из последствий неразвивающейся беременности могут стать трудности во время хирургических манипуляций по удалению погибшего эмбриона.
Лечение неразвивающейся беременности
Длительное нахождение погибшего эмбриона в полости матки представляет серьезную угрозу жизни и здоровью матери, поэтому, если подтвердился диагноз, то отдают предпочтение хирургическому лечению неразвивающейся беременности, так как консервативное ведение пациентки неэффективно и небезопасно. В принципе, лечение неразвивающейся беременности предусматривает проведение аборта по медицинским показаниям, который может быть выполнен во время операции или после приема лекарственных препаратов.
Перед проведением оперативного лечения неразвивающейся беременности женщине необходимо сдать анализы и пройти мероприятия, направленные на снижение риска возможных осложнений. Также лечение неразвивающейся беременности подразумевает назначение противовоспалительных и антибактериальных препаратов, витаминов, гормональных средств и других медикаментов по показаниям.
Также лечение неразвивающейся беременности подразумевает назначение противовоспалительных и антибактериальных препаратов, витаминов, гормональных средств и других медикаментов по показаниям.
Помимо удаления погибшего эмбриона, лечение неразвивающейся беременности заключается в анализе патологического состояния для выяснения причин его формирования, нормализации общего состояния, чтобы в будущем предотвратить формирование подобных состояний. А самое главное, лечение неразвивающейся беременности невозможно без восстановления психического состояния пациентки.
Новая беременность после неразвивающейся беременности
Планировать новую беременность после неразвивающейся беременности рекомендуется не раньше, чем через 3 месяцев после лечения (оптимально 6 месяцев). Этот срок необходим для восстановления организма женщины для полноценной беременности после неразвивающейся беременности, если им пренебречь, то исход может быть неблагоприятным.
К тому же, приступать к планированию беременности после неразвивающейся беременности можно после пройденного курса лечения: восстановления гормонального фона, устранения нарушений иммунитета и инфекции и т.
Бесплатный прием репродуктолога
по 30 апреля 2023
Осталось 10 дней
Уважаемые пациенты! Клиника «Центр ЭКО» приглашает вас на бесплатный прием репродуктолога с проведением УЗИ и составлением плана лечения.
Начните свой путь к счастью — прямо сейчас!
Имя *
Телефон *
E-mail *
Сообщение *
Отправляя данную форму, я подтверждаю, что в соответствии с требованиями “Федерального закона О персональных данных № 152-ФЗ” и в соответствии с Условиями даю согласие на обработку моих персональных данных
Leave this field blank
Искусственное оплодотворение: что это такое и как его проводят?
Читать статью
Что можно и чего нельзя после ЭКО?
Читать статью
Неразвивающаяся (замершая) беременность.
 Причины и признаки.
Причины и признаки.Зачатие ребенка не всегда приводит к успешным родам. Есть много разных патологий, которые прерывают этот процесс. Среди них часто встречается замершая беременность. При этом в полости матки остаются мертвые ткани, способные вызвать воспалительные и другие заболевания. Важно регулярно посещать врача, чтобы вовремя заметить нарушение и провести своевременное лечение.
Что это такое
Если у женщины диагностирована беременность, но в какой-то период она перестала развиваться, то такую патологию называют замершей беременностью. В этом случае возникает гибель плода, которая сопровождается определенными симптомами. Также можно встретить другое название подобного нарушения – несостоявшийся выкидыш. То есть плод погиб, все процессы его жизнедеятельности остановились, но выкидыша как такового не случилось, и ткани остались в матке.
К неразвивающейся беременности относят и анэмбрионию – отсутствие плода в околоплодном яйце. Зародыш мог отсутствовать там с самого начала или погибнуть в течение 2 – 3 недель после зачатия. При этом плодное яйцо растет, вырабатывается ХГЧ, происходят другие процессы, указывающие на нормальную беременность. Если сделать тест, то он будет положительным. Однако со временем клетки плодного яйца перестают делиться, и его развитие замирает.
Зародыш мог отсутствовать там с самого начала или погибнуть в течение 2 – 3 недель после зачатия. При этом плодное яйцо растет, вырабатывается ХГЧ, происходят другие процессы, указывающие на нормальную беременность. Если сделать тест, то он будет положительным. Однако со временем клетки плодного яйца перестают делиться, и его развитие замирает.
Наиболее часто такая проблема возникает у женщин в возрасте ближе к тридцати годам и старше. Однако даже молодые девушки не застрахованы от этой патологии.
Опасные сроки
Беременность может замирать в первом и втором триместре. Чаще всего остановка развития зародыша случается на 3 – 4 или 8 – 11 неделе. Реже патологию диагностируют в ситуации, когда эмбрион уже более сформирован и женщина чувствует его шевеление, это 16 – 18 неделя.
Наиболее критический срок наступает через полтора, два месяца после зачатия. В это время у эмбриона закладываются и формируются все органы и системы, и практически любое серьезное отклонение приводит к его гибели.
Почему прекращается развитие беременности
Причин внутриутробной гибели эмбриона может быть много, и они имеют разную этиологию. Даже гинеколог не всегда может точно назвать факторы, которые привели к замершей беременности. В любом случае каждая ситуация детально изучается и делаются выводы для того, чтобы избежать повтора.
Основные причины:
-
Гормональные нарушения. Если у женщины мало вырабатывается гормона прогестерон или много андрогенов, то это плохо сказывается на нормальном течении беременности, что существенно повышает риск гибели плода.
-
Инфекционные заболевания. При вынашивании ребенка важно исключить любые инфекции, так как состояние иммунной системы становится хуже и борьба с патогенными микроорганизмами находится на низком уровне. По этой причине врачи рекомендуют планировать зачатие, то есть предварительно проходить полное исследование организма.
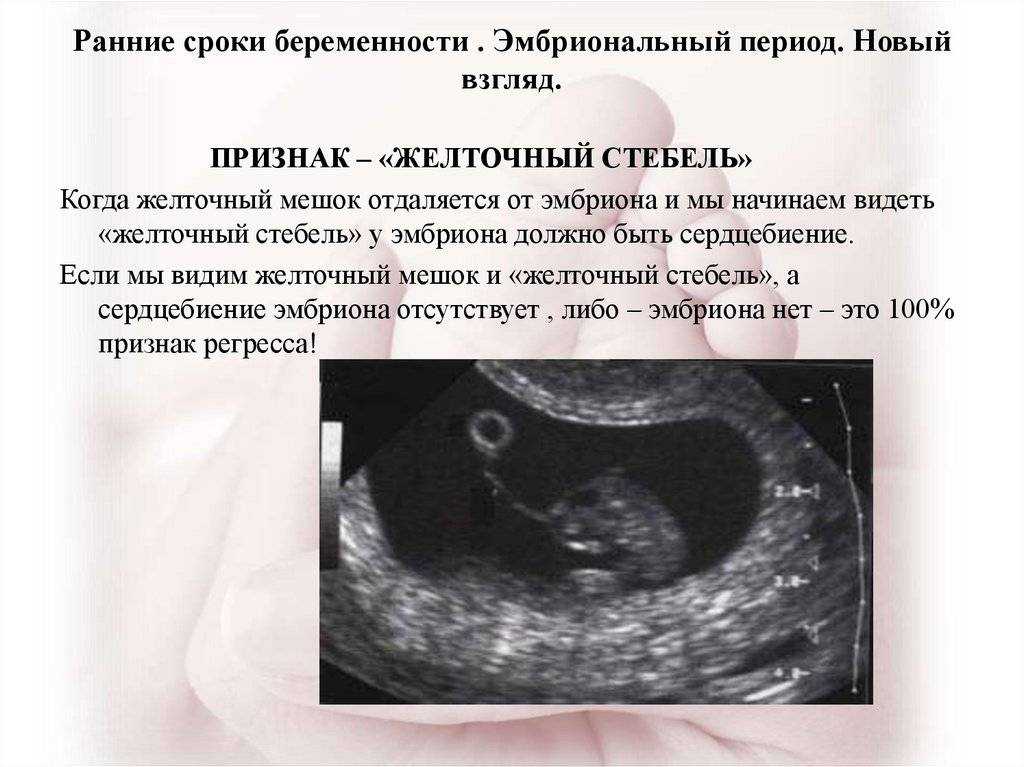 Но даже при нормальных показателях здоровья, любые инфекционные заболевания, в том числе обычная простуда, могут стать фактором развития патологии. Особенно опасны такие болезни как герпес, краснуха, токсоплазмоз, цитомегаловирус.
Но даже при нормальных показателях здоровья, любые инфекционные заболевания, в том числе обычная простуда, могут стать фактором развития патологии. Особенно опасны такие болезни как герпес, краснуха, токсоплазмоз, цитомегаловирус.
-
Генетические патологии. Если у плода есть генетические аномалии, например, лишние хромосомы, то в период закладки органов и систем (примерно восьмая неделя) возникают пороки, несовместимые с жизнью.
-
Патологии органов репродуктивной системы. У женщины могут быть врожденные аномалии: двурогая, однорогая или седловидная матка, удвоение матки и т.д., что нарушает нормальное развитие беременности. При патологическом состоянии эндометрия нарушается питание плода. Также есть приобретенные патологии: внутриматочные спайки, доброкачественные образования, истмико-цервикальная недостаточность и другие нарушения.
-
Тератозооспермия.
 Если сперматозоиды имеют отклонение от нормы (неправильная форма), то зачатие возможно, но это может вызвать аномалии у зародыша.
Если сперматозоиды имеют отклонение от нормы (неправильная форма), то зачатие возможно, но это может вызвать аномалии у зародыша.
-
Образ жизни. Любой врач дает рекомендации женщине о поведении во время вынашивания ребенка, так как это необходимо для нормального развития плода и течения беременности. Если беременная продолжает курить, употреблять алкоголь, находиться в состоянии постоянных стрессов, не соблюдать режим дня (мало спать, не вовремя есть и т.д.), то это значительно повышает риск замирания беременности.
Среди других причин можно назвать наличие в анамнезе выкидышей, абортов, антифосфолипидный синдром, патологии свертываемости крови, резкую смену климата, обострение хронических заболеваний, ожирение или недостаточный вес, прием ряда препаратов без предварительной консультации с врачом.
Диагностика
При наступлении беременности женщина встает на учет к гинекологу и регулярно посещает его для осмотра. Врач спрашивает о самочувствии беременной, прощупывает матку, определяя, как изменился ее размер по сравнению с предыдущим посещением, проводит другие исследования.
Врач спрашивает о самочувствии беременной, прощупывает матку, определяя, как изменился ее размер по сравнению с предыдущим посещением, проводит другие исследования.
Заподозрить неразвивающуюся беременность можно в следующих случаях:
-
Размер матки не соответствует сроку.
-
Матка имеет низкий тонус.
-
Снижена базальная температура (измеряется в прямой кишке).
Если есть подозрение на гибель эмбриона, то гинеколог направляет женщину на УЗИ для более детального анализа ситуации. При проведении ультразвукового исследования можно увидеть признаки замершей беременности: отслойку плаценты (хориона – зародышевой части), отсутствие зародыша в плодном яйце. Также о патологии говорит нечеткое изображение плода, отсутствие биения сердца.
Симптомы и признаки
Независимо от срока беременности, симптоматика будет схожей:
-
Появляются кровянистые выделения из матки.
 Кровотечение может быть как при месячных или просто скудные мазки.
Кровотечение может быть как при месячных или просто скудные мазки.
-
Молочные железы теряют характерные признаки: нет болезненности, набухания.
-
Женщина ощущает боли тянущего характера в нижней части живота.
-
Повышается температура до субфебрильных значений. Беременная жалуется на слабость, озноб, что сигнализирует об интоксикации организма.
-
Если был токсикоз, то его проявления прекращаются.
-
Отсутствует шевеление плода (толчки обычно ощущаются после 16 недели).
В некоторых случаях симптомы слабо выражены и женщина не всегда может заподозрить проблему. Даже тесты не могут показать гибель плода, так как высокий уровень ХГЧ сохраняется еще до двух, трех недель после остановки его развития. В этом случае определить патологию может только гинеколог на очередном приеме.
Нужно отметить, что некоторые признаки не всегда характеризуют гибель плода. Незначительное повышение температуры, слабость являются также следствием какого-либо воспаления в организме, а токсикоз может прекратиться сам по себе в любой момент.
Лечение
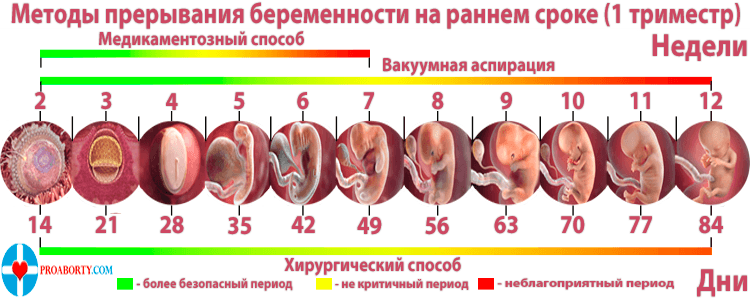
Если плод погиб, то мертвые ткани нужно извлечь из матки. Для этого применяются медикаментозные или хирургические методы. Какую методику выбрать решает врач, исходя из срока беременности, состояния пациентки, данных обследования и других факторов.
Препараты для изгнания патологического содержимого из полости матки применяются реже, чем хирургический способ. Однако лекарственные средства — прекрасная альтернатива в случае, если женщине не рекомендуется наркоз по состоянию здоровья. Медикаментозный аборт можно использовать на сроке до 7 недель.
Хирургическое лечение наиболее надежный метод и всегда дает нужный результат. С помощью инструментов, врач может полностью удалить все мертвые ткани и быстро завершить неразвивающуюся беременность.
При хирургическом вмешательстве применяют несколько методик:
-
Вакуум-аспирация. Содержимое удаляют специальным вакуумным отсосом. Это щадящая операция, которую можно делать на сроке до 12 недель. Плюсы: местная анестезия, не используются расширители.
-
Кюретаж. Выполняется под наркозом, так как процедура травматичная и болезненная. Кюретой выскабливается не только погибший плод, но и верхний слой слизистой оболочки. Операция проводится в стационаре, где женщина остается еще на несколько дней под наблюдением врача.
Кесарево сечение или искусственную стимуляцию родов применяют на более поздних сроках.
В каких случаях чистка обязательна
Самый частый вопрос, которым интересуются женщины с диагнозом замершая беременность – «Обязательно ли делать операцию?». Однозначный ответ дать нельзя, ведь каждый случай индивидуален, но можно дать общее представление по этой теме.
Если беременность перестала развиваться на раннем сроке и стремиться к саморазрешению, то есть появились менструальные выделения, то можно чистку не делать. После завершения кровотечения, нужно пройти ультразвуковое исследование, которое исключит элементы околоплодного яйца и других включений в полости матки.
В случае, когда неразвивающаяся беременность диагностирована, но кровянистых выделений нет, то есть она не разрешается сама по себе, то чистка нужна. На небольших сроках (2 — 7 недель) возможен медикаментозный аборт, однако, по мнению экспертов, лучше сделать вакуум-аспирацию или кюретаж.
Врачи часто сталкиваются с тем, что после приема препаратов патологическое содержимое удаляется не полностью, что приводит к воспалению матки. Чистка потребуется все равно, но травма матки будет сильнее и возможно развитие осложнений. По этой причине, рекомендуется сразу выбирать выскабливание, чтобы потом не прибегать к нему вынуждено и с большими рисками для здоровья.
Кровянистые выделения и боли внизу живота – симптомы, с которыми нужно срочно обращаться к врачу. При нормальном течении беременности их быть не должно. Если вовремя обследоваться, то можно надеяться спасти плод при угрозе замирания. Если эмбрион уже погиб, то нужно быстро избавиться от патологического содержимого, чтобы оно не вызвало воспалительных явлений в матке.
Восстановление после замершей беременности
Независимо от метода лечения, женщине нельзя беременеть минимум полгода, так как организм должен восстановиться. Чтобы снизить вероятность зачатия, врач выписывает пациентке гормональные контрацептивы. Эти препараты также способствуют нормализации гормонального фона, поэтому принимать их нужно не только с целью контрацепции, но и для здоровья.
В это период нужно сбалансировано питаться, гулять на свежем воздухе, принимать витамины, то есть придерживаться здорового образа жизни. Врачи рекомендуют избегать стрессов, а если женщина испытала психологическую травму от произошедшей ситуации, то желательно обратиться за помощью к психологу.
Обследование после лечения
Для выявления причин замершей беременности и исключения рецидивов, женщина должна пройти полное обследование. Это поможет ей подготовиться к следующей беременности и устранить провоцирующие факторы. Если обнаружатся заболевания, то нужно будет пройти соответствующее лечение.
Обследование рекомендуют проходить не только женщине, но и ее супругу. Его можно пройти примерно через месяц после лечения, когда у женщины пройдет менструация.
Какие исследования проводят:
-
УЗИ репродуктивных органов;
-
Анализы крови на гормональный фон, TORCH-инфекции, коагулограмма (свертываемость крови).
-
Спермограмма.
-
Генетическое обследование.
-
Иммунограмма.
Возможны дополнительные исследования и консультации узких специалистов. Если серьезные патологии не выявлены или обнаружены, но устранены, то супруги могут надеяться на успешные роды при наступлении следующей беременности.
Если серьезные патологии не выявлены или обнаружены, но устранены, то супруги могут надеяться на успешные роды при наступлении следующей беременности.
Популярные вопросы
Замершая беременность для многих женщин становится сложным испытанием, поэтому ее часто обсуждают на форумах:
-
Возможны ли ошибки при постановке диагноза по УЗИ? На сроках до 6 недель сложно дать однозначный ответ, так как некоторые показатели не имеют четких критериев. Если есть подозрения, но нет четких признаков, то пациентке назначают повторное УЗИ через неделю, которое исключит ошибки.
-
Что лучше – таблетки или чистка? Изгнание замершего плода медикаментами можно проводить у тех женщин, которые уже рожали. Однако даже в этом случае возможны осложнения. Если содержимое вышло не полностью, то матка воспаляется и сильно травмируется при вынужденной чистке. Некоторые эксперты считают, что лечить замершую беременность можно только хирургическим путем.

-
Через какое время происходит выкидыш? При медикаментозном или самопроизвольном изгнании плодное яйцо отторгается от эндометрия и выходит вместе с выделениями. Это может занять до нескольких дней. Если замерший плод некоторое время находился в матке, то возможно развитие эндометрита. При воспалении эндометрий плохо отторгает плодное яйцо, что может растянуть процесс до нескольких недель. Кроме того, оно может выйти не полностью и в последующем из этих элементов сформируется плацентарный полип, что станет препятствием для последующего зачатия.
Может ли замершая беременность проходить бессимптомно? Первые признаки гибели
эмбриона могут проявиться через две или три недели. До этого времени женщина
может абсолютно ничего не ощущать. Иногда проблема обнаруживается на очередном
приеме у гинеколога, когда он замечает, что размер матки не соответствует
сроку.
Назад к списку статей
Уровни прогестерона в сыворотке выше 20 нг/дл в день переноса эмбрионов связаны с более низкими показателями живорождения и более высокими показателями невынашивания беременности
J Assist Reprod Genet. 2015 сен; 32 (9): 1395–1399.
Опубликовано в Интернете 4 августа 2015 г. doi: 10.1007/s10815-015-0546-7
, , , и
Информация об авторе 6 Фон
Прогестерон (P4 ) необходим для поддержки эндометрия и имплантации эмбриона при нормальном менструальном цикле. В запрограммированных циклах переноса замороженных эмбрионов использование экзогенного P4 необходимо, поскольку эндогенное производство P4 требует функционирующего желтого тела, которого нет в запрограммированных циклах. На сегодняшний день продолжаются споры об идеальных значениях эстрадиола и P4 в сыворотке в циклах переноса замороженных эмбрионов.
Методы
В период с 2010 по 2013 год в одном крупном академическом центре пациенты прошли одиночные циклы переноса замороженных эуплоидных эмбрионов. Были исключены пациентки, использующие донорские ооциты, и пациентки с изменением дозы прогестерона в течение рассматриваемых циклов. Все циклы были запрограммированы, и использовался исключительно внутримышечный Р4. В исследование были включены только пациенты, получавшие одинаковую суточную дозу P4 на протяжении всего цикла ( N = 213 пациентов). Основными исходами были частота продолжающейся беременности/живорождения (OPR/LBR), частота клинической беременности (CPR) и спонтанные аборты/биохимическая беременность. СЛР определяли по наличию мешка на УЗИ в 1 триместре. Количество замерших абортов рассчитывали на одну беременность с плодным мешком. Кривые характеристик оператора приемника (кривые ROC) и критерий хи-квадрат были выполнены для статистического анализа.
Были исключены пациентки, использующие донорские ооциты, и пациентки с изменением дозы прогестерона в течение рассматриваемых циклов. Все циклы были запрограммированы, и использовался исключительно внутримышечный Р4. В исследование были включены только пациенты, получавшие одинаковую суточную дозу P4 на протяжении всего цикла ( N = 213 пациентов). Основными исходами были частота продолжающейся беременности/живорождения (OPR/LBR), частота клинической беременности (CPR) и спонтанные аборты/биохимическая беременность. СЛР определяли по наличию мешка на УЗИ в 1 триместре. Количество замерших абортов рассчитывали на одну беременность с плодным мешком. Кривые характеристик оператора приемника (кривые ROC) и критерий хи-квадрат были выполнены для статистического анализа.
Результаты
Сравнивали две группы на основе уровней P4 на 19-й день (группа A, P4 < 20 нг/мл; группа B, P4 > 20 нг/мл). OPR/LBR были 65 против 49%, группа A против B, p значение = 0,02, RR = 1,33 (1,1–1,7). Частота замершей беременности и биохимические показатели были выше в группе В по сравнению с группой А, 27 против 12%, p = 0,01, RR = 0,45 (0,24–0,86). Когда P4 был разделен на пять групп на основе нанограммов на миллилитр прогестерона на 19-й день (10–15, 15–20, 20–30, 30–40 и >40), наблюдалась тенденция к снижению OPR/LBR (70). , 62, 52, 50 и 33 % соответственно). Также наблюдалось увеличение количества замерших абортов/биохимических показателей (7, 15, 27, 32 и 20 % соответственно). Множественная логистическая регрессия показала увеличение OPR/LBR при учете возраста, уровня ФСГ на 2-й день, веса, количества эмбрионов, подвергнутых биопсии, и количества эуплоидных эмбрионов.
Частота замершей беременности и биохимические показатели были выше в группе В по сравнению с группой А, 27 против 12%, p = 0,01, RR = 0,45 (0,24–0,86). Когда P4 был разделен на пять групп на основе нанограммов на миллилитр прогестерона на 19-й день (10–15, 15–20, 20–30, 30–40 и >40), наблюдалась тенденция к снижению OPR/LBR (70). , 62, 52, 50 и 33 % соответственно). Также наблюдалось увеличение количества замерших абортов/биохимических показателей (7, 15, 27, 32 и 20 % соответственно). Множественная логистическая регрессия показала увеличение OPR/LBR при учете возраста, уровня ФСГ на 2-й день, веса, количества эмбрионов, подвергнутых биопсии, и количества эуплоидных эмбрионов.
Заключение
Уровни P4 >20 нг/мл в день переноса (во время циклов переноса замороженных одиночных эуплоидных эмбрионов) были связаны со снижением OPR/LBR.
Ключевые слова: Лютеиновая поддержка, Экстракорпоральное оплодотворение, Прегестационный скрининг, Прогестерон, Перенос замороженных эмбрионов и циклы переноса замороженных эмбрионов (FET) [1]. В частности, женщины, подвергающиеся циклу замороженного переноса, не могут обеспечить адекватный эндогенный P4 и нуждаются в добавках прогестерона для инициации и поддержания секреторного эндометрия и беременности. Ранее проводились исследования поддержки лютеиновой фазы в замороженных циклах, которые показали, что добавление прогестерона действительно влияет на исход FET [2]. Несколько исследований показали, что лютеиновая поддержка P4 увеличивает частоту живорождения, но существуют смешанные данные о том, снижает ли поддержка P4 частоту выкидышей или биохимическую беременность [3, 4].
В частности, женщины, подвергающиеся циклу замороженного переноса, не могут обеспечить адекватный эндогенный P4 и нуждаются в добавках прогестерона для инициации и поддержания секреторного эндометрия и беременности. Ранее проводились исследования поддержки лютеиновой фазы в замороженных циклах, которые показали, что добавление прогестерона действительно влияет на исход FET [2]. Несколько исследований показали, что лютеиновая поддержка P4 увеличивает частоту живорождения, но существуют смешанные данные о том, снижает ли поддержка P4 частоту выкидышей или биохимическую беременность [3, 4].
Несмотря на эти доказательства роли P4, имеется на удивление мало данных об оптимальных значениях P4 в сыворотке во время лютеиновой фазы и особенно в день переноса эмбрионов в замороженных циклах. После многих лет преобладающего мнения о том, что более высокие значения P4 лучше [5], теперь кажется, что может существовать оптимальное окно для значений P4 во время лютеиновой фазы при ЭКО крупного рогатого скота [10]. Хотя уровни прогестерона в день переноса еще недостаточно изучены у людей, определение времени переноса замороженного эмбриона на основе серийных значений P4, а не только числа дней цикла, приводит к более высокой частоте наступления беременности [11].
Хотя уровни прогестерона в день переноса еще недостаточно изучены у людей, определение времени переноса замороженного эмбриона на основе серийных значений P4, а не только числа дней цикла, приводит к более высокой частоте наступления беременности [11].
Это первое исследование, специально посвященное переносу аутологичных эуплоидных одиночных эмбрионов и связанным с ними уровням P4 во время FET. Цель этого исследования состояла в том, чтобы определить, предсказывает ли уровень P4 в день переноса замороженных эмбрионов клинический исход.
Ретроспективный обзор карт переноса замороженных эмбрионов был проведен в нашем Центре репродуктивной медицины с 2010 по 2013 год. Критериями включения были пациенты, которым была проведена стимуляция яичников и извлечение яйцеклеток с последующей биопсией бластоцистной трофэктодермы (ТЭ) и криоконсервацией всех эмбрионов. Были проанализированы только те FET с переносом одного эмбриона эуплоидного эмбриона. Всем пациентам был предложен преимплантационный генетический скрининг (ПГС). В частности, пациенты старше 40 лет и пациенты с привычным невынашиванием беременности и документально подтвержденными цитогенными аномалиями в продуктах зачатия были проинформированы о преимуществах прегестационного скрининга. Около ~ 50 % пациентов, включенных в это исследование, были пациентками с ЭКО впервые, и ~ 50 % имели неудачное ЭКО в других учреждениях и/или имели рецидивирующее невынашивание беременности. Большинству пациентов в нашем центре и в этом исследовании была проведена стандартная техника осеменения, в отличие от ИКСИ. Критерии исключения включали пациентов, использующих ооциты, полученные от доноров, а также эмбрионы, полученные в результате предыдущих циклов замораживания и оттаивания яйцеклеток. Пациенты также были исключены, если внутримышечная доза P4 была изменена по какой-либо причине во время цикла переноса замороженных эмбрионов. Пациенты, получавшие другие методы поддержки лютеиновой кислоты, кроме внутримышечного инъекционного введения P4, также были исключены из анализа.
В частности, пациенты старше 40 лет и пациенты с привычным невынашиванием беременности и документально подтвержденными цитогенными аномалиями в продуктах зачатия были проинформированы о преимуществах прегестационного скрининга. Около ~ 50 % пациентов, включенных в это исследование, были пациентками с ЭКО впервые, и ~ 50 % имели неудачное ЭКО в других учреждениях и/или имели рецидивирующее невынашивание беременности. Большинству пациентов в нашем центре и в этом исследовании была проведена стандартная техника осеменения, в отличие от ИКСИ. Критерии исключения включали пациентов, использующих ооциты, полученные от доноров, а также эмбрионы, полученные в результате предыдущих циклов замораживания и оттаивания яйцеклеток. Пациенты также были исключены, если внутримышечная доза P4 была изменена по какой-либо причине во время цикла переноса замороженных эмбрионов. Пациенты, получавшие другие методы поддержки лютеиновой кислоты, кроме внутримышечного инъекционного введения P4, также были исключены из анализа. Наконец, две внематочные беременности также были исключены из анализа. Таким образом, всего было включено 213 пациентов.
Наконец, две внематочные беременности также были исключены из анализа. Таким образом, всего было включено 213 пациентов.
Протоколы стимуляции были выбраны на основе характеристик пациенток и исходных лабораторных значений овариального резерва. Максимальный уровень ФСГ на 2-й день составлял 10,3 мМЕ/мл. В большинстве циклов стимуляции яичников использовались гонадотропины/антагонисты ГнРГ, за исключением 11 циклов, которые представляли собой циклы микродоз ацетата лепролида и 11 циклов длинного протокола ацетата лепролида. В циклах гонадотропина/антагониста ГнРГ, когда свинцовый фолликул достигал 13 мм или если уровень эстрадиола >1000 пг/мл, начинали прием антагониста ГнРГ. Когда по крайней мере два свинцовых фолликула достигали ≥17–18 мм, вводили триггер овуляции с использованием 10 000 МЕ ХГЧ или 40 единиц ацетата лейпролида или обоих 40 единиц ацетата лейпролида и 1000 МЕ ХГЧ, в зависимости от уровня эстрогена в момент триггера и количество фолликулов на триггере. Приблизительно через 35 часов ооциты были собраны с помощью трансвагинальной аспирации под ультразвуковым контролем.
Условия инкубатора были установлены на 37 °C, 6 % CO 2 , 5 % O 2 и 89 % N 2 . Ооциты помещали в 25 мкл капель одноступенчатой среды (LifeGlobal), покрытых 1,2 мл минерального масла (LifeGlobal; Онтарио, Канада). Осеменение проводили во второй половине дня после извлечения ооцитов. Если сперма оказалась серьезно повреждена, вместо стандартной инсеминации выполняли ИКСИ. В 1-й день оплодотворение оценивали по визуализации двух ядер. Эмбрионы снова проверяли на прогресс на 3-й день культивирования. Эмбрионы извлекали из культуры ненадолго, на 3-й день, и в прозрачной оболочке делали отверстие с помощью лазера Cronus (Research Instruments; Фалмут, Великобритания) перед возвращением в инкубатор.
Эмбрионы оценивали на 5/6 день в соответствии со стандартными морфологическими критериями, описанными Гарднером и Лейном [12]. Когда эмбрионы достигли стадии расширяющейся бластоцисты, им была проведена ТЕ-биопсия (5, 6 или 7 дни). Сразу после биопсии эмбрионы витрифицируют на криокамерах (Biotech, Inc. ) с использованием растворов для замораживания витрификации для криопектантов эмбрионов (Irvine Scientific, Санта-Ана, Калифорния). Биопсийный материал анализировали с помощью aCGH по нашему стандартному протоколу [13, 14]. Наша культура и протокол замораживания были описаны ранее [15].
) с использованием растворов для замораживания витрификации для криопектантов эмбрионов (Irvine Scientific, Санта-Ана, Калифорния). Биопсийный материал анализировали с помощью aCGH по нашему стандартному протоколу [13, 14]. Наша культура и протокол замораживания были описаны ранее [15].
Перенос одного эмбриона выполнялся в последующих циклах переноса замороженных эмбрионов в соответствии со стандартным протоколом нашего центра. Пациенткам давали пероральный эстрадиол ступенчато до максимальной дозы 6 мг к 14-му дню менструального цикла. На 14-й день были проверены значения эстрадиола и прогестерона, чтобы убедиться в адекватности уровня эстрадиола и убедиться, что у пациентки не было овуляции. Толщину эндометрия также оценивали с помощью трансвагинальной сонографии на 14-й день. Когда толщина эндометрия достигала 7 мм или более и носила трехслойный вид, пациенткам начинали внутримышечное (в/м) введение P4 в течение 6 дней при постоянной дозе 50 или 75 мг в день. P4 давали в качестве добавки, потому что нормальная выработка стероидов яичниками и фолликулярный переход яичников в лютеин подавлялись эстрадиолом. Учитывая отсутствие овуляции, образования желтого тела и продукции эндогенного Р4, введение экзогенного Р4 продолжали до 9 лет.-неделя беременности. Значения P4 проверяли через 2 дня после начала, чтобы обеспечить адекватные уровни. В нашем центре пациентам рекомендуют вводить прогестерон вечером между 6 и 9 часами вечера. и вернуться через два календарных дня между 7 и 9 часами утра, чтобы обеспечить адекватный ответ на значения P4. Перенос эмбрионов произошел на 6-й день внутримышечного введения Р4. На 19-й день проверяли значения эстрадиола и Р4. В частности, кровь брали у каждого пациента примерно от 30 минут до 1 часа до переноса эмбрионов. Важно отметить, что значение P4 еще не было известно до передачи и не влияло на решения о продолжении передачи. Опубликована литература, подтверждающая мнение о том, что устойчивое состояние P4 в тканях эндометрия достигается в течение 24–48 часов, а пиковые значения P4 достигаются через 7,3 часа после введения P4 в виде масляных инъекций. Эти данные об устойчивом состоянии подтверждают мнение о том, что время закачки менее важно, если значения анализируются через > 48 ч после начала P4 в нефти [16].
Учитывая отсутствие овуляции, образования желтого тела и продукции эндогенного Р4, введение экзогенного Р4 продолжали до 9 лет.-неделя беременности. Значения P4 проверяли через 2 дня после начала, чтобы обеспечить адекватные уровни. В нашем центре пациентам рекомендуют вводить прогестерон вечером между 6 и 9 часами вечера. и вернуться через два календарных дня между 7 и 9 часами утра, чтобы обеспечить адекватный ответ на значения P4. Перенос эмбрионов произошел на 6-й день внутримышечного введения Р4. На 19-й день проверяли значения эстрадиола и Р4. В частности, кровь брали у каждого пациента примерно от 30 минут до 1 часа до переноса эмбрионов. Важно отметить, что значение P4 еще не было известно до передачи и не влияло на решения о продолжении передачи. Опубликована литература, подтверждающая мнение о том, что устойчивое состояние P4 в тканях эндометрия достигается в течение 24–48 часов, а пиковые значения P4 достигаются через 7,3 часа после введения P4 в виде масляных инъекций. Эти данные об устойчивом состоянии подтверждают мнение о том, что время закачки менее важно, если значения анализируются через > 48 ч после начала P4 в нефти [16].
Витрифицированные эуплоидные бластоцисты нагревали в день переноса эмбрионов (определяемый как День 19) с использованием среды для оттаивания, уравновешивания и промывки и протокола, приведенного на листке-вкладыше (Irvine Scientific, Санта-Ана, Калифорния). Нагретые бластоцисты содержались в культуральной среде в инкубаторе до момента переноса эмбрионов (между 30 и 300 минутами после нагревания). Отдельные эмбрионы загружали в катетер для переноса (Sureview, Wallace, Smith’s Medical, XXX UK) и переносили в матку пациентки. Во время процедуры переноса размещение катетера в матке было подтверждено ультразвуковым исследованием брюшной полости.
Пациенты были разделены на две группы (группа A, значения P4 на 19-й день <20 нг/дл и группа B, значения P4 на 19-й день ≥20 нг/дл). Двадцать нанограмм на децилитр были выбраны на основании опубликованной литературы и общепринятой практики. Тесты на беременность были завершены на 28-й день менструального цикла. Первое УЗИ обычно проводят на 40-42 день цикла. Если в матке не было видно плодного яйца, биохимическая беременность считалась положительной при тестировании на беременность (уровень ХГЧ > 5,3 мМЕ/мл). При наличии в матке плодного яйца и сердечной деятельности плода беременность считалась клинической. Если в матке был обнаружен гестационный мешок, а сердечная деятельность плода никогда не наблюдалась или не продолжалась после наблюдения, беременность считалась самопроизвольным абортом.
Если в матке не было видно плодного яйца, биохимическая беременность считалась положительной при тестировании на беременность (уровень ХГЧ > 5,3 мМЕ/мл). При наличии в матке плодного яйца и сердечной деятельности плода беременность считалась клинической. Если в матке был обнаружен гестационный мешок, а сердечная деятельность плода никогда не наблюдалась или не продолжалась после наблюдения, беременность считалась самопроизвольным абортом.
Статистический анализ проводили с использованием бесплатного онлайн-эпидемиологического калькулятора (http://www.openepi.com/v37/Menu/OE_Menu.htm). T тесты средств были завершены, если это соответствовало исходным характеристикам пациента. При необходимости также были построены кривые характеристик оператора приемника (ROC). Тесты хи-квадрат использовались для оценки исхода беременности между двумя группами, стратифицированными по их уровням P4. Множественная регрессия использовалась для подтверждения результатов для OPR, LBR и замерших абортов/биохимических беременностей.
Для каждого цикла FET собирали информацию из исходного цикла стимуляции гонадотропином/извлечения яйцеклеток. Все перенесенные эмбрионы были эуплоидными. Характеристики цикла между группой A (P4 < 20 нг/мл) и группой B (P4 ≥ 20 нг/мл) не оказались значимыми для возраста, значений эстрадиола и ФСГ на 2-й день, общего количества использованных гонадотропинов, эстрадиола при триггере, количества извлеченных яйцеклеток, количество оплодотворенных эмбрионов (2PN) и количество эмбрионов, подвергнутых биопсии (см. Таблицу ). Уровни прогестерона значительно различались между двумя группами.
Таблица 1
Характеристики базового цикла
| P4 < 20 нг/мл день 19 | P4 > 20 нг/мл день 19 | p значение | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Возраст | 37 ± 4,2 | 37 ± 4,3 | NS | 9191 дюймы (МЕ)| 3400 ± 1375 | 3571 ± 1497 | НС | 2-й день ФСГ (мМЕ/мл) | 5,99 ± 2,74 | 5,87 ± 2,94 | NS | Эстрадиол 2-й день (пг/мл) | 38,3 ± 14,2 | ±46,134 NS | Эстрадиол на момент запуска (пг/мл) | 2904 ± 1173 | 2656 ± 1131 | NS | # Яйца | 17,3 ± 8,1 | 16,2 909 6009 9009 9009 | Эмбрионы # 2PN | 10,9 ± 5,4 | 10,9 ± 6,7 | NS | # Эмбрионы биопсии | 5,9 ± 4,2 | 5,5 ± 4,6 | NS | P4 на 19-й день (нг/мл) | 9,5 ±95 1 6 | 30,5 ± 11 | <0,001 | |
Открыть в отдельном окне
T тест средств
После переноса размороженных эуплоидных эмбрионов OPR/LBR составили 65 против 49 %, группа A против B, p значение = 0,02, RR = 1,33 (1,1–1,7). Частота самопроизвольных абортов и биохимических показателей была выше в группе B по сравнению с группой A, 27 против 12 %, p = 0,01, RR = 0,45(0,24–0,86). Когда P4 был разделен на группы на основе нанограммов на миллилитр P4 на 19-й день (10–15, 15–20, 20–30, 30–40 и >40), наблюдалась тенденция к снижению OPR/LBR (70, 62, 52, 50 и 33 % соответственно). Также наблюдалось увеличение частоты самопроизвольных абортов/биохимических показателей (7, 15, 27, 32 и 20 % соответственно) (рис. ).
Частота самопроизвольных абортов и биохимических показателей была выше в группе B по сравнению с группой A, 27 против 12 %, p = 0,01, RR = 0,45(0,24–0,86). Когда P4 был разделен на группы на основе нанограммов на миллилитр P4 на 19-й день (10–15, 15–20, 20–30, 30–40 и >40), наблюдалась тенденция к снижению OPR/LBR (70, 62, 52, 50 и 33 % соответственно). Также наблюдалось увеличение частоты самопроизвольных абортов/биохимических показателей (7, 15, 27, 32 и 20 % соответственно) (рис. ).
Открыто в отдельном окне
Частота самопроизвольных абортов/биохимической беременности
Наблюдалось значительное снижение OPR/LBR, когда уровень прогестерона превышал отметку 40 нг/мл на 19-й день цикла(33 % для этих циклов). Наибольшая частота самопроизвольных абортов/биохимической беременности была обнаружена в диапазоне 30–40 нг/мл P4 и составила в среднем 32 % (рис. ). Были построены
ROC-кривые, площадь под кривыми можно увидеть в таблице. Площадь под кривой, оценивающей уровень P4 на 19-й день как предиктор продолжающейся беременности или живорождения, составила 0,60. Соотношение E2/P4 на 19-й день затем оценивали на предмет его способности прогнозировать текущую беременность или живорождение, и было обнаружено, что AUC составляет 0,53. Низкое значение AUC ROC-кривой для отношения E2/P4 на 19-й день.указали, что это соотношение не является хорошим предиктором продолжающейся беременности или живорождения, поэтому мы не проводили дальнейшего анализа этого соотношения.
Соотношение E2/P4 на 19-й день затем оценивали на предмет его способности прогнозировать текущую беременность или живорождение, и было обнаружено, что AUC составляет 0,53. Низкое значение AUC ROC-кривой для отношения E2/P4 на 19-й день.указали, что это соотношение не является хорошим предиктором продолжающейся беременности или живорождения, поэтому мы не проводили дальнейшего анализа этого соотношения.
Таблица 2
Площадь под кривой для 19-го дня прогестерона и соотношения эстрадиол/прогестерон
| OPR/LBR | Клиническая беременность | ||
|---|---|---|---|
| P4 день 19 | AUC 0,60 | ППК 0,56 | ППК 0,60 |
| Отношение E2/P4, день 19 | AUC 0,53 | н/д | н/д |
Открыть в отдельном окне
Также была выполнена множественная логистическая регрессия. При анализе изучали возраст пациентов, ФСГ на 2-й день, вес, количество эмбрионов, подвергнутых биопсии, и количество эуплоидных эмбрионов. OPR/LBR был значительно связан со значением P4 в день перевода и ни с одной из других переменных. Самопроизвольный аборт/биохимическая беременность не были связаны со значением P4 в день перевода, однако были связаны с возрастом.
При анализе изучали возраст пациентов, ФСГ на 2-й день, вес, количество эмбрионов, подвергнутых биопсии, и количество эуплоидных эмбрионов. OPR/LBR был значительно связан со значением P4 в день перевода и ни с одной из других переменных. Самопроизвольный аборт/биохимическая беременность не были связаны со значением P4 в день перевода, однако были связаны с возрастом.
Число женщин, подвергающихся переносу замороженных эмбрионов, увеличилось по многим причинам, в том числе как по выбору, так и по медицинским показаниям для сохранения ооцитов и эмбрионов. В настоящее время существует три различных способа введения экзогенного Р4; вагинально, внутримышечно и перорально [5, 6]. По сравнению с хорионическим гонадотропином человека (ХГЧ) использование лютеиновой поддержки P4 предпочтительнее использования ХГЧ, поскольку он лучше работает в циклах FET [7] и имеет меньшую вероятность синдрома гиперстимуляции яичников [5]. Поэтому важно понимать влияние поддержки P4 и оптимальных значений P4 во время FET.
Это первое исследование, в котором значения P4 на 19-й день во время циклов переноса замороженных эмбрионов связываются с исходами после переноса одиночных размороженных эуплоидных эмбрионов (STEET). Частота ошибок 1,9 % в статусе плоидности эмбрионов установлена и принята в литературе [14]. Таким образом, мы считаем, что эмбрионы, которые мы переносили, действительно были эуплоидными в 98,1 % циклов переноса на основании ранее опубликованной литературы о частоте ошибок с использованием того же метода, который использовался в этом исследовании, сравнительной геномной гибридизации массивов [14]. Наше использование эуплоидных эмбрионов, в свою очередь, позволяет более непосредственно оценить роль уровней P4 при имплантации, не опасаясь, что генетически аномальные эмбрионы исказят общий анализ.
Несколько исследований показали, что значения P4 в узком диапазоне в день триггера ХГЧ коррелируют с более высокими показателями беременности [8, 9]. Во многих исследованиях сообщается, что преждевременное повышение уровня прогестерона неблагоприятно влияет на исход живорождения [17–22] после переноса эмбрионов в свежих циклах ЭКО. Этот феномен (преждевременная лютеинизация) уникален для свежих циклов, когда яичники стимулируются экзогенно введенными гонадотропинами. В нашем исследовании изучаются уровни P4 в циклах, контролируемых экзогенно, но с использованием только эстрогенов и прогестеронов без неконтролируемых реакций яичников, вызванных экзогенными гонадотропинами.
Этот феномен (преждевременная лютеинизация) уникален для свежих циклов, когда яичники стимулируются экзогенно введенными гонадотропинами. В нашем исследовании изучаются уровни P4 в циклах, контролируемых экзогенно, но с использованием только эстрогенов и прогестеронов без неконтролируемых реакций яичников, вызванных экзогенными гонадотропинами.
Недавно было обнаружено, что значения P4 ниже 20 нг/мл в день переноса эмбрионов связаны с более низкими показателями живорождения и клинической беременности в циклах донор-реципиент [23]. Их исследование заметно отличается, потому что эмбрионы не подвергались генетическому скринингу (хотя они были созданы из донорских ооцитов, для которых мы ожидаем высокую частоту эуплоидии), и они не подвергались криоконсервации. Их вывод зависит от предположения, что эмбрионы имели высокую степень эуплоидии. Напротив, наша рукопись обеспечивает исключение смешанных эффектов анеуплоидных эмбрионов, ограничивая используемые эмбрионы известными эуплоидными эмбрионами. Мы считаем, что использование только явно эуплоидных эмбрионов важно для устранения эффектов эмбриона при попытке определить влияние P4 на исходы.
Мы считаем, что использование только явно эуплоидных эмбрионов важно для устранения эффектов эмбриона при попытке определить влияние P4 на исходы.
Весьма вероятно, что повышенные значения P4 на 19-й день указывают на то, что более высокие значения P4 достигаются раньше, а также сохраняются на более высоких уровнях. Это может привести к прямому влиянию на «окно имплантации», сдвинув его на более раннее время. Ускоренное развитие эндометрия может привести к десинхронизации развития матки и эмбриона. Когда матка становится восприимчивой к имплантации раньше, чем эмбрион достигает состояния, пригодного для имплантации, это может привести к снижению имплантации или имплантации «плохого качества». Представленные здесь данные подтверждают это мнение. Основываясь на этом представлении, наши данные показывают, что значения P4 должны поддерживаться в пределах от 10 до 20 нг/мл на 19-й день.. Возможно, нам следует попытаться поддерживать уровни между 10 и 20 нг/мл в течение всего предимплантационного лютеинового периода, по крайней мере, во время циклов переноса замороженных эмбрионов. Мы признаем, что OPR/LBR не претерпел существенных изменений, если P4 находился в пределах от 20 до 30 нг/мл. С другой стороны, значения P4 >30 нг/мл явно ухудшают исход цикла, и их следует избегать. Не было документально подтвержденных значений P4 ниже 10 нг/мл. Наш протокол заключается в увеличении внутримышечного введения P4, если его уровень в сыворотке составляет менее 10 нг/мл через 48 ч после первоначального введения. Поскольку этим пациентам с уровнем прогестерона менее 10 нг/мл требовалось повышение уровня прогестерона, они были исключены из этого анализа, и нам неизвестно о влиянии более низких уровней P4.
Мы признаем, что OPR/LBR не претерпел существенных изменений, если P4 находился в пределах от 20 до 30 нг/мл. С другой стороны, значения P4 >30 нг/мл явно ухудшают исход цикла, и их следует избегать. Не было документально подтвержденных значений P4 ниже 10 нг/мл. Наш протокол заключается в увеличении внутримышечного введения P4, если его уровень в сыворотке составляет менее 10 нг/мл через 48 ч после первоначального введения. Поскольку этим пациентам с уровнем прогестерона менее 10 нг/мл требовалось повышение уровня прогестерона, они были исключены из этого анализа, и нам неизвестно о влиянии более низких уровней P4.
В заключение, в литературе продолжают существовать разногласия относительно оптимальных значений P4, и это, вероятно, связано с различиями в характеристиках пациентов, включая динамику матки, всасывание прогестерона и использование/метаболизм. Мы предлагаем, чтобы поддержание уровней между 10 и 20 нг/мл до имплантации максимально увеличило частоту имплантации и продолжающихся беременностей для FET с использованием одиночных эуплоидных эмбрионов (ESTEET). Однако это небольшое исследование на одном объекте. Потребуются дальнейшие исследования, чтобы изучить универсальность этого предложенного диапазона для оптимизации результатов после эуплоидного полевого транзистора.
Однако это небольшое исследование на одном объекте. Потребуются дальнейшие исследования, чтобы изучить универсальность этого предложенного диапазона для оптимизации результатов после эуплоидного полевого транзистора.
Капсула Наши результаты показывают, что избыток прогестерона во время циклов FET может привести к худшим результатам, предположительно вторичным по отношению к диссинхронному эндометрию и эмбриональной стадии развития.
1. Daya S. Лютеиновая поддержка: прогестагены для предохранения от беременности. Зрелые. 2009; 65 (с1): С29–34. doi: 10.1016/j.maturitas.2009.09.012. [PubMed] [CrossRef] [Google Scholar]
2. Veleva Z, Orava M, Nuojua-Huttunen S, Tapanainen JS, Martikainen H. Факторы, влияющие на результат переноса замороженных-размороженных эмбрионов. Хум Репрод. 2013;28(9): 2425–31. doi: 10.1093/humrep/det251. [PubMed] [CrossRef] [Google Scholar]
3. Bjuresten K, Landgren B, Hovatta O, Stavreus-Evers A. Прогестерон в лютеиновой фазе увеличивает частоту живорождения после переноса замороженных эмбрионов. Фертил Стерил. 2011;95(2):534–537. doi: 10.1016/j.fertnstert.2010.05.019. [PubMed] [CrossRef] [Google Scholar]
Фертил Стерил. 2011;95(2):534–537. doi: 10.1016/j.fertnstert.2010.05.019. [PubMed] [CrossRef] [Google Scholar]
4. Kim C, Lee Y, Lee K, Kwon S, Kim S, Chae H и др. Влияние добавок прогестерона в лютеиновую фазу на естественные циклы переноса замороженных-размороженных эмбрионов. Акушерство Gynecol Sci. 2014;57(4):291–6. doi: 10.5468/ogs.2014.57.4.291. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
5. Пензиас А.С. Поддержка лютеиновой фазы. Фертил Стерил. 2002;77(2):318–23. doi: 10.1016/S0015-0282(01)02961-2. [PubMed] [CrossRef] [Google Scholar]
6. Shapiro DB, Pappadakis JA, Ellsworth NM, Hait HI, Nagy ZP. Замена прогестерона вагинальным гелем по сравнению с внутримышечной инъекцией: цикл и исходы беременности у пациенток с ЭКО, получающих витрифицированные бластоцисты. Хум Репрод. 2014;29(8):1706–11. дои: 10.1093/humrep/deu121. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
7. Ван дер Линден М., Букингем К., Фаркухар С., Кремер Дж. А., Метвалли М. Поддержка лютеиновой фазы для циклов вспомогательной репродукции. Cochrane Datab Syst Rev 2011;(10):CD009154. doi: 10.1002/14651858.CD009154.pub2. [PubMed]
А., Метвалли М. Поддержка лютеиновой фазы для циклов вспомогательной репродукции. Cochrane Datab Syst Rev 2011;(10):CD009154. doi: 10.1002/14651858.CD009154.pub2. [PubMed]
8. Сильверберг К.М., Бернс В.Н., Олив Д.Л., Рил Р.М., Шенкен Р.С. Уровни прогестерона в сыворотке предсказывают успех экстракорпорального оплодотворения/переноса эмбрионов у пациенток, стимулированных ацетатом лейпролида и человеческими менопаузальными гонадотропинами. J Clin Метабол эндокринолов. 1991;73(4):797–803. doi: 10.1210/jcem-73-4-797. [PubMed] [CrossRef] [Google Scholar]
9. Xu B, Li Z, Zhang H, Jin L, Li Y, Ai J, et al. Влияние уровня прогестерона в сыворотке на исход экстракорпорального оплодотворения у пациенток с различной реакцией яичников: анализ более 10 000 циклов. Фертил Стерил. 2012;97(6):1321–7. doi: 10.1016/j.fertnstert.2012.03.014. [PubMed] [CrossRef] [Google Scholar]
10. Niemann H, Sacher B, Elsaesser F. Частота наступления беременности относительно уровня прогестерона в плазме реципиента в день нехирургического переноса замороженных/размороженных эмбрионов крупного рогатого скота. Териогнология. 1985;23(4):631–639. doi: 10.1016/0093-691X(85)-9. [PubMed] [CrossRef] [Google Scholar]
Териогнология. 1985;23(4):631–639. doi: 10.1016/0093-691X(85)-9. [PubMed] [CrossRef] [Google Scholar]
11. Zhe D, Sun L, Zhang H, Chen Z, Jian Y. Время переноса замороженных-оттаивающих эмбрионов определяется уровнем прогестерона в сыворотке: ретроспективное последующее исследование. Eur J Obstet Gynecol Reprod Biol. 2014;181:210–3. doi: 10.1016/j.ejogrb.2014.07.012. [PubMed] [CrossRef] [Google Scholar]
12. Гарднер Д.К., Лейн М. Культура и отбор жизнеспособных бластоцист: возможное предложение для ЭКО человека? Обновление воспроизведения гула. 1997;3:367–82. doi: 10.1093/humupd/3.4.367. [PubMed] [CrossRef] [Google Scholar]
13. Gutierrez-Mateo C, Colls P, Sanchez-Garcia J, Escudero T, Prates R, Ketterson K, et al. Валидация сравнительной геномной гибридизации микрочипов для комплексного хромосомного анализа эмбрионов. Фертил Стерил. 2011;95:953–8. doi: 10.1016/j.fertnstert.2010.09.010. [PubMed] [CrossRef] [Google Scholar]
14. Colls P, Escudero T, Fischer J, Cekleniak NA, Ben-Ozer S, Meyer B, et al. Валидация сравнительной гибридизации генома для диагностики транслокаций в преимплантационных эмбрионах человека. Воспроизведение Биомед онлайн. 2012;24(6):621–9.. doi: 10.1016/j.rbmo.2012.02.006. [PubMed] [CrossRef] [Google Scholar]
Валидация сравнительной гибридизации генома для диагностики транслокаций в преимплантационных эмбрионах человека. Воспроизведение Биомед онлайн. 2012;24(6):621–9.. doi: 10.1016/j.rbmo.2012.02.006. [PubMed] [CrossRef] [Google Scholar]
15. Kramer YG, Kofinas JD, Melzer K, Noyes N, McCaffrey C, Buldo-Licciardi J, et al. Оценка морфокинетических параметров с помощью интервальной микроскопии (TLM) для прогнозирования эуплоидии: универсальны ли модели классификации риска анеуплоидии? J Assist Reprod Genet. 2014;31(9):1231–42. doi: 10.1007/s10815-014-0285-1. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Полсон Р.Дж., Коллинз М.Г., Янков В.И. Фармакокинетика и фармакодинамика прогестерона с 3 дозировками и 2 схемами шипучей микронизированной вагинальной вставки прогестерона. J Clin Endocrinol Metab. 2014;99(11):4241–9. doi: 10.1210/jc.2013-3937. [PubMed] [CrossRef] [Google Scholar]
17. Santos-Ribeiro S, Polyzos NP, Haentjens P, Smitz J, Camus M, Tournaye H, et al. Частота живорождения после ЭКО снижается как при низком, так и при высоком уровне прогестерона в день введения хорионического гонадотропина. Хум Репрод. 2014;29(8):1698–705. doi: 10.1093/humrep/deu151. [PubMed] [CrossRef] [Google Scholar]
Частота живорождения после ЭКО снижается как при низком, так и при высоком уровне прогестерона в день введения хорионического гонадотропина. Хум Репрод. 2014;29(8):1698–705. doi: 10.1093/humrep/deu151. [PubMed] [CrossRef] [Google Scholar]
18. Venetis CA, Kolibianakis EM, Bosdou JK, Tarlatzis BC. Повышение прогестерона и вероятность беременности после ЭКО: систематический обзор и метаанализ более 60 000 циклов. Репрод Биомед Онлайн. 2012;97:1321–7. [PubMed] [Google Scholar]
19. Huang R, Fang C, Xu S, Yi Y, Liang X. Преждевременное повышение уровня прогестерона отрицательно коррелирует с коэффициентом живорождения в циклах ЭКО с агонистом ГнРГ: анализ 2566 циклов. Фертил Стерил. 2012; 98: 644–70. doi: 10.1016/j.fertnstert.2012.05.024. [PubMed] [CrossRef] [Google Scholar]
20. Burns WN, Witz CA, Klein NA, Silverberg KM, Schenken RS. Концентрация прогестерона в сыворотке крови на следующий день после введения хорионического гонадотропина человека и соотношение прогестерон/яйцеклетка предсказывают исход экстракорпорального оплодотворения/переноса эмбриона. J Assist Reprod Genet. 1994;11:17–23. doi: 10.1007/BF02213692. [PubMed] [CrossRef] [Google Scholar]
J Assist Reprod Genet. 1994;11:17–23. doi: 10.1007/BF02213692. [PubMed] [CrossRef] [Google Scholar]
21. Huang CC, Lien YR, Chen HF, Chen MJ, SHieh CJ, et al. Продолжительность преовуляторного повышения прогестерона в сыворотке до введения ХГЧ влияет на исход циклов ЭКО/ИКСИ. Хум Репрод. 2012;27:2036–45. doi: 10.1093/humrep/des141. [PubMed] [CrossRef] [Google Scholar]
22. Проверьте JH, AMui J, Choe JK, Brasile D. Взаимосвязь уровня прогестерона в сыворотке на следующий день после инъекции хорионического гонадотропина человека с исходом после переноса эмбриона при экстракорпоральном оплодотворении. Clin Exp Obstet Gynecol. 2009 г.;36:214–5. [PubMed] [Google Scholar]
23. Brady PC, Kaser DJ, Ginsburg ES, Ashby RK, Missmer SA, Correia KF. Раковский. Концентрация прогестерона в сыворотке в день переноса эмбрионов в циклах донорских ооцитов. J Assist Reprod Genet. 2014;31(5):569–75. doi: 10.1007/s10815-014-0199-y. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
Врачи-ученые получают эмбрион после того, как ткань яичника пациентки с раком молочной железы замораживается, хранится в течение шести лет, а затем реимплантируется под кожу живота
Нью-Йорк, штат Нью-Йорк (3 марта 2004 г. ) — Впервые врачи-ученые из Центра репродуктивной медицины и бесплодия (CRMI) Пресвитерианской больницы Нью-Йорка / Медицинского центра Вейл Корнелл взяли ткань яичника пациентки с раком груди. которую заморозили на шесть лет, повторно имплантировали под кожу живота и получили эмбрион из яиц, собранных из ткани.
) — Впервые врачи-ученые из Центра репродуктивной медицины и бесплодия (CRMI) Пресвитерианской больницы Нью-Йорка / Медицинского центра Вейл Корнелл взяли ткань яичника пациентки с раком груди. которую заморозили на шесть лет, повторно имплантировали под кожу живота и получили эмбрион из яиц, собранных из ткани.
Это уникальное достижение повышает вероятность того, что женщинам или девочкам, которые собираются пройти химиотерапию, облучение или другие методы лечения, повреждающие яичники, можно будет удалить яичники, заморозить их и, возможно, использовать для восстановления фертильности или отмены менопаузы в более поздние сроки. Некоторые методы лечения рака и других заболеваний могут разрушить все шансы на будущую беременность и вызвать преждевременную менопаузу у женщин.
Результаты были ускорены для публикации в журнале The Lancet – они будут опубликованы в Интернете 9 марта, а в печати – 13 марта. Исследование проводилось под руководством доктора Кутлука Октая из NewYork-Presbyterian/Weill Cornell’s Center for Reproductive Medicine and Бесплодие (КРМИ).
«Это первый случай в истории медицины, когда эмбрион был получен из замороженной ткани яичника после трансплантации яичника», — сказал доктор Кутлук Х. Октай, доцент кафедры акушерства и гинекологии Медицинского колледжа Вейл Корнелл и специалист в области Репродуктивная эндокринология и бесплодие в NewYork-Presbyterian/Weill Cornell’s CRMI.
«Это исследование представляет собой потенциально значительный прогресс в репродуктивной сфере в двух отношениях: во-первых, женщины могут сохранить свою фертильность, заморозив ткань яичника, а во-вторых, беременность может быть возможной даже после того, как ткань остается замороженной в течение длительного времени», — сказал доктор. Зев Розенвакс, соавтор исследования Lancet и директор CRMI.
У пациентки был диагностирован рак молочной железы в возрасте 30 лет, ей удалили и заморозили яичник. Пять лет спустя, после химиотерапии, которая излечила ее от рака, она связалась с доктором Октаем. После подробного консультирования 15 кусочков ткани яичника были разморожены и трансплантированы под кожу живота. Через три месяца ткань начала вырабатывать гормоны и яйцеклетки, и каждый месяц яйцеклетки собирали для экстракорпорального оплодотворения.
Через три месяца ткань начала вырабатывать гормоны и яйцеклетки, и каждый месяц яйцеклетки собирали для экстракорпорального оплодотворения.
«За восемь месяцев мы собрали около 20 яйцеклеток, и восемь из них были достаточно хороши для оплодотворения. Наконец-то мы получили эмбрион, который достиг здоровой на вид четырехклеточной стадии», — сказал доктор Октай. «Эмбрион был перенесен в матку пациентки, хотя она не забеременела. Шансы на беременность с одним эмбрионом ограничены, вероятно, менее 10%, поэтому мы собираемся продолжать попытки».
Доктор Октай сказал, что процедура может быть интересна многим типам пациентов, как детям, так и взрослым.
«В этой стране потенциально есть несколько сотен тысяч женщин и детей, которые могли бы получать от этого выгоду ежегодно», — сказал он. «У нас есть пациенты в возрасте от 6-7 лет и старше», — сказал доктор Октай.
«Вы можете сделать это для детей, больных раком, взрослых и женщин, перенесших операцию по поводу доброкачественных состояний, при которых вы теряете яичники», — добавил доктор Октай. «Есть гематологические заболевания, при которых вы даете пациентам лекарства с такими побочными эффектами; это касается не только рака».
«Есть гематологические заболевания, при которых вы даете пациентам лекарства с такими побочными эффектами; это касается не только рака».
При некоторых заболеваниях костей требуется лучевая терапия таза, которая также снижает фертильность.
Также существует вероятность того, что процедура может быть выполнена выборочно. «Может ли женщина сохранить часть яичника для будущего использования против старения? Это всегда обсуждается», — сказал доктор Октай. «На самом деле вы можете сохранить ткань яичников — потенциально столько, сколько захотите — и, возможно, сохранить фертильность. Но это требует дальнейшего изучения».
Процедура относительно неинвазивная, сказал доктор Октай. «Введение под кожу выполняется под местной анестезией, как и сбор яйцеклетки», — сказал он. «Вы можете продолжать разговор с пациентом, пока это происходит».
По словам доктора Октай, на данный момент менее дюжины женщин во всем мире пересадили ткань яичника в свое тело после лечения, нарушающего фертильность.

