Содержание
УЗИ плода, профилактика и диагностика
От того как расположен плод в утробе матери, зависит то, как будет протекать родовая деятельность. На протяжении всего срока беременности ребенок не только активно растет, но и часто меняет положение своего тела. Особенно подвижен малыш бывает в первых двух триместрах беременности, потом же ему остается все меньше места в матке матери и смена позы становится для него проблематичной. Предлежание плода — крайне важный фактор, от которого будет зависеть то, каким образом будет рожать женщина – естественным путем или при помощи кесарева сечения.
Достоверной можно считать информацию, полученную не ранее 32 недели, до этого времени ситуация может поменяться и не один раз. Для того, чтобы узнать в каком месте находится головка малыша, врач-гинеколог при каждом плановом посещении проводит осмотр и методом пальпации определяет положение плода. Для более точных результатов проводится УЗИ плода.
Виды предлежания плода
Существуют следующие виды предлежания плода.
- Затылком вперед. В этом случае, первой на свет появляется эта часть головы – этот вариант считается самым удачным, как для матери, так и для малыша.
- Лобное – ребенок будет рождаться лбом вперед.
- Лицевое – этот вариант предполагает появление ребенка затылком назад.
Тазовое положение – у входа в малый таз находится нижняя часть тела малыша:
- Ягодицами вперед. Ребенок располагается в матке таким образом, что его ножки находятся, примерно на одном уровне с головой, они вытянуты вдоль тела, а к основанию матки направлены ягодицы.
- Ножное предлежание представляет собой вариант, при котором одна или две ноги ребенка направлены к входу в малый таз.
- Смешанное положение – это тот случай, когда и ножки и ягодицы плода находятся у основания матки.

Головное предлежание считается лучшим вариантом, как для матери, так и для плода. В этом положении ребенку будет проще проходить по родовым путям, а женщине легче родить. К тому же, это самый безопасный вариант для естественных родов.
Тазовое положение плода: возможные причины и признаки
Такое предлежание плода не считается патологией, но оно является крайне нежелательным. Существует ряд факторов, которые могут спровоцировать это явление, главными из которых является снижение тонуса матки или ее крайней возбудимости.
Помимо этого, причинами такого положения малыша в утробе матери может стать количество околоплодных вод (многоводье или маловодье). Аномальные изменения матки, предлежание плаценты и некоторые пороки развития плода могут спровоцировать то, что малыш примет неправильное положение. Сама женщина, практически не ощущает то, что ребенок принял тазовое предлежание – это не вызывает дискомфорта или болевых ощущений.
Этот факт может выявить только специалист, на основании проведения обследований, самым точным из которых является УЗИ.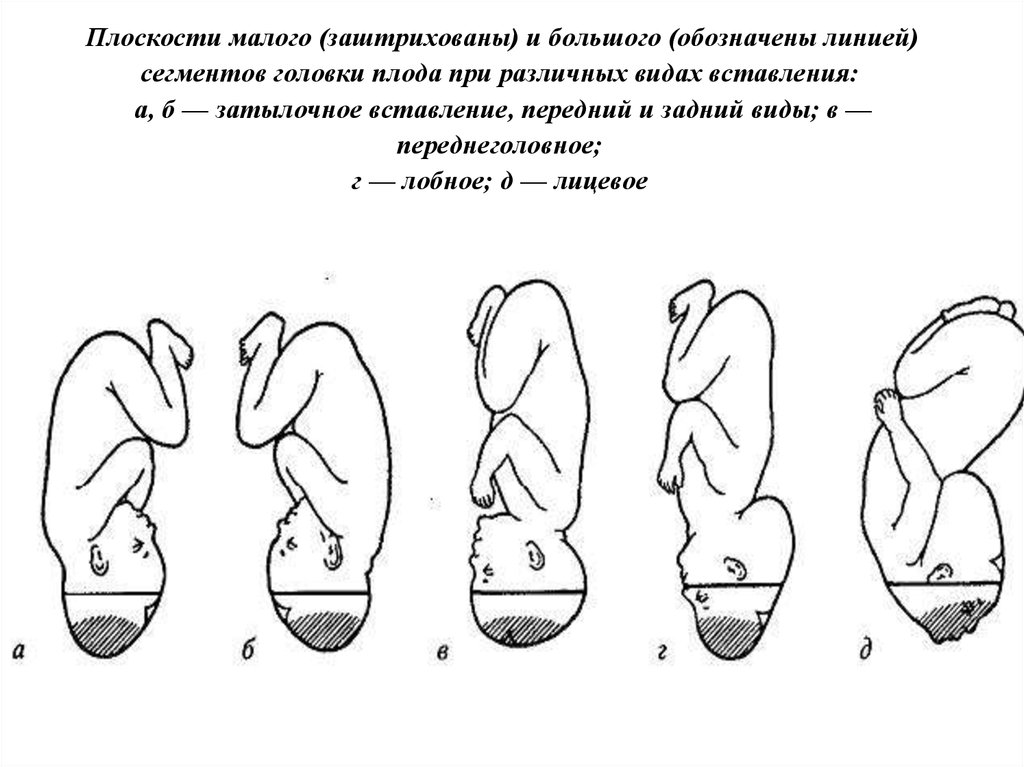 Считается, что малыш не меняет положения, начиная с 22 недели, но это не является непреложной истиной – наиболее точные данные можно получить только после 32 недели.
Считается, что малыш не меняет положения, начиная с 22 недели, но это не является непреложной истиной – наиболее точные данные можно получить только после 32 недели.
Роды при тазовом предлежание плода
Если женщина имеет противопоказания к проведению процедуры кесарева сечения, то ей разрешают родить самостоятельно. Такой вариант возможен и в том случае, когда роженица настаивает на том, чтобы малыш появился на свет естественным путем.
Есть ряд ограничений, при которых кесарево сечение не подлежит обсуждению: крупный плод, наличие рубцов на матке роженицы, узкий таз беременной, предлежание плаценты.
Генетика — виды генетических исследований
О направлении
Репродуктология тесно связана с медицинской генетикой. Изучение генов человека позволяет врачам выявить причины бесплодия, в том числе неясной этиологии, оценить вероятность наступления беременности, а также получить прогноз развития, как эмбриона, так и ребенка после рождения.
Причин проявления у будущего ребенка генетических патологий немало: это и наследственность, и перенесенные матерью эндокринные заболевания и инфекции, и мутации, возникшие в половых клетках родителей с возрастом, и негативное влияние окружающей среды.
В случае если вы не уверены в необходимости проведения генетических исследований, специалисты клиники «Сканферт» готовы проконсультировать вас.
Врач оценит риски возникновения генной или хромосомной патологии у будущего ребенка, изучит анамнез и информацию о вашем партнере и ваших родственниках и определит целесообразность назначения генетической диагностики.
Виды генетических исследований
В клинике «Сканферт» у вас есть возможность, при наличии показаний, пройти такие исследования как молекулярно-генетические анализы, преимплантационная диагностика, кариотипирование, пренатальная диагностика. Эти процедуры не входят в стоимость программы ЭКО и оплачиваются дополнительно.
Преимплантационное генетическое тестирование (ПГТ)
Морфологическая оценка эмбрионов не позволяет оценить их генетический статус. Иными словами, внешний вид эмбриона не строго коррелирует с его генетическим материалом. Свыше 50% морфологически хороших эмбрионов имеет отклонения наследственного материала. Это может объяснить некоторые неудачи имплантации при переносе морфологически хороших эмбрионов.
Это может объяснить некоторые неудачи имплантации при переносе морфологически хороших эмбрионов.
Например, 90% анеуплоидных эмбрионов (с аномальным количеством хромосом) прекращают развиваться на ранней стадии и неспособны имплантироваться. В оставшихся 10% случаев возникает биохимическая беременность или выкидыш. Очень редко результатом является рождение ребенка с синдромом Дауна.
С целью исключения генетических аномалий у эмбрионов до момента их имплантации проводится ПГТ. Такое исследование позволяет отобрать эмбрионы с нормальным числом хромосом. ПГТ значительно повышает шансы успешного результата ЭКО.
Показания для ПГТ
Абсолютными показаниями является наличие наследственных заболеваний, сцепленных с полом, а также хромосомной аномалии у одного из супругов или у родственников. Кроме того, среди показаний:
-
неоднократные попытки ЭКО, закончившиеся неудачей;
-
возраст женщины от 35 лет;
-
частые контакты женщины с токсичными веществами, перенесенная лучевая нагрузка или лечение препаратами, способными вызвать мутации;
-
возраст мужчины больше 49 лет;
- неоднократное самопроизвольное прерывание беременности, замершая беременность в анамнезе
-
мужское бесплодие, обусловленное проблемами сперматогенеза.
Методы ПГТ
Генетический анализ может выполняться разными методами. На сегодняшний день методы aCGH и NGS обеспечивают самые надежные и информативные результаты.
В клинике Сканферт применяется наиболее прогрессивный. информативный и безопасный метод преимплантационного исследования на сегодняшний день — NGS (секвенирование нового поколения).
В результате врачи-генетики получают описание структуры нуклеотидов в молекулах РНК и ДНК, которое сравнивается с нормативными данными для выявления отклонений. Данная процедура отличается высокой информативностью и точностью (99,99%).
Для исследования осуществляется биопсия (забор генетического материала) эмбриона на пятые или шестые сутки. При этом используется несколько клеток трофэктодермы, из которых впоследствии формируются внезародышевые ткани — плацента, так что манипуляция совершенно безопасна: вероятность негативных последствий – менее 1%.
Такое исследование позволяет отобрать на перенос эмбрионы с нормальным числом хромосом.
Кариотипирование
Одним из способов выяснить причины бесплодия пары и риск проявления у ребенка хромосомных заболеваний – кариотипирование. Данный вид исследования включает в себя анализ набора хромосом для выявления их аномалий.
В геноме человека 46 хромосом (или 23 пары хромосом): 22 пары аутосомных и одна пара половых (две X-хромосомы у женщин, X- и Y-хромосомы у мужчин). Каждая из двух хромосом в паре получена от яйцеклетки и от сперматозоида соответственно. Нормальный кариотип обозначают как 46XX (для женщин) и 46XY (для мужчин).
Показания для определения кариотипа:
- Наличие каких-либо пороков развития у одного из партнеров;
- Хромосомные заболевания у родственников;
- Самопроизвольные аборты, замершая беременность или мертворождение;
- Наличие у ранее родившихся детей пороков развития, в том числе умственного, и хромосомных заболеваний;
- Диагностированное бесплодие в браке;
- Аномалии полового развития;
- Длительный контакт с токсичными веществами или радиацией;
- Возраст хотя бы одного из партнеров больше 40 лет;
- Преждевременная менопауза;
- Отставание в половом развитии.
Что показывает генетическое тестирование
Кариотипирование помогает выявить изменение количества отдельных соматических хромосом (моносомия, трисомия и полисомии), например, болезни Дауна, Патау и Эдвардса, а также изменение количества половых хромосом, которые приводят к заметным отклонениям в психике и умственном развитии (синдром Клайнфельтера, болезнь Шерешевского-Тернера).
Кроме того, данный вид диагностики показывает структурные изменения хромосом или хромосомные перестройки (дупликации, транслокации, делеции, инверсии, образование кольцевых структур).
Особенности процедуры
Для проведения кариотипирования достаточно сдать кровь из вены. Во время анализа исследуются ядра лейкоцитов. Если обследуются оба родителя, забор крови производится у каждого из них. Кроме того, в медицинской генетике применяется кариотипирование тканей плода. Это может быть осуществлено в рамках инвазивной пренатальной диагностики или в случае замершей беременности или выкидыша – для того, чтобы в дальнейшем выбрать оптимальный вариант пути к материнству.
Молекулярно-генетические анализы
Чтобы оценить риск проявления у будущего ребенка таких патологий, как муковисцидоз, миодистрофия Дюшенна или гемофилия, требуется молекулярно-генетический анализ – он позволяет выявить соответствующие мутации отдельных генов. Для проведения анализа используется венозная кровь пациента.
Пренатальная диагностика
Развитие плода может происходить с аномалиями – как правило, причиной этого являются хромосомные отклонения. Результатом может быть не только замершая беременность, но и мертворождение или летальный исход в первый год жизни ребенка. Выявить подобные патологии возможно во время беременности, как неинвазивным, так и инвазивным методом.
Показаниями для пренатальной диагностики являются:
- возраст женщины старше 35 лет;
- диагностированные у ранее родившихся детей хромосомных аномалий и врожденных отклонений в развитии;
- выявленные при УЗИ признаки хромосомных аномалий;
- сбалансированная хромосомная перестройка у одного из родителей;
- значительный риск проявления патологии, выявленный при анализе крови.

Неинвазивное пренатальное тестирование (НИПТ)
Это исследование проводится после наступления беременности, на сроке от 10 недель. Для анализа генома плода не нужно никаких затрагивающих его манипуляций: достаточно сдать кровь из вены. Специалисты определяют наличие аномалий, изучая фрагменты ДНК будущего ребенка, которые находятся в крови матери. При этом можно выявить различные хромосомные аномалии, включая синдром Дауна. Кроме того, по медицинским показаниям производится определение пола плода.
Инвазивная пренатальная диагностика (ИПД)
При этом виде исследования проводят биопсию оболочек плода для дальнейшего кариотипирования клеток. Необходимость хирургического вмешательства является недостатком метода, однако шансы выкидыша по причине ИПД невелики: всего 0,5%, при этом в обычных условиях этот показатель составляет от 15 до 25%. При биопсии тело плода не подвергается какому-либо воздействию – исследуется только образец пуповинной крови или ворсины хориона.
ИПД проводят в стационаре под контролем ультразвукового аппарата, без применения наркоза.
Противопоказанием для ИПД является наличие ВИЧ-инфекции у матери. При резус-конфликте данный вид исследования применяют с особой осторожностью.
Виды ИПД
Хорионбиопсия. Осуществляется в первом триместре. Позволяет выяснить наличие тяжелых патологий плода на раннем сроке, в результате прерывание беременности будет наименее опасно для пациентки. Среди минусов хорионбиопсии – возможность ложноположительного результата.
Плацентобиопсия. Проводится при сроке в 14-20 недель. В данном случае исследуют клеточный материал плаценты.
Кордоцентез. Проводится при сроке от 19-20 недель, материалом является пуповинная кровь. Кроме генетических исследований, ее можно подвергнуть всем возможным видам анализов (на гормоны, инфекции и так далее). Этот метод ИПД является наиболее информативным, но, к сожалению, может быть применен только на более поздних сроках.
Гемолитическая болезнь новорожденных – Группы крови и антигены эритроцитов
Гемолитическая болезнь новорожденных (ГБН) раньше была основной причиной потери плода и смертность среди новорожденных. Считается, что первое описание HDN датируется 1609 годом. французская акушерка, которая родила близнецов — один ребенок распух и вскоре умер после рождения у другого ребенка развилась желтуха, и через несколько дней он умер. Для последующие 300 лет было описано множество подобных случаев, когда новорожденные не выживать.
Только в 1950-х годах была выяснена основная причина ГБН; а именно, красные кровяные тельца (эритроциты) новорожденного подвергаются атаке антител из мать. Приступ начинается, когда ребенок еще находится в утробе матери, и вызван несовместимость крови матери и ребенка.
К 1960-м годам испытания в США и Великобритании проверили использование
терапевтические антитела, которые могли бы удалить антитела, вызывающие ГБН, из
кровообращение матери. Испытания показали, что введение терапевтических антител женщинам
во время их беременности в значительной степени предотвратили развитие ГБН (1). К 1970-е годы, рутинная дородовая помощь включена
скрининг всех будущих матерей для выявления тех, чья беременность может быть под угрозой
ГБН и соответствующее профилактическое лечение. Это привело к драматическому
снижение частоты ГБН, особенно тяжелых случаев, которые были причиной
для мертворождения и неонатальной смерти.
К 1970-е годы, рутинная дородовая помощь включена
скрининг всех будущих матерей для выявления тех, чья беременность может быть под угрозой
ГБН и соответствующее профилактическое лечение. Это привело к драматическому
снижение частоты ГБН, особенно тяжелых случаев, которые были причиной
для мертворождения и неонатальной смерти.
В этой главе обсуждаются причины ГБН и методы лечения или свести к минимуму, если не предотвратить полностью.
Материнские антитела проникают через плаценту и атакуют эритроциты плода
Во время беременности некоторые антитела матери переносятся через плаценту и попадают в кровоток плода. Это необходимо, потому что к моменту рождения новорожденные имеют только примитивную иммунную систему, и постоянное присутствие материнские антитела помогают им выжить, пока их иммунная система созревает. Недостатком этой защиты является то, что, воздействуя на фетальные эритроциты, материнские антитела также могут вызывать ГБН.
Основной причиной ГБН является несовместимость резус-группы крови матери
и плод. Чаще всего гемолитическая болезнь вызывается антигеном D, хотя
другие антигены Rh, такие как c, C, E и e, также могут вызывать проблемы.
Чаще всего гемолитическая болезнь вызывается антигеном D, хотя
другие антигены Rh, такие как c, C, E и e, также могут вызывать проблемы.
Беременность с риском HND – это беременность, при которой резус-отрицательная мать становится беременных резус-положительным ребенком (ребенок, унаследовавший антиген D от отец). Иммунный ответ матери на антиген D плода должен сформироваться антитела к нему (анти-D). Эти антитела обычно относятся к типу IgG. тип, который транспортируется через плаценту и, следовательно, доставляется к плоду обращение.
ГБН также может быть вызвана несовместимостью группы крови ABO. Оно возникает, когда мать с группой крови 0 беременеет плодом с другой группой крови (тип А, В или АВ). Сыворотка матери содержит встречающиеся в природе анти-А и анти-В, которые, как правило, относятся к классу IgG и поэтому могут проникать через плаценту и гемолиз фетальных эритроцитов.
ГБН из-за несовместимости по системе ABO обычно менее тяжелая, чем резус-несовместимость. Один
Причина в том, что эритроциты плода экспрессируют меньше антигенов групп крови системы АВО по сравнению с
взрослые уровни. Кроме того, в отличие от резус-антигенов группа крови АВО
антигены экспрессируются различными тканями плода (и взрослого человека), уменьшая
вероятность связывания анти-А и анти-В антигенов-мишеней на эритроцитах плода.
Один
Причина в том, что эритроциты плода экспрессируют меньше антигенов групп крови системы АВО по сравнению с
взрослые уровни. Кроме того, в отличие от резус-антигенов группа крови АВО
антигены экспрессируются различными тканями плода (и взрослого человека), уменьшая
вероятность связывания анти-А и анти-В антигенов-мишеней на эритроцитах плода.
Менее распространенные причины ГБН включают антитела, направленные против антигенов Келл группа крови (например, анти-K и анти-k), группа крови по Кидду (например, анти-Jka и анти-K анти-Jkb), группу крови Даффи (например, анти-Fya) и антитела MNS и s группы крови. На сегодняшний день антитела, направленные против групп крови Р и Льюис, не обнаружены. связанные с ГБН.
Сенсибилизация происходит во время первой беременности
Сенсибилизация к антигену возникает, когда иммунная система сталкивается с антигеном для
первый раз и вызывает иммунный ответ. В случае ГБН, вызванной Rh
несовместимости, резус-D-отрицательная мать может сначала столкнуться с D-антигеном, в то время как
при беременности резус-положительным ребенком или при переливании крови
Резус-положительная кровь. После сенсибилизации матери к D-антигену ее сыворотка
будет содержать анти-D. Прямой тест Кумбса (см. ниже) подтверждает наличие
анти-D и, следовательно, мать была сенсибилизирована.
После сенсибилизации матери к D-антигену ее сыворотка
будет содержать анти-D. Прямой тест Кумбса (см. ниже) подтверждает наличие
анти-D и, следовательно, мать была сенсибилизирована.
Лишь небольшое количество крови плода должно попасть в кровоток матери для иметь место сенсибилизация. Как правило, это происходит во время родов первенца. Rh D-положительный ребенок. Кровотечение у плода и матери часто встречается во время родов и увеличивается во время затяжных или осложненных родов, что, в свою очередь, увеличивает риск сенсибилизации. Сенсибилизация может произойти и на ранних сроках беременности, например во время внутриутробного кровотечения или выкидыша. Это также может произойти во время медицинских процедуры, такие как прерывание беременности или взятие проб ворсин хориона.
Риск сенсибилизации к антигену Rh D снижается, если плод относится к группе ABO
несовместимый. Это связано с тем, что любые эмбриональные клетки, попадающие в материнскую
быстро разрушаются мощными материнскими анти-А и/или анти-В, уменьшая
вероятность контакта матери с антигеном D.
ГБН возникает при последующих беременностях
Первоначально материнские анти-D, которые образуются во время сенсибилизации IgM типа, которые не могут проникать через плаценту. При последующих беременностях повтор встреча с антигеном Rh D стимулирует быструю выработку анти-D типа IgG, которые могут транспортироваться через плаценту и попадать в кровоток плода. Один раз в кровотоке плода анти-D прикрепляются к антигенам RhD, обнаруженным на плодах. эритроцитов, помечая их как подлежащие уничтожению.
Скорость гемолиза определяет, является ли характер ГБН легкой, умеренной или тяжелый. В легких случаях небольшое увеличение скорости гемолиза переносится больными. плод. При рождении и в период новорожденности симптомы включают легкую анемию. и желтуха, которые могут пройти без лечения.
В случаях, когда имеется большее увеличение скорости гемолиза, уровень
билирубин может оставаться низким во время беременности из-за способности
плаценты для выведения билирубина из кровотока плода. Однако после рождения
незрелая печень новорожденного не способна метаболизировать повышенное количество билирубина
который вместо этого накапливается в его или ее крови. В течение 24 часов после рождения уровень
билирубин может резко возрасти. Если уровень продолжает повышаться, билирубин может попасть в
головного мозга, чтобы вызвать ядерную желтуху, потенциально смертельное состояние, которое оставляет навсегда
неврологические нарушения у выживших детей.
Однако после рождения
незрелая печень новорожденного не способна метаболизировать повышенное количество билирубина
который вместо этого накапливается в его или ее крови. В течение 24 часов после рождения уровень
билирубин может резко возрасти. Если уровень продолжает повышаться, билирубин может попасть в
головного мозга, чтобы вызвать ядерную желтуху, потенциально смертельное состояние, которое оставляет навсегда
неврологические нарушения у выживших детей.
Еще более быстрое и продолжительное разрушение эритроцитов приводит к тяжелой анемии в
плод. Печень, селезенка и другие органы увеличивают выработку эритроцитов до
компенсировать их потерю. Стремление производить эритроциты заставляет печень и селезенку
увеличение размеров (гепатоспленомегалия) и нарушение функции печени. Незрелый
Эритроциты (эритробласты) попадают в кровоток, отсюда и альтернативное название
этого заболевания, эритробластоз плода. Осложнением тяжелой ГБН является водянка.
fetalis, при котором ткани плода становятся отечными (отечными). Это условие
обычно фатально, либо внутриутробно или вскоре после рождения.
Это условие
обычно фатально, либо внутриутробно или вскоре после рождения.
Реакция Кумбса для выявления резус-несовместимости между матерью и плодом
Для выявления ГБН необходимо определить наличие у матери анти-Rh IgG. В vivo эти антитела разрушают Rh D-положительные эритроциты плода, но в vitro , они не лизируют клетки и даже не вызывают агглютинацию, делая их трудно определить. Поэтому используется тест Кумбса. В этом тесте используются антитела которые связываются с анти-D-антителами. Тест назван в честь Робина Кумбса, который первым разработали методику использования антител, направленных против других антитела.
Прямой тест Кумбса: диагностика ГБН
Прямой тест Кумбса выявляет материнские анти-D-антитела, которые уже связались к эритроцитам плода.
Сначала образец фетальных эритроцитов промывают для удаления любых несвязанных антител (Ig). Когда
добавляют тестовые антитела (анти-Ig), они агглютинируют любые эритроциты плода до
какие материнские антитела уже связаны.
Этот тест называется прямым тестом Кумбса, поскольку анти-Ig связывается «напрямую» с материнские анти-D Ig, покрывающие эритроциты плода при ГБН.
Непрямой тест Кумбса: используется для профилактики ГБН
Непрямой тест Кумбса обнаруживает анти-D-антитела в сыворотке крови матери. Если эти должны были вступить в контакт с эритроцитами плода, они вызывали их гемолиз и, следовательно, вызвать ГБН. Обнаружив материнский анти-D до того, как эритроциты плода подверглись атаке, Лечение может быть назначено для предотвращения или ограничения тяжести ГБН.
Для этого теста сыворотку матери инкубируют с Rh D-положительными эритроцитами. Если есть анти-D присутствуют в сыворотке матери, они будут связываться с клетками. Клетки затем промывают для удаления всех свободных антител. Когда анти-Ig антитела Кроме того, они будут агглютинировать любые эритроциты, с которыми связаны материнские антитела.
Это называется непрямым тестом Кумбса, потому что анти-Ig находит «непрямой»
наличие вредных материнских антител, требующих добавления фетальных эритроцитов к
показывают способность материнского анти-D связываться с эритроцитами плода.
См. схему прямого и непрямого тестов Кумбса в Janeway & Траверс Иммунобиология
Профилактика ГБН
Определение резус-статуса матери
В рамках плановой дородовой или дородовой помощи определяется группа крови матери (система ABO и Rh) определяется по анализу крови. Тест на наличие атипичных антител в сыворотке крови матери. В настоящее время RhD несовместимость является единственной причиной ГБН, для которой скрининг является рутинным.
В США частота Rh D-отрицательного статуса колеблется примерно от 17% у европеоидов примерно до 7% у латиноамериканцев и чернокожих. Частота намного ниже у лиц азиатского происхождения (включая выходцев из Китая, Индии и Японии), в среднем около 2% (2).
Если мать не сенсибилизирована, снизить риск сенсибилизации в будущем D проводится непрямой тест Кумбса (см. выше). Если анти-D не обнаружен в сыворотке матери вполне вероятно, что она не была сенсибилизирована к резус-фактору D. антиген.
Риск будущей сенсибилизации может быть значительно снижен, если
несенсибилизированные матери анти-D Ig, которые «вытирают» любые фетальные эритроциты, которые могут иметь
просачивается в материнский кровоток, снижая риск первого контакта
к антигену D.
Обычно резус-отрицательные матери получают инъекцию анти-D Ig примерно в 28 лет. недель беременности, то есть примерно в то время, когда эритроциты плода начинают экспрессировать D антиген, и матери получают еще одну дозу примерно в 34 недели, за несколько недель до начинаются роды, во время которых высок риск фетоматеринского кровотечения. Финал доза анти-D Ig вводится после родов. Кроме того, анти-D Ig назначают для покрытия других событий во время беременности, которые могут привести к сенсибилизация, например, дородовые кровотечения и преэклампсия.
Этот профилактический режим против резус-сенсибилизации эффективен. Однако, в настоящее время не существует рутинной профилактики ГБН, вызванной несовместимостью антигены других групп крови.
Если мать сенсибилизирована, определите, находится ли плод в группе риска, и контролировать соответственно
Как только наличие материнского анти-D было подтверждено, следующим шагом будет
определить, являются ли эритроциты плода мишенью, т. е. подтвердить резус-статус
плод. Если отец гомозиготен по аллелю D (D/D), плод будет
Д положительный. Однако, если отец гетерозиготен (D/d), вероятность 50:50
что плод D-положительный, и единственный способ точно узнать группу крови
заключается в тестировании образца клеток плода, взятого из амниотической жидкости или пуповины.
шнур.
е. подтвердить резус-статус
плод. Если отец гомозиготен по аллелю D (D/D), плод будет
Д положительный. Однако, если отец гетерозиготен (D/d), вероятность 50:50
что плод D-положительный, и единственный способ точно узнать группу крови
заключается в тестировании образца клеток плода, взятого из амниотической жидкости или пуповины.
шнур.
Если плод резус-положительный, беременность тщательно контролируется на наличие признаков HDN. Мониторинг включает регулярное УЗИ плода и мониторинг количество анти-D в сыворотке крови матери. На активный гемолиз указывает рост анти-D. Если анализ крови плода подтверждает анемию плода, в зависимости от ее степени тяжести можно сделать переливание крови внутриутробно для замены лизированные фетальные эритроциты.
Переливание крови также может потребоваться для коррекции анемии в период новорожденности.
В этот период также может наблюдаться резкий подъем уровня билирубина в
у новорожденных, который можно снизить с помощью фототерапии и обменных трансфузий.
Ссылки
- 1.
Урбаниак С.Дж., Грейсс М.А. RhD-гемолитическая болезнь плода и новорожденного. Blood Rev. 2000; 14:44–61. [PubMed: 10805260]
- 2.
Гарратти Г., Глинн С.А., Макинтайр Р. Частоты фенотипов ABO и Rh(D) разных расовые/этнические группы в США. Переливание. 2004;44:703–6. [PubMed: 15104651]
Хирургия плода: риски и виды
Получение диагноза состояния плода — это эмоциональный опыт. Команда экспертов Banner Health всегда рядом, чтобы поддержать вас и помочь вам в принятии срочных решений, оказывая тщательную и заботливую помощь вам и вашему ребенку. Наши опытные специалисты по охране материнства и плода могут дополнительно предложить полный спектр диагностических тестов и вариантов лечения, если это необходимо.
В некоторых отделениях Banner Health круглосуточно работают специалисты по фетальной медицине (MFM). Специалисты MFM являются экспертами в области беременностей высокого риска. Они прошли продвинутую подготовку по уходу за женщинами с неожиданными проблемами во время беременности, а также по уходу за плодами еще не рожденных детей, например, по наблюдению, лечению и хирургическому вмешательству.
Они прошли продвинутую подготовку по уходу за женщинами с неожиданными проблемами во время беременности, а также по уходу за плодами еще не рожденных детей, например, по наблюдению, лечению и хирургическому вмешательству.
Что такое хирургия плода?
Нерожденным детям, у которых диагностированы врожденные дефекты или другие патологии плода, может потребоваться внутриутробная хирургия. Этот тип процедуры выполняется на плоде внутриутробно (еще в матке матери). Часто дефекты усугубляются по мере развития ребенка, поэтому раннее вмешательство до рождения имеет важное значение.
Младенцы, перенесшие внутриутробную хирургию, часто нуждаются в особом уходе после родов. Отделение интенсивной терапии новорожденных (ОИТН) Banner Health укомплектовано персоналом и полностью оборудовано для оказания деликатной помощи, в которой нуждается ваш новорожденный.
Риски операций на плоде
Операции на плоде сложны и трудны. Опытная команда Banner Health обеспечивает квалифицированную комплексную помощь как матери, так и будущему ребенку. Как и при любой операции, при хирургии плода существуют риски, включая разрыв матки, гибель плода, операционные осложнения, ранние роды и потенциальную неудачу лечения врожденного дефекта.
Как и при любой операции, при хирургии плода существуют риски, включая разрыв матки, гибель плода, операционные осложнения, ранние роды и потенциальную неудачу лечения врожденного дефекта.
Ваш врач объяснит вам все аспекты вашей процедуры, но обязательно задавайте вопросы. Важно, чтобы вы были проинформированы и довольны своим решением.
Насколько распространена хирургия плода?
По данным CDC, каждый 33-й ребенок рождается с врожденным дефектом – примерно 120 000 детей в год. Фетальная хирургия становится вариантом для растущего числа таких детей. Возможность вмешаться раньше и вылечить инвалидизирующие или смертельные врожденные дефекты дает семьям новую надежду.
Какие виды операций на плоде предлагает Banner Health?
Компания Banner Health предлагает следующие процедуры хирургии плода, чтобы обеспечить наилучшие результаты как для матери, так и для ребенка:
- Чрескожный забор пуповины и внутриматочное переливание плода: Диагностический пренатальный тест, также известный как кордоцентез, берет образец кровь ребенка из пуповины для выявления определенных генетических нарушений, состояний крови и инфекций.

