Содержание
Что такое протозойные инфекции: Невидимые враги нашего здоровья
Протозойные инфекции — это настоящие невидимки в мире болезней. Эти микроскопические паразиты умудряются проникать в наш организм, оставаясь незамеченными, и устраивают там настоящий переполох. Но как же распознать этих скрытных захватчиков? Давайте копнем глубже и разберемся, что к чему.
Коварные простейшие: кто они такие?
К возбудителям протозойных инфекций относятся одноклеточные организмы, которые, несмотря на свои крошечные размеры, способны вызывать серьезные проблемы со здоровьем. Эти микроскопические паразиты — настоящие мастера маскировки. Они могут годами жить в нашем теле, не вызывая явных симптомов, а потом внезапно активизироваться и устроить настоящую бурю.
Представьте себе армию крошечных солдат, которые проникают в крепость вашего организма. Они настолько малы, что проходят через все защитные барьеры незамеченными. А потом, когда вы меньше всего этого ожидаете, они начинают свою подрывную деятельность. Вот так и работают простейшие паразиты.
Симптомы: когда бить тревогу?
- Хроническая усталость и слабость
- Частые расстройства желудка
- Необъяснимая потеря веса
- Повышенная температура, которая держится долгое время
- Кожные высыпания или зуд
Конечно, эти симптомы могут быть вызваны и другими причинами. Но если вы заметили у себя несколько из них, особенно после путешествия в экзотические страны или контакта с загрязненной водой, стоит насторожиться.
Диагностика: как поймать невидимку?
Выявить протозойную инфекцию — задача не из легких. Эти хитрые паразиты умеют прятаться от наших диагностических методов. Но наука не стоит на месте, и современные лаборатории вооружены целым арсеналом для борьбы с этими микроскопическими врагами.
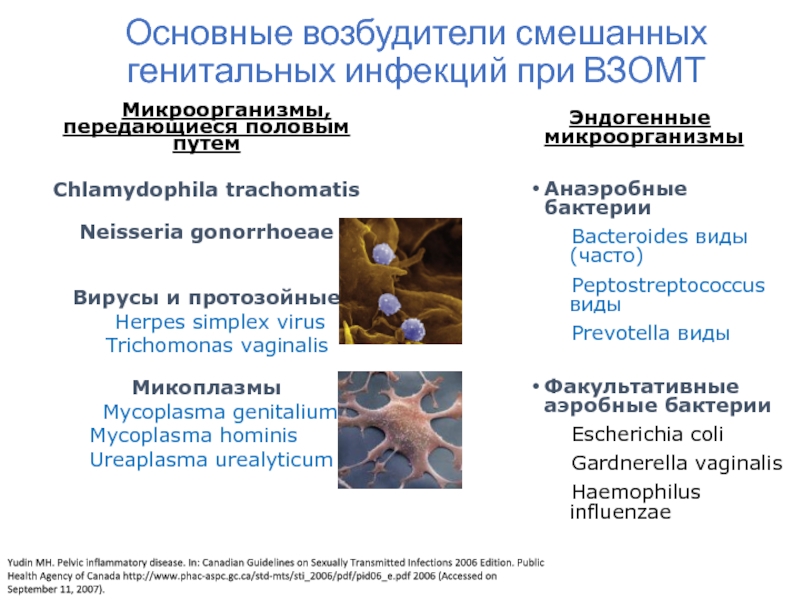
Основной метод диагностики — это анализ кала на яйца гельминтов и простейших. Звучит не очень аппетитно, согласен. Но это самый надежный способ поймать паразитов с поличным. Кроме того, врачи могут назначить анализ крови на антитела к конкретным видам простейших. Это как проверка на детекторе лжи — организм не сможет скрыть, что в нем поселились непрошеные гости.
Лечение: как изгнать захватчиков?
Когда диагноз поставлен, начинается самое интересное — борьба с паразитами. И тут в ход идет тяжелая артиллерия в виде антипротозойных препаратов. Эти лекарства — настоящие снайперы. Они точечно уничтожают простейших, не причиняя серьезного вреда нашему организму.
Но не думайте, что одной таблеткой можно решить все проблемы. Лечение протозойных инфекций — это целая военная операция, которая может длиться несколько недель или даже месяцев. Важно строго соблюдать схему приема препаратов и не прекращать лечение раньше времени, даже если вам кажется, что все симптомы уже прошли.
Профилактика: как не пустить врага на порог?
Знаете, как говорится — лучшая защита это нападение. В случае с протозойными инфекциями это означает, что лучше предотвратить заражение, чем потом бороться с его последствиями. Вот несколько простых, но эффективных мер предосторожности:
- Мойте руки. Да-да, это банально, но невероятно эффективно. Особенно после посещения общественных мест, контакта с животными или перед едой.
- Пейте только очищенную или кипяченую воду, особенно в путешествиях.
- Тщательно мойте фрукты и овощи перед употреблением.
- Избегайте контакта с фекалиями животных (это касается и уборки за домашними питомцами).
- При купании в открытых водоемах старайтесь не глотать воду.
Эти простые правила могут показаться очевидными, но именно они — ваш первый рубеж обороны от протозойных инфекций.
Мифы и реальность
Вокруг протозойных инфекций ходит множество мифов. Например, многие считают, что паразиты живут только в организме людей из развивающихся стран. Это не так! Простейшие не признают границ и социального статуса. Они могут поселиться в организме любого человека, независимо от того, где он живет и сколько зарабатывает.
Другой распространенный миф — что все паразитарные инфекции сопровождаются сильной болью в животе. На самом деле, многие протозойные инфекции протекают бессимптомно или с очень слабо выраженными симптомами. Именно поэтому они так опасны — человек может годами не подозревать о том, что в его организме живут непрошеные гости.
Исследования и перспективы
Наука не стоит на месте, и ученые постоянно ищут новые способы борьбы с протозойными инфекциями. Например, недавние исследования показали, что некоторые виды простейших могут быть чувствительны к определенным натуральным компонентам, таким как экстракт чеснока или некоторые эфирные масла. Это открывает новые перспективы для разработки более безопасных и эффективных методов лечения.
Кроме того, активно разрабатываются новые методы диагностики, которые позволят выявлять протозойные инфекции на самых ранних стадиях. Представьте себе тест, который сможет обнаружить даже одну клетку паразита в вашем организме! Звучит как научная фантастика, но ученые уверены, что в ближайшем будущем это станет реальностью.
Жизнь после диагноза
Если вам поставили диагноз «протозойная инфекция», не паникуйте. Да, это неприятно, но не смертельно. Современная медицина имеет в своем арсенале эффективные методы лечения. Главное — вовремя обратиться к врачу и строго следовать его рекомендациям.
После успешного лечения важно укрепить свой иммунитет. Ведь сильная иммунная система — это ваш личный телохранитель, который будет бдительно следить за тем, чтобы непрошеные гости больше не проникли в ваш организм. Правильное питание, регулярные физические нагрузки, полноценный сон — все это поможет вашему организму быстрее восстановиться и стать более устойчивым к различным инфекциям.
Протозойные инфекции — это не приговор, а всего лишь временное неудобство. С правильным подходом и своевременным лечением вы сможете быстро избавиться от непрошеных гостей и вернуться к полноценной жизни. Главное — не игнорировать симптомы и регулярно проходить профилактические обследования. Ведь ваше здоровье — в ваших руках!

Основные возбудители протозоозов: От малярийного плазмодия до лямблий
Мир протозойных инфекций — это настоящий микрокосмос, населенный удивительными и опасными созданиями. К возбудителям протозойных инфекций относятся одноклеточные организмы, способные превратить нашу жизнь в настоящий кошмар. Но кто же они, эти микроскопические злодеи? Давайте познакомимся с главными действующими лицами этого невидимого мира.
Малярийный плазмодий: король протозойных инфекций
Малярийный плазмодий — это настоящая суперзвезда среди возбудителей протозоозов. Этот микроскопический паразит ежегодно заражает миллионы людей по всему миру. Представьте себе крошечного вампира, который проникает в ваши красные кровяные тельца и устраивает там настоящий пир. Звучит как сюжет фильма ужасов, не так ли? Но для многих людей это суровая реальность.
Малярийный плазмодий передается через укусы комаров рода Anopheles. Эти насекомые — словно шприцы с крыльями, которые вводят паразитов прямо в наш кровоток. А дальше начинается настоящее веселье: периодические приступы лихорадки, озноб, потливость. И это только верхушка айсберга. Без своевременного лечения малярия может привести к серьезным осложнениям и даже смерти.
Токсоплазма: скрытая угроза
Токсоплазма — это настоящий мастер маскировки среди протозойных паразитов. Этот хитрец может годами жить в нашем организме, не вызывая никаких симптомов. Но стоит иммунитету ослабнуть, и токсоплазма тут как тут — готова устроить настоящий переполох.
Интересно, что токсоплазма может влиять даже на наше поведение. Некоторые исследования показывают, что зараженные люди становятся более склонными к риску. Представьте себе: микроскопический паразит, который может заставить вас прыгнуть с парашютом или поставить все деньги на красное в казино. Звучит как научная фантастика, но наука говорит, что это вполне возможно.
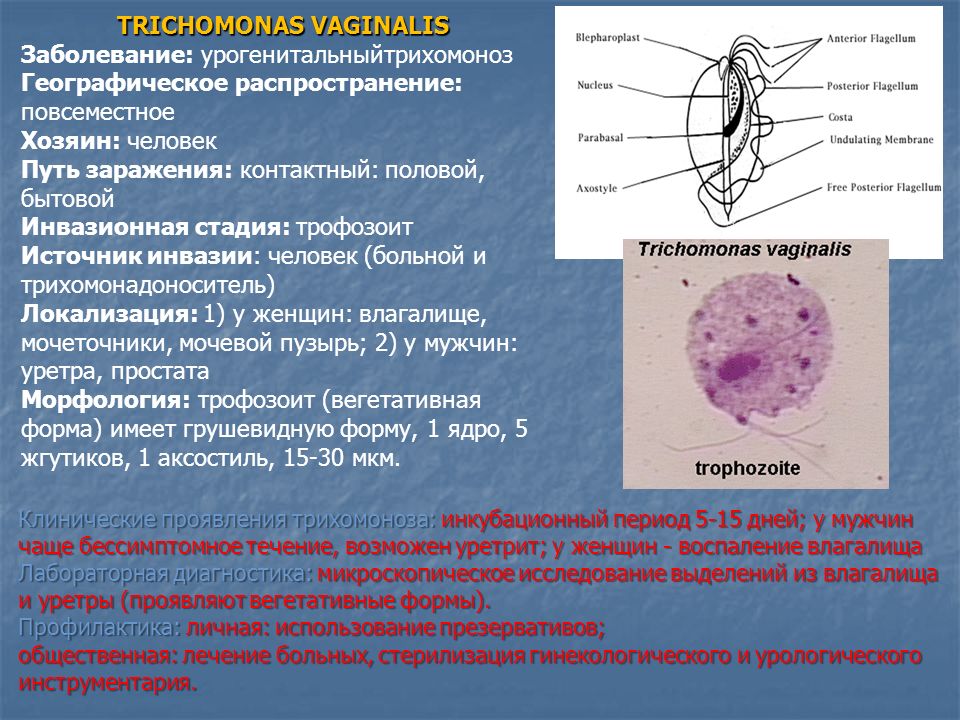
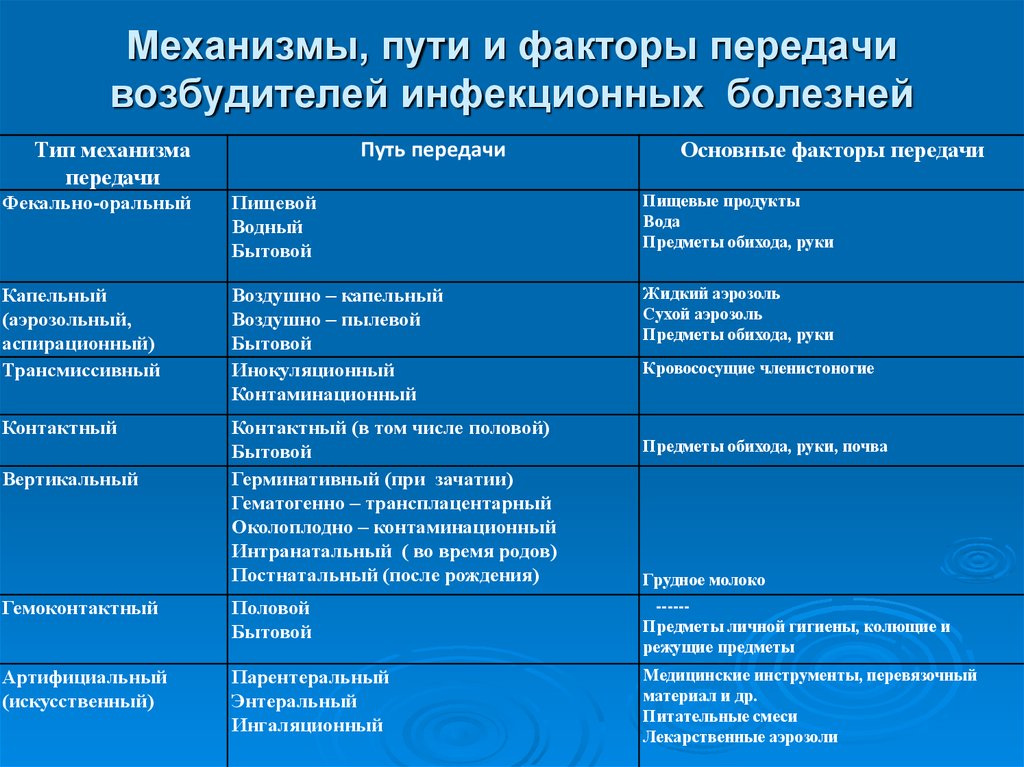
Лямблии: непрошеные гости в кишечнике
Лямблии — это настоящие squatters нашего кишечника. Эти маленькие паразиты обожают устраиваться в нашем пищеварительном тракте и устраивать там настоящую вечеринку. Результат? Диарея, боли в животе, тошнота — в общем, все «прелести» кишечных расстройств.

Но самое коварное в лямблиях — это их способность маскироваться под другие заболевания. Многие люди годами лечат «синдром раздраженного кишечника», не подозревая, что на самом деле в их организме поселились эти микроскопические паразиты. Вот так бывает: думаешь, что у тебя просто чувствительный желудок, а на самом деле в кишечнике идет настоящая война с лямблиями.
Трипаносомы: кровососы из Африки
Трипаносомы — это настоящие экзоты среди протозойных паразитов. Эти ребята вызывают сонную болезнь — заболевание, которое может буквально усыпить человека навсегда. Представьте себе: вы гуляете по африканской саванне, вас кусает муха цеце, и бац — через несколько недель вы начинаете чувствовать непреодолимую сонливость. Звучит как сюжет для фантастического рассказа, но для многих людей в Африке это суровая реальность.
Трипаносомы — настоящие мастера выживания. Они умеют менять свою внешнюю оболочку, чтобы иммунная система не могла их распознать. Это как если бы преступник постоянно менял маски, чтобы полиция не могла его поймать. Хитро, не правда ли?
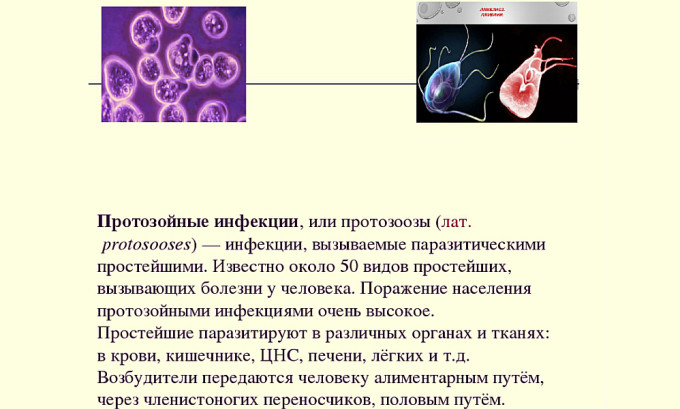
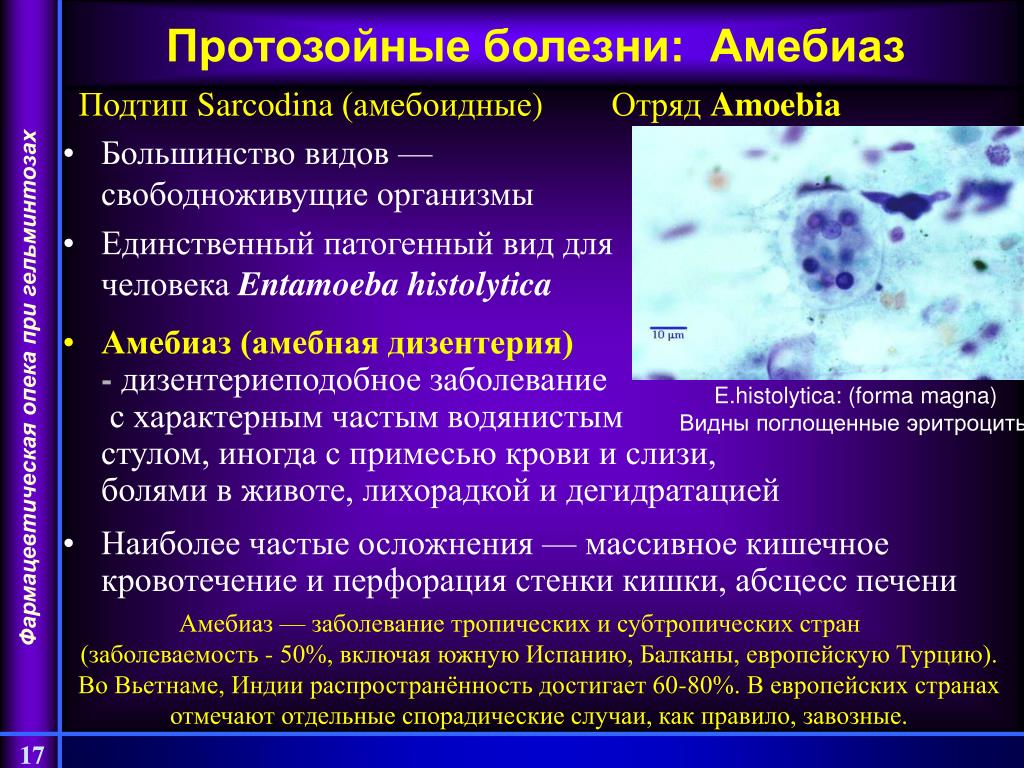
Амебы: жидкие убийцы
Амебы — это, пожалуй, самые странные из всех протозойных паразитов. Представьте себе живую каплю, которая может менять форму и проникать практически куда угодно. Звучит как описание персонажа из фильма «Терминатор», но это реальный организм.
Самая известная из амеб — это Entamoeba histolytica, возбудитель амебной дизентерии. Эта малышка способна буквально прогрызать ходы в стенках кишечника. Результат? Кровавая диарея, боли в животе и, если не лечиться, серьезные осложнения. А ведь все начинается с того, что человек выпил немного загрязненной воды или съел немытые фрукты. Вот такие они, эти микроскопические хищники.
Криптоспоридии: водоплавающие паразиты
Криптоспоридии — это настоящие water babies среди протозойных паразитов. Эти ребята обожают воду и могут выживать даже в хлорированных бассейнах. Представьте себе: вы приходите в бассейн, чтобы расслабиться и поплавать, а в итоге получаете «в подарок» целую колонию микроскопических паразитов.

Криптоспоридиоз, вызываемый этими паразитами, особенно опасен для людей с ослабленным иммунитетом. У таких пациентов он может вызвать тяжелую, изнуряющую диарею, которая буквально высасывает из организма все соки. Вот такие они, эти водные вампиры.
Балантидии: гиганты микромира
Балантидии — это настоящие гиганты среди протозойных паразитов. Если большинство простейших можно разглядеть только под микроскопом, то балантидий можно увидеть даже в обычную лупу. Это как если бы среди муравьев вдруг появился слон.
Но размер в данном случае не делает балантидий менее опасными. Эти ребята способны вызывать серьезные поражения кишечника, особенно у людей с ослабленным иммунитетом. Представьте себе микроскопического бульдозера, который прокладывает себе путь через стенки вашего кишечника. Примерно так и действуют балантидии.
Лейшмании: кожные террористы
Лейшмании — это настоящие специалисты по биологическому террору. Эти паразиты атакуют кожу и внутренние органы, вызывая заболевание под названием лейшманиоз. Представьте себе: вас укусила маленькая мушка, а через несколько недель на коже появляется язва, которая не заживает месяцами. Звучит как проклятие из фильма ужасов, но это реальное заболевание, с которым сталкиваются миллионы людей по всему миру.
Самое коварное в лейшманиозе — это его способность маскироваться под другие заболевания. Врачи часто путают его с раком кожи или другими инфекциями. А тем временем паразиты продолжают свою разрушительную работу. Вот такие они, эти микроскопические диверсанты.
Как защититься от этой невидимой армии?
Теперь, когда мы познакомились с основными «героями» мира протозойных инфекций, возникает логичный вопрос: как же защититься от этой невидимой армии? Ответ прост, но требует дисциплины:
- Мойте руки. Да-да, это банально, но невероятно эффективно. Особенно после посещения общественных мест и перед едой.
- Пейте только очищенную или кипяченую воду, особенно в путешествиях.
- Тщательно мойте фрукты и овощи перед употреблением.
- Используйте репелленты и москитные сетки в районах, где распространены малярия и лейшманиоз.
- Избегайте контакта с фекалиями животных.
- Проходите регулярные медицинские обследования, особенно если вы много путешествуете.
Помните: знание — сила. Теперь, когда вы знаете своих «врагов в лицо», вы можете лучше защитить себя от их атак. Ведь в мире протозойных инфекций лучшая защита — это профилактика. Будьте здоровы и не давайте микроскопическим паразитам шанса испортить вашу жизнь!

Симптомы и признаки: Когда бить тревогу при подозрении на протозойную инвазию
Протозойные инфекции — это настоящие мастера маскировки в мире болезней. Их симптомы часто настолько неспецифичны, что могут сойти за обычную простуду или расстройство желудка. Но не стоит недооценивать эти микроскопические угрозы! К возбудителям протозойных инфекций относятся одноклеточные паразиты, способные вызвать серьезные проблемы со здоровьем, если их вовремя не обнаружить и не начать лечение.
Общие симптомы: красные флажки, на которые стоит обратить внимание
Представьте себе, что ваш организм — это крепость, а простейшие — это невидимые захватчики. Как узнать, что крепость атакована? Вот несколько общих симптомов, которые могут сигнализировать о протозойной инвазии:
- Хроническая усталость (будто вы пробежали марафон, даже не вставая с дивана)
- Необъяснимая потеря веса (словно кто-то втихаря ворует ваши калории)
- Частые расстройства желудка (ваш кишечник устраивает «американские горки» без вашего согласия)
- Повышенная температура, которая держится долгое время (как будто ваш внутренний термостат сломался)
- Кожные высыпания или зуд (ваша кожа пытается подать сигнал SOS)
Конечно, эти симптомы могут быть вызваны и другими причинами. Но если вы заметили у себя несколько из них, особенно после путешествия в экзотические страны или контакта с загрязненной водой, пора насторожиться и обратиться к врачу.
Малярия: когда лихорадка бьет как часы
Малярия — это, пожалуй, самая известная из протозойных инфекций. Ее симптомы настолько характерны, что их трудно спутать с чем-то другим. Представьте себе, что в вашем организме поселился злобный будильник, который каждые 48-72 часа устраивает настоящий переполох.
Типичный приступ малярии выглядит так:
- Сначала вас бросает в озноб (будто вы оказались на Северном полюсе в купальнике)
- Затем температура подскакивает до небес (вы чувствуете себя как печка на максимуме)
- И наконец, вас прошибает холодный пот (словно вы только что увидели счет за коммунальные услуги)
Эти приступы повторяются с пугающей регулярностью. Если вы недавно вернулись из тропических стран и у вас начались такие «веселые качели», немедленно обращайтесь к врачу. Малярия — не та болезнь, с которой можно шутить.

Амебиаз: когда кишечник устраивает революцию
Амебиаз — это инфекция, вызываемая амебами, которые устраивают настоящий переворот в вашем кишечнике. Основные симптомы амебиаза могут включать:
- Диарею с примесью крови и слизи (ваш стул становится похожим на клубничное желе — простите за такое сравнение)
- Спазмы и боли в животе (словно в вашем животе поселился злой гном с молотком)
- Тошноту и рвоту (ваш желудок пытается устроить забастовку)
- Потерю аппетита (даже ваше любимое блюдо кажется невкусным)
Если вы заметили у себя эти симптомы, особенно после путешествия в страны с низким уровнем гигиены, не тяните с визитом к врачу. Амебиаз может привести к серьезным осложнениям, если его не лечить.
Лямблиоз: когда пищеварение превращается в квест
Лямблиоз — это инфекция, вызываемая паразитами, которые превращают ваш кишечник в настоящий лабиринт проблем. Симптомы лямблиоза могут быть очень разнообразными:
- Вздутие живота (словно вы проглотили воздушный шар)
- Тошнота и рвота (ваш желудок решил устроить генеральную уборку)
- Хроническая диарея (ваш кишечник работает как сломанный кран)
- Потеря веса (будто кто-то тайком высасывает из вас калории)
- Усталость и слабость (даже подъем с дивана кажется подвигом)
Лямблиоз часто путают с синдромом раздраженного кишечника или пищевой непереносимостью. Если вы заметили у себя эти симптомы, особенно если они держатся долгое время, стоит проверить свой организм на наличие этих микроскопических «квартирантов».
Токсоплазмоз: когда паразит играет в прятки
Токсоплазмоз — это инфекция-невидимка. У большинства людей с нормальным иммунитетом она протекает бессимптомно. Но если иммунитет ослаблен, токсоплазма может устроить настоящий переполох:
- Увеличение лимфоузлов (словно у вас под кожей растут маленькие шарики для пинг-понга)
- Головные боли и лихорадка (ваша голова превращается в печку)
- Усталость и мышечные боли (будто вы пробежали марафон во сне)
Особенно опасен токсоплазмоз для беременных женщин, так как может привести к серьезным нарушениям развития плода. Поэтому если вы беременны и заметили у себя эти симптомы, особенно если у вас есть кошка или вы любите есть сырое мясо, немедленно обратитесь к врачу.
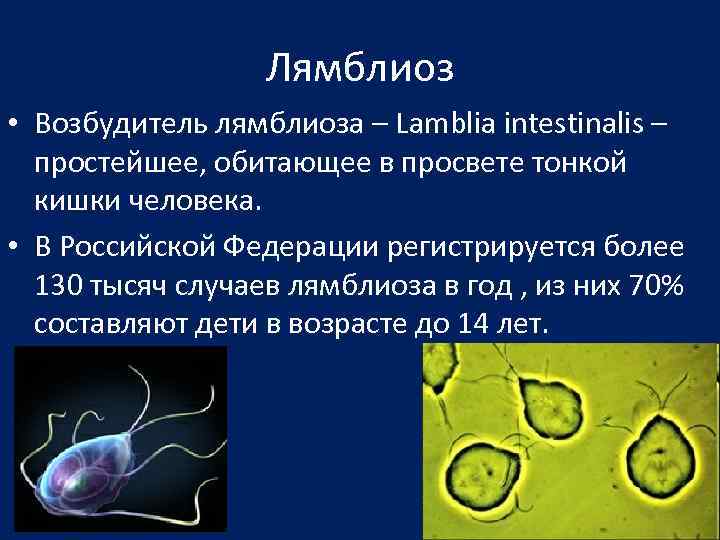
Трихомониаз: когда интимная зона бьет тревогу
Трихомониаз — это инфекция, которая в основном поражает мочеполовую систему. Ее симптомы могут включать:
- Неприятные выделения из половых органов (словно ваше тело решило устроить «генеральную уборку» в неподходящее время)
- Зуд и жжение в интимной зоне (будто вы случайно натерли эту область острым перцем)
- Боль при мочеиспускании (посещение туалета превращается в испытание на прочность)
Трихомониаз часто протекает бессимптомно, особенно у мужчин. Но это не значит, что его можно игнорировать. Если вы заметили у себя эти симптомы или у вас был незащищенный половой контакт с новым партнером, стоит провериться у врача.
Когда симптомы обманывают: скрытые угрозы
Самое коварное в протозойных инфекциях — это их способность маскироваться под другие заболевания или вообще не проявлять себя. Вот несколько ситуаций, когда стоит насторожиться, даже если явных симптомов нет:
- Вы недавно вернулись из путешествия в тропическую страну
- У вас был контакт с загрязненной водой или пищей
- Вы работаете с животными или часто контактируете с ними
- У вас ослаблен иммунитет (например, из-за ВИЧ или химиотерапии)
В этих случаях даже небольшое недомогание может быть сигналом тревоги. Лучше перестраховаться и пройти обследование, чем пропустить начало серьезной инфекции.
Когда пора бить в колокола: экстренные симптомы
Есть ситуации, когда медлить нельзя ни минуты. Если у вас появились следующие симптомы, особенно в сочетании с другими признаками протозойной инфекции, немедленно обращайтесь за медицинской помощью:
- Сильная головная боль и ригидность затылочных мышц (словно кто-то зажал вашу шею в тиски)
- Спутанность сознания или изменение поведения (будто ваш мозг решил поиграть в прятки)
- Судороги или потеря сознания (ваше тело устраивает «бунт на корабле»)
- Сильная боль в животе (словно внутри вас взорвалась маленькая бомба)
- Обильное кровотечение из прямой кишки (ваш кишечник превратился в неисправный водопровод)
Эти симптомы могут указывать на серьезные осложнения протозойных инфекций, такие как абсцесс печени при амебиазе или церебральная малярия. В таких случаях счет идет на часы, и промедление может стоить жизни.
Помните, что своевременное обращение к врачу — ключ к успешному лечению протозойных инфекций. Не стоит заниматься самодиагностикой или самолечением. Эти микроскопические паразиты слишком хитры и опасны, чтобы сражаться с ними в одиночку. Будьте внимательны к своему организму, прислушивайтесь к его сигналам, и не стесняйтесь обращаться за профессиональной помощью. Ваше здоровье — это та крепость, которую стоит защищать всеми силами!
Диагностика простейших: Современные методы выявления паразитов
В мире микроскопических угроз, где к возбудителям протозойных инфекций относятся хитрые и коварные одноклеточные организмы, диагностика становится настоящим детективным расследованием. Представьте себе: вы — Шерлок Холмс мира медицины, а простейшие — это неуловимые преступники, которых нужно поймать. Как же выследить этих микроскопических злодеев?
Микроскопия: классика жанра
Начнем с самого очевидного — микроскопии. Это как если бы вы взяли лупу и отправились на поиски следов преступления. Только вместо лупы у нас микроскоп, а вместо следов — образцы кала, мочи или крови. Звучит не очень аппетитно, согласен, но что поделать — такова цена здоровья!
Микроскопия позволяет нам буквально увидеть паразитов «в лицо». Представьте, что вы смотрите на каплю воды из лужи под микроскопом — примерно так же выглядит и поиск простейших в биологических образцах. Этот метод особенно эффективен для диагностики таких инфекций, как:
- Амебиаз (когда амебы устраивают вечеринку в вашем кишечнике)
- Лямблиоз (эти ребята любят «кататься» на волнах вашего пищеварительного тракта)
- Малярия (когда ваша кровь превращается в «курорт» для плазмодиев)
Но у микроскопии есть свои подводные камни. Во-первых, нужен опытный специалист, который сможет отличить простейших от других микроорганизмов или клеток организма. Во-вторых, паразиты могут быть очень хитрыми и прятаться, выделяясь в образцы не постоянно. Поэтому иногда приходится делать несколько анализов, чтобы поймать этих микроскопических «преступников» с поличным.

Серологические тесты: охота на антитела
Если микроскопия — это поиск самих преступников, то серологические тесты — это поиск следов их пребывания в организме. Представьте, что ваша иммунная система — это полиция, которая оставляет «ориентировки» на разыскиваемых паразитов. Эти «ориентировки» — антитела, которые мы и ищем в крови.
Серологические тесты особенно полезны для диагностики таких инфекций, как:
- Токсоплазмоз (когда ваш мозг становится «убежищем» для хитрых токсоплазм)
- Амебиаз (эти ребята оставляют после себя «улики» в виде антител)
- Лейшманиоз (когда ваша кожа становится полем боя с микроскопическими захватчиками)
Но и у этого метода есть свои ограничения. Антитела могут сохраняться в организме долгое время после выздоровления, что может привести к ложноположительным результатам. Кроме того, у людей с ослабленным иммунитетом антитела могут вообще не вырабатываться. Поэтому серологические тесты часто используются в комбинации с другими методами диагностики.
ПЦР: молекулярная охота на паразитов
ПЦР (полимеразная цепная реакция) — это как если бы у вас был суперкомпьютер, способный найти преступника по одной молекуле ДНК. Этот метод позволяет обнаружить генетический материал паразитов даже в очень малых количествах. Представьте, что вы ищете иголку в стоге сена, но у вас есть магнит, который притягивает только эту конкретную иголку — вот так работает ПЦР.
ПЦР особенно эффективна для диагностики таких инфекций, как:
- Малярия (когда нужно найти плазмодиев среди миллиардов ваших собственных клеток крови)
- Токсоплазмоз (эти хитрецы могут прятаться годами, но ПЦР их все равно найдет)
- Трихомониаз (когда нужно обнаружить этих микроскопических «хулиганов» в мочеполовой системе)
ПЦР — очень чувствительный и специфичный метод, но он тоже не идеален. Он может быть дорогим и не всегда доступным в некоторых регионах. Кроме того, ПЦР может обнаруживать ДНК мертвых паразитов, что может привести к ложноположительным результатам после успешного лечения.
Культуральный метод: выращиваем «преступников»
Культуральный метод — это как если бы вы создали идеальные условия для преступников, чтобы они вышли из укрытия. Мы берем образец, помещаем его в питательную среду и ждем, пока паразиты не начнут размножаться. Звучит немного как научная фантастика, не правда ли?

Этот метод особенно полезен для диагностики таких инфекций, как:
- Трихомониаз (эти ребята любят «вечеринки» в специальных питательных средах)
- Лейшманиоз (когда нужно вырастить целую колонию этих микроскопических паразитов)
- Амебиаз (амебы в лаборатории чувствуют себя как дома)
Культуральный метод позволяет не только обнаружить паразитов, но и изучить их свойства, например, чувствительность к различным лекарствам. Однако у этого метода есть свои недостатки: он требует времени (иногда несколько недель) и специального оборудования.
Иммунохроматографические тесты: экспресс-детективы
Представьте себе тест на беременность. Помните, как это работает? Две полоски — беременна, одна — нет. Теперь представьте, что вместо беременности мы определяем наличие паразитов. Вот так работают иммунохроматографические тесты!
Эти тесты особенно полезны для быстрой диагностики в полевых условиях, например:
- Малярии (когда каждая минута на счету, и нужно быстро начать лечение)
- Лейшманиоза (эти тесты могут «поймать» паразитов даже в отдаленных районах)
- Амебиаза (когда нужно быстро понять, что творится в вашем кишечнике)
Иммунохроматографические тесты дают результат за считанные минуты и не требуют специального оборудования. Однако они могут быть менее чувствительными, чем другие методы, и иногда дают ложноположительные или ложноотрицательные результаты.
Комплексный подход: когда один метод хорошо, а несколько — лучше
В реальности врачи редко ограничиваются одним методом диагностики. Это как если бы детектив использовал и отпечатки пальцев, и показания свидетелей, и анализ ДНК. Комбинация различных методов позволяет повысить точность диагностики и не упустить коварных паразитов.
Например, при подозрении на малярию врач может назначить:
- Микроскопию мазка крови (чтобы увидеть паразитов «в лицо»)
- Быстрый иммунохроматографический тест (для экспресс-диагностики)
- ПЦР (для подтверждения диагноза и определения вида плазмодия)
Такой комплексный подход позволяет не только поставить точный диагноз, но и выбрать наиболее эффективное лечение.

Будущее диагностики: что нас ждет?
Мир не стоит на месте, и методы диагностики протозойных инфекций постоянно совершенствуются. Что же нас ждет в будущем?
- CRISPR-диагностика: представьте, что у вас есть молекулярные ножницы, которые могут «разрезать» ДНК паразитов с невероятной точностью. Звучит как научная фантастика, но это уже реальность!
- Искусственный интеллект в микроскопии: компьютеры учатся распознавать паразитов быстрее и точнее, чем человеческий глаз.
- Нанотехнологии: микроскопические роботы, способные путешествовать по нашему организму в поисках паразитов. Пока это только в фантастических фильмах, но кто знает, что будет через 10-20 лет?
Диагностика протозойных инфекций — это настоящее искусство, сочетающее в себе передовые технологии и опыт специалистов. Это как игра в кошки-мышки, где мы — кошки, а простейшие — очень хитрые мыши. Но с каждым годом наши «когти» становятся все острее, а «нюх» — все тоньше. Так что у микроскопических паразитов становится все меньше шансов остаться незамеченными!
Лечение и профилактика: Эффективные стратегии борьбы с простейшими
Когда речь заходит о борьбе с протозойными инфекциями, мы словно вступаем в настоящую войну с микроскопическими захватчиками. К возбудителям протозойных инфекций относятся хитрые и изворотливые одноклеточные организмы, которые могут превратить нашу жизнь в настоящий кошмар. Но не стоит отчаиваться! У нас в арсенале есть мощное оружие и надежные щиты. Давайте разберемся, как же победить этих невидимых врагов и не дать им шанса на реванш.
Антипротозойные препараты: тяжелая артиллерия
Представьте себе, что ваш организм — это крепость, а простейшие — армия захватчиков. Антипротозойные препараты в этой аналогии — это наша тяжелая артиллерия. Они бьют точно в цель, уничтожая паразитов, но при этом стараются не задеть «мирное население» — клетки нашего организма.
Какие же «пушки» у нас есть на вооружении?
- Метронидазол — настоящий универсальный солдат. Он эффективен против многих простейших, включая лямблий и трихомонад. Это как швейцарский нож в мире антипротозойных препаратов.
- Хлорохин — специалист по борьбе с малярией. Этот препарат словно снайпер, который выслеживает малярийных плазмодиев в наших эритроцитах.
- Тинидазол — близкий родственник метронидазола, но с некоторыми преимуществами. Он как усовершенствованная модель уже проверенного оружия.
- Фуразолидон — эффективен против лямблий и некоторых других простейших. Это как гранатомет в нашем арсенале — мощный, но требует осторожного обращения.
Но помните, что любое мощное оружие требует умелого обращения. Антипротозойные препараты могут вызывать побочные эффекты, поэтому их нужно применять только по назначению врача и строго следовать инструкции. Это как в армии — нельзя просто так взять и начать палить из пушки!
Поддерживающая терапия: укрепляем оборону
Одной только атакой на паразитов не обойтись. Нужно еще и укреплять собственные силы организма. Это как ремонтировать стены крепости во время осады. Что же входит в нашу поддерживающую терапию?
- Регидратация — восстановление водного баланса. Это особенно важно при инфекциях, сопровождающихся диареей. Представьте, что вы заливаете водой пересохшие рвы вокруг крепости.
- Пробиотики — для восстановления микрофлоры кишечника. Это как если бы вы призвали на помощь армию дружественных микроорганизмов.
- Витамины и минералы — для поддержки иммунной системы. Считайте это дополнительным питанием для ваших «солдат» — клеток иммунной системы.
- Противовоспалительные средства — чтобы уменьшить повреждения, нанесенные паразитами. Это как бригада скорой помощи, которая лечит раненых во время битвы.
Помните, что поддерживающая терапия — это не менее важная часть лечения, чем прием антипротозойных препаратов. Нельзя победить врага, если твои собственные силы на исходе!
Народные средства: помощники или обуза?
А как насчет народных средств? Многие люди верят в силу чеснока, тыквенных семечек или полыни в борьбе с паразитами. Но действительно ли они эффективны?
С одной стороны, некоторые растения действительно обладают антипаразитарными свойствами. Например, чеснок содержит аллицин, который может подавлять рост некоторых простейших. Это как если бы у вас в садке стояш чемодачник со «слезоточивым газом» против микроскопических захватчиков.
Но с другой стороны, эффективность народных средств часто не подтверждена клиническими исследованиями, а их применение может быть опасным. Это как если бы вы решили защищать крепость с помощью самодельного оружия — может сработать, а может и навредить.
Поэтому лучше всего обсудить применение любых народных средств с врачом. Пусть они будут дополнением к основной терапии, а не ее заменой.
Профилактика: лучшая защита — это нападение?
А теперь поговорим о том, как не допустить вторжения паразитов в нашу «крепость». Ведь лучшая битва — это та, которой удалось избежать, верно?

Вот несколько ключевых стратегий профилактики протозойных инфекций:
- Гигиена рук — это как регулярная чистка оружия. Мойте руки часто и тщательно, особенно перед едой и после посещения туалета.
- Чистая вода — не пейте воду из непроверенных источников. Это все равно что оставить ворота крепости открытыми.
- Тщательная обработка пищи — хорошо мойте фрукты и овощи, избегайте сырого или недоваренного мяса. Считайте это проверкой всех припасов, поступающих в крепость.
- Защита от насекомых — используйте репелленты и москитные сетки в районах, эндемичных по малярии. Это как выставить дополнительную охрану на стенах.
- Избегайте контакта с фекалиями животных — особенно при работе в саду или уборке за питомцами. Представьте, что это потенциально зараженная территория.
Помните, что профилактика — это не разовая акция, а образ жизни. Это как постоянная боевая готовность вашей крепости.
Вакцинация: мечта или реальность?
А что насчет вакцин? Увы, в отличие от многих бактериальных и вирусных инфекций, для большинства протозоозов эффективных вакцин пока не существует. Это как если бы у нас не было возможности провести предварительную подготовку наших «войск» к конкретному противнику.
Однако наука не стоит на месте. Ведутся активные исследования по разработке вакцин против малярии, лейшманиоза и других протозойных инфекций. Например, вакцина RTS,S/AS01 против малярии уже прошла клинические испытания и рекомендована ВОЗ для использования в эндемичных регионах Африки.
Кто знает, может быть через несколько лет у нас появится целый арсенал вакцин против простейших? Это было бы настоящей революцией в борьбе с протозойными инфекциями!
Глобальные стратегии: битва на мировой арене
Борьба с протозойными инфекциями — это не только личное дело каждого человека, но и глобальная задача. Всемирная организация здравоохранения (ВОЗ) и другие международные организации разрабатывают и реализуют масштабные программы по борьбе с этими заболеваниями.
Например, программа по элиминации малярии включает в себя:
- Массовое распространение москитных сеток, обработанных инсектицидами
- Улучшение диагностики и лечения в эндемичных регионах
- Распыление инсектицидов в помещениях
- Осушение водоемов, где размножаются комары
Это как если бы против армии паразитов выступила целая коалиция стран со всеми своими ресурсами. И знаете что? Эта стратегия работает! За последние 20 лет удалось значительно снизить заболеваемость и смертность от малярии во многих регионах мира.
Будущее борьбы с простейшими: что нас ждет?
Наука не стоит на месте, и методы борьбы с протозойными инфекциями постоянно совершенствуются. Вот несколько перспективных направлений:
- Генная инженерия комаров — создание популяций, устойчивых к малярийным плазмодиям. Это как если бы мы превратили армию противника в наших союзников!
- Разработка новых лекарств с использованием искусственного интеллекта. Представьте, что у нас появится суперкомпьютер, способный создавать идеальное «оружие» против каждого конкретного паразита.
- Использование наночастиц для точечной доставки лекарств. Это будет похоже на отряд микроскопических снайперов, которые уничтожают только вражеских солдат, не трогая мирных жителей.
Борьба с протозойными инфекциями — это непрерывный процесс, требующий постоянного совершенствования наших «вооружений» и стратегий. Но с каждым годом мы становимся все сильнее в этой борьбе. Кто знает, может быть через пару десятилетий протозойные инфекции станут такой же редкостью, как оспа или полиомиелит?
А пока что помните: ваше здоровье — это крепость, которую нужно защищать всеми доступными средствами. Соблюдайте правила гигиены, будьте внимательны к симптомам, не занимайтесь самолечением и регулярно проходите медицинские осмотры. И тогда никакие микроскопические захватчики не смогут нарушить ваш покой!
Иммунитет против протозоа: Как укрепить защитные силы организма
Протозойные инфекции — настоящие невидимки в мире заболеваний. Эти микроскопические паразиты могут годами жить в нашем организме, не вызывая явных симптомов. Но стоит иммунитету ослабнуть, и они тут как тут — готовы атаковать. Как же распознать этих скрытых врагов и защитить себя от их коварных планов? Давайте разберемся!

К возбудителям протозойных инфекций относятся одноклеточные организмы, такие как лямблии, трихомонады, токсоплазмы и малярийные плазмодии. Эти микроскопические паразиты могут проникать в наш организм через загрязненную воду, пищу или при контакте с инфицированными людьми и животными. Они настолько малы, что их невозможно увидеть невооруженным глазом, но последствия их присутствия могут быть весьма ощутимыми.
Представьте себе, что ваш организм — это крепость, а иммунная система — ее защитники. Протозоа — это коварные лазутчики, которые пытаются проникнуть внутрь незамеченными. Они могут использовать различные уловки, чтобы обмануть бдительность иммунных клеток. Например, токсоплазма способна «прятаться» внутри клеток хозяина, становясь невидимой для иммунной системы. А малярийный плазмодий и вовсе может менять свою внешнюю оболочку, словно переодеваясь в разные костюмы, чтобы сбить с толку защитников организма.
Как же понять, что в вашей «крепости» завелись непрошеные гости? Симптомы протозойных инфекций могут быть весьма разнообразными и неспецифичными. Это делает их диагностику настоящим вызовом для врачей. Часто первыми звоночками становятся общая слабость, утомляемость, снижение аппетита. У некоторых людей может наблюдаться повышение температуры, головные боли или боли в мышцах. При поражении желудочно-кишечного тракта (например, лямблиозе) могут возникать тошнота, диарея, вздутие живота.
Но здесь кроется одна из главных опасностей протозойных инфекций — они мастера маскировки. Их симптомы легко спутать с другими заболеваниями или списать на обычную усталость. Многие люди годами живут с такими паразитами, даже не подозревая об их присутствии. А ведь чем дольше протозоа находятся в организме, тем больший вред они могут нанести.
Скрытые угрозы протозойных инфекций
Почему же так важно вовремя выявить и начать лечение протозойных инфекций? Дело в том, что эти микроорганизмы способны вызывать серьезные нарушения в работе различных органов и систем. Например, токсоплазмоз может привести к поражению головного мозга и глаз, особенно опасен он для беременных женщин и людей с ослабленным иммунитетом. Лямблиоз нарушает работу желудочно-кишечного тракта, вызывая мальабсорбцию — нарушение всасывания питательных веществ. А малярия и вовсе может стать смертельно опасной, если вовремя не начать лечение.

Но не спешите паниковать! Наш организм не беззащитен перед лицом этих микроскопических захватчиков. Иммунная система — это сложный и эффективный механизм защиты, который постоянно совершенствуется в борьбе с различными патогенами. При встрече с протозоа она запускает целый каскад защитных реакций. Т-лимфоциты, словно разведчики, обнаруживают чужаков и подают сигнал тревоги. В ответ активируются макрофаги — клетки-пожиратели, которые атакуют и уничтожают паразитов. Одновременно В-лимфоциты начинают производить специфические антитела, которые помогают нейтрализовать протозоа и их токсины.
Интересно, что наш иммунитет способен «запоминать» встречу с конкретными видами протозоа. После первого контакта с паразитом в организме формируются клетки памяти. При повторном заражении они быстро активируются и запускают мощный иммунный ответ, не давая инфекции развиться. Это объясняет, почему люди, живущие в эндемичных районах (например, в некоторых тропических странах), часто обладают более высокой устойчивостью к определенным протозойным инфекциям.
Как укрепить защиту от протозойных инфекций?
Существует ли способ сделать нашу «крепость» неприступной для протозоа? К сожалению, абсолютной защиты не существует, но мы можем значительно усилить свои оборонительные рубежи. Вот несколько проверенных стратегий:
- Соблюдение правил гигиены. Это may звучит банально, но именно тщательное мытье рук, фруктов и овощей может предотвратить попадание многих протозоа в организм.
- Правильное питание. Сбалансированный рацион, богатый витаминами и минералами, помогает поддерживать иммунитет в тонусе. Особенно важны продукты, содержащие цинк, селен, витамины С и D.
- Физическая активность. Регулярные умеренные нагрузки стимулируют работу иммунной системы, повышая ее эффективность в борьбе с различными патогенами.
- Управление стрессом. Хронический стресс — настоящий враг иммунитета. Медитация, йога, дыхательные практики помогут снизить уровень стресса и укрепить защитные силы организма.
- Здоровый сон. Во время сна наш организм восстанавливается и перезагружает иммунную систему. Недостаток сна может сделать нас более уязвимыми перед инфекциями.
Отдельно стоит упомянуть о пробиотиках и пребиотиках. Исследования показывают, что здоровая микрофлора кишечника играет важную роль в защите от протозойных инфекций. Полезные бактерии не только создают неблагоприятную среду для размножения паразитов, но и стимулируют иммунный ответ. Включение в рацион ферментированных продуктов (йогурт, кефир, квашеная капуста) и пищевых волокон может стать еще одним щитом в вашей защите.

А что делать, если вы подозреваете у себя протозойную инфекцию? Первым делом — не заниматься самолечением! Диагностика этих заболеваний требует специальных лабораторных исследований. Только врач может правильно интерпретировать результаты анализов и назначить эффективное лечение. Современная медицина располагает целым арсеналом противопаразитарных препаратов, которые позволяют успешно бороться с протозойными инфекциями.
Важно помнить, что профилактика всегда эффективнее лечения. Особую осторожность следует проявлять при путешествиях в страны с высоким риском заражения протозойными инфекциями. Использование репеллентов, москитных сеток, кипячение воды — эти простые меры могут уберечь вас от серьезных проблем со здоровьем.
В заключение хочется отметить, что наш организм — удивительная самовосстанавливающаяся система. При правильном подходе мы можем значительно усилить свою защиту от протозойных инфекций и других патогенов. Регулярные профилактические осмотры, внимательное отношение к своему здоровью и здоровый образ жизни — вот ключи к крепкому иммунитету и долгой активной жизни. Помните: ваше здоровье — в ваших руках!
Путешествия и протозойные инфекции: Меры предосторожности для туристов
Путешествия открывают перед нами новые горизонты, дарят незабываемые впечатления и обогащают наш жизненный опыт. Но, отправляясь в экзотические страны, мы порой забываем о невидимых опасностях, которые могут подстерегать нас на каждом шагу. Речь идет о протозойных инфекциях — коварных заболеваниях, вызываемых одноклеточными паразитами. Эти микроскопические «хитрецы» способны превратить долгожданный отпуск в настоящий кошмар. Как же обезопасить себя и не стать «сувениром» для непрошеных гостей?
К возбудителям протозойных инфекций относятся различные виды простейших организмов, которые приспособились паразитировать в человеческом теле. Среди них — печально известная лямблия, вызывающая неприятные «сюрпризы» в работе желудочно-кишечного тракта, коварная токсоплазма, способная нанести серьезный урон здоровью будущих мам, и зловещий малярийный плазмодий, чье имя наводит ужас на путешественников в тропических странах.

Представьте, что ваше тело — это уютный «отель», а протозоа — непрошеные постояльцы, которые норовят заселиться без регистрации и оплаты. Они могут проникнуть через «парадный вход» (рот) с загрязненной водой или пищей, или же найти «черный ход» — например, через укус насекомого-переносчика. Оказавшись внутри, эти микроскопические «квартиранты» начинают активно обживаться, нанося ущерб вашему здоровью.
Как распознать незваных гостей?
Симптомы протозойных инфекций зачастую настолько неспецифичны, что их легко спутать с обычным пищевым отравлением или акклиматизацией. Вот почему так важно быть внимательным к сигналам своего организма. Общая слабость, утомляемость, снижение аппетита — эти первые «звоночки» могут говорить о том, что в вашем «отеле» поселились нежелательные микрогости.
При поражении желудочно-кишечного тракта (например, при лямблиозе) могут возникнуть тошнота, диарея, вздутие живота. А вот малярия способна устроить настоящие «американские горки» с температурой — периоды жара сменяются ознобом, заставляя вас буквально трястись под несколькими одеялами. Токсоплазмоз же может долгое время протекать бессимптомно, но при ослаблении иммунитета способен нанести удар по центральной нервной системе и органам зрения.
Профилактика — лучшее лекарство
Как же не допустить заселения этих нежелательных «постояльцев»? Вот несколько ключевых правил, которые помогут сохранить ваш организм свободным от протозойных захватчиков:
- Вода — только бутилированная или кипяченая. Забудьте о романтике питья из горных ручьев — они могут стать источником неприятных сюрпризов.
- Фрукты и овощи — тщательно мыть и по возможности очищать от кожуры. Не поленитесь потратить лишнюю минуту на гигиену — ваш организм скажет вам спасибо.
- Мясо и рыба — только после хорошей термической обработки. Экзотические блюда вроде сырой рыбы лучше оставить для ресторанов с проверенной репутацией.
- Насекомые — ваши главные враги. Используйте репелленты, москитные сетки и закрытую одежду, особенно в вечернее и ночное время.
Но что делать, если вы все-таки подозреваете, что стали «хозяином» для непрошеных микрогостей? Первым делом — не паниковать и не заниматься самолечением! Протозойные инфекции требуют точной диагностики и грамотного лечения. Обратитесь к врачу, специализирующемуся на тропических болезнях. Современная медицина располагает эффективными методами диагностики и лечения протозойных инфекций.
Укрепляем защиту: Как повысить устойчивость к протозойным инфекциям
Представьте, что ваш организм — это крепость, а иммунная система — ее гарнизон. Чем сильнее и подготовленнее будут ваши «защитники», тем меньше шансов у протозойных захватчиков преодолеть оборону. Вот несколько стратегий для укрепления вашей «крепости»:
- Правильное питание. Ваш рацион должен быть богат витаминами и минералами. Особое внимание уделите продуктам, содержащим цинк, селен, витамины С и D — они играют ключевую роль в поддержании иммунитета.
- Физическая активность. Регулярные умеренные нагрузки — это как тренировки для вашего иммунного «гарнизона». Они помогают поддерживать защитные силы организма в тонусе.
- Управление стрессом. Хронический стресс — настоящая «пятая колонна» для вашего иммунитета. Медитация, йога, дыхательные практики помогут снизить уровень стресса и укрепить защитные силы организма.
- Здоровый сон. Во время сна ваш организм не просто отдыхает, а проводит «техобслуживание» иммунной системы. Недостаток сна может сделать вас более уязвимыми перед инфекциями.
- Пробиотики и пребиотики. Здоровая микрофлора кишечника — это ваши союзники в борьбе с протозойными инфекциями. Включите в рацион ферментированные продукты и пищевые волокна.
Интересный факт: исследования показывают, что люди, регулярно практикующие закаливание, менее подвержены протозойным инфекциям. Это связано с тем, что умеренный стресс от холодовых процедур стимулирует выработку защитных факторов в организме. Но помните — начинать закаливание нужно постепенно и под контролем специалиста.
Экзотика без риска: Как путешествовать и оставаться здоровым
Путешествия в экзотические страны — это прекрасно, но они требуют особой подготовки. Вот несколько советов, которые помогут вам наслаждаться новыми впечатлениями без риска для здоровья:
- Заранее узнайте о эпидемиологической обстановке в стране назначения. Информацию можно получить в туристических агентствах или на сайтах здравоохранительных организаций.
- Сделайте необходимые прививки. Некоторые страны требуют сертификат о вакцинации при въезде.
- Соберите аптечку первой помощи, включив в нее средства от диареи, жаропонижающие препараты и антисептики.
- Будьте осторожны с уличной едой. Как бы аппетитно она ни выглядела, риск заражения протозойными инфекциями в таких местах особенно высок.
- Не пренебрегайте страховкой. Медицинская помощь за границей может стоить очень дорого.
А что, если вы все-таки почувствовали себя плохо во время путешествия? Не стоит терпеть и надеяться, что «само пройдет». Обратитесь за медицинской помощью как можно скорее. Многие отели сотрудничают с местными клиниками и могут помочь вам получить квалифицированную помощь.

Мифы и реальность: Что нужно знать о протозойных инфекциях
Вокруг протозойных инфекций существует немало мифов. Давайте разберем некоторые из них:
Миф 1: «Протозойные инфекции встречаются только в тропических странах». Это не так. Хотя риск заражения действительно выше в теплом и влажном климате, некоторые виды простейших (например, лямблии) широко распространены и в умеренных широтах.
Миф 2: «Если я уже болел малярией, у меня иммунитет». К сожалению, переболев малярией один раз, вы не получаете пожизненный иммунитет. Малярийный плазмодий способен мутировать, обходя защиту организма.
Миф 3: «Протозойные инфекции всегда проявляются явными симптомами». Это опасное заблуждение. Многие протозойные инфекции могут протекать бессимптомно или с неспецифическими симптомами, что затрудняет их своевременное выявление.
Понимание реальных рисков и правильных мер профилактики поможет вам наслаждаться путешествиями без лишних страхов и с минимальным риском для здоровья. Помните: ваше здоровье — в ваших руках, и правильная подготовка к путешествию — ключ к незабываемым и безопасным приключениям!
