Содержание
Стволовые клетки: ключ к регенеративной медицине будущего
Воображали ли вы когда-нибудь мир, где любой орган можно восстановить, а старение — обратить вспять? Звучит как научная фантастика, не так ли? Но что, если я скажу вам, что ключ к этому фантастическому будущему уже хранится в специальных хранилищах по всему миру? Да-да, речь идет о банках стволовых клеток — настоящих сокровищницах потенциального бессмертия!
Стволовые клетки — это удивительные строительные блоки нашего организма, способные превращаться практически в любой тип клеток. Представьте себе волшебный конструктор, из которого можно собрать что угодно — от нейронов мозга до клеток сердечной мышцы. Круто, правда? Именно поэтому ученые возлагают на них такие большие надежды в области регенеративной медицины.
Но откуда же берутся эти чудо-клетки? Основные источники — это пуповинная кровь новорожденных, костный мозг взрослых людей и даже жировая ткань! Кто бы мог подумать, что наш лишний жирок может оказаться настоящим кладезем молодости? Однако самые «мощные» стволовые клетки получают из эмбрионов на ранних стадиях развития. Правда, тут возникает куча этических вопросов, поэтому ученые активно ищут альтернативные источники.
А теперь представьте себе огромное хранилище, заполненное контейнерами с жидким азотом при температуре -196°C. Именно так выглядит современный банк стволовых клеток! Здесь в специальных криопробирках хранятся миллионы образцов, каждый из которых может однажды спасти чью-то жизнь. Круто, да? Но как это работает на практике?
Допустим, вы решили сохранить стволовые клетки из пуповинной крови вашего новорожденного малыша. После родов врач собирает кровь из пуповины (это абсолютно безболезненно и безопасно как для мамы, так и для ребенка). Затем образец отправляется в лабораторию, где из него выделяют стволовые клетки. Их проверяют на жизнеспособность, считают, а затем замораживают в жидком азоте. И вуаля — персональный запас «запчастей» для вашего ребенка готов!

Но зачем это нужно, спросите вы? Дело в том, что стволовые клетки уже сейчас успешно применяются для лечения более 80 заболеваний! Это и различные виды лейкемии, и наследственные нарушения иммунитета, и даже некоторые виды рака. А в будущем список может расшириться до сотен и тысяч болезней. Представьте, что вместо пересадки донорского органа вам просто вводят ваши же стволовые клетки, которые сами «знают», как восстановить поврежденную ткань. Звучит как чудо? Но это уже реальность!
Однако не все так радужно в мире банков стволовых клеток. Во-первых, это недешевое удовольствие. Сбор и хранение образца может обойтись в несколько тысяч долларов, плюс ежегодная плата за хранение. Во-вторых, вероятность того, что сохраненные клетки действительно понадобятся, относительно невелика — около 1:2500. Но разве можно измерить деньгами потенциальное спасение жизни?
Еще один спорный момент — это частные versus публичные банки. Частные банки хранят персональные образцы за деньги, в то время как публичные собирают добровольные пожертвования для общего пользования. С одной стороны, личный запас гарантирует 100% совместимость. С другой — шанс найти подходящего донора в публичном банке достаточно высок, а стоимость хранения распределяется на всех.
Но давайте заглянем в будущее! Ученые работают над созданием искусственных стволовых клеток — так называемых индуцированных плюрипотентных стволовых клеток (ИПСК). Представьте, что можно взять обычную клетку кожи и «перепрограммировать» ее, превратив в стволовую! Это открывает совершенно новые горизонты в регенеративной медицине.
А что если пойти еще дальше? Представьте банк стволовых клеток, где хранятся не просто замороженные образцы, а миниатюрные органоиды — крошечные версии наших органов, выращенные из стволовых клеток. Нужна новая печень? Нет проблем — просто достаньте ее «зародыш» из хранилища и дорастите до нужного размера! Звучит как научная фантастика? Но первые шаги в этом направлении уже делаются.
Конечно, на пути к светлому будущу регенеративной медицины еще много препятствий. Как контролировать рост и дифференцировку стволовых клеток? Как избежать образования опухолей? Как сделать лечение доступным для всех, а не только для избранных? Эти вопросы еще предстоит решить ученым.
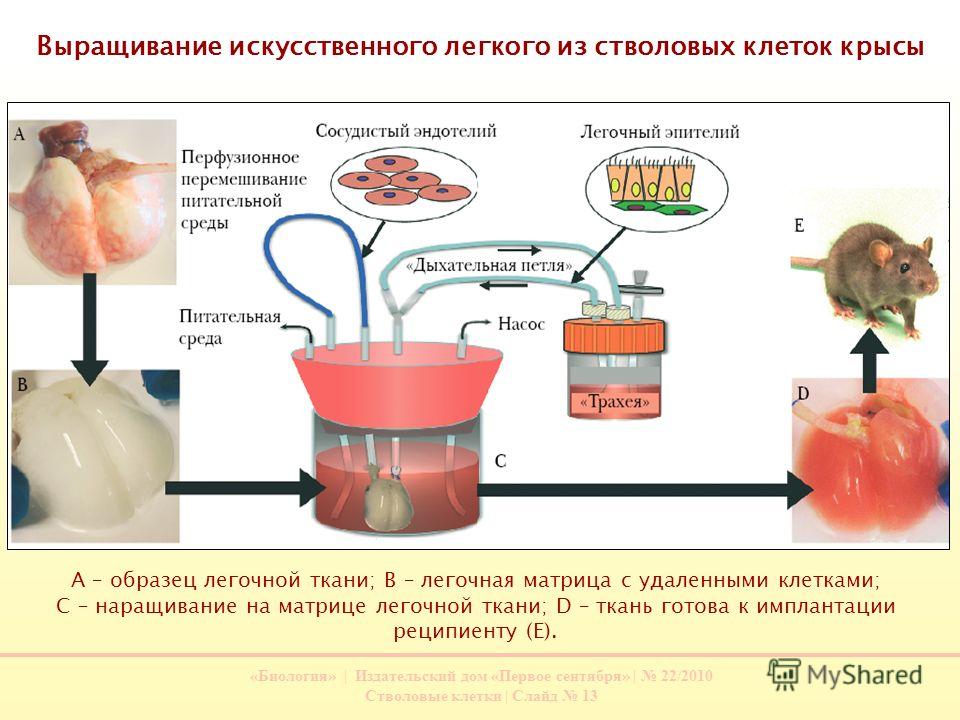
Но одно можно сказать точно — банки стволовых клеток уже сейчас хранят в себе огромный потенциал. Это не просто хранилища биологического материала, это настоящие банки надежды для миллионов людей по всему миру. И кто знает, может быть именно там, в толще жидкого азота, уже хранится ключ к бессмертию человечества?
Криоконсервация: как сохранить жизнь на клеточном уровне
Представьте себе, что вы можете заморозить время. Нет, не как в фантастических фильмах, а на уровне отдельных клеток. Звучит невероятно? А ведь именно это и происходит в банках стволовых клеток благодаря процессу криоконсервации. Это не просто научный термин, а настоящее волшебство, позволяющее сохранить жизнь в состоянии анабиоза на долгие годы.
Но как это работает? Давайте нырнем в мир экстремально низких температур и удивительных технологий. Криоконсервация — это процесс замораживания биологических образцов при сверхнизких температурах, обычно в жидком азоте при -196°C. При такой температуре все биологические процессы в клетках практически останавливаются. Представьте, что вы нажимаете кнопку «пауза» в игре жизни — вот что происходит с клетками при криоконсервации.
Однако все не так просто, как кажется на первый взгляд. Нельзя просто взять и заморозить клетки — вода внутри них превратится в кристаллы льда, которые разорвут клеточные мембраны. Это как пытаться заморозить помидор в морозилке — на выходе получится бесформенная масса. Чтобы избежать этого, ученые разработали специальные криопротекторы — вещества, которые заменяют воду в клетках и не дают образовываться кристаллам льда.
Один из самых популярных криопротекторов — диметилсульфоксид (ДМСО). Это вещество проникает внутрь клеток и защищает их от повреждений при замораживании. Кроме того, используются различные сахара, гликоли и даже антифризные белки, которые некоторые организмы вырабатывают естественным путем. Представьте себе, что вы обволакиваете каждую клетку защитным коконом перед долгим зимним сном — вот что делают криопротекторы.

Но и это еще не все! Процесс замораживания должен быть очень точным и контролируемым. Слишком быстрое охлаждение может привести к образованию микрокристаллов льда внутри клеток, а слишком медленное — к обезвоживанию и повреждению клеточных мембран. Поэтому используются специальные программируемые замораживатели, которые постепенно снижают температуру по заданному алгоритму. Это похоже на то, как опытный пилот плавно сажает самолет — любое резкое движение может привести к катастрофе.
А что происходит после того, как клетки заморожены? Их помещают в специальные криохранилища — огромные термосы с жидким азотом. Здесь они могут храниться десятилетиями без каких-либо изменений. Представьте себе, что вы можете сохранить кусочек своей молодости на долгие годы — именно это и происходит в банках стволовых клеток.
Но вот вопрос — насколько эффективна криоконсервация? Казалось бы, заморозка и разморозка должны сильно повреждать клетки. Однако, благодаря современным технологиям, выживаемость клеток после криоконсервации может достигать 90% и даже выше! Это как если бы вы могли заснуть на 100 лет и проснуться практически без потерь — фантастика, ставшая реальностью.
Интересно, что разные типы клеток по-разному переносят криоконсервацию. Например, сперматозоиды и яйцеклетки относительно легко замораживаются и размораживаются, что открывает огромные возможности в области репродуктивной медицины. А вот с целыми органами дела обстоят сложнее — пока ученым не удалось разработать методы их успешной криоконсервации. Но работа в этом направлении идет полным ходом!
Теперь давайте поговорим о том, как происходит разморозка клеток. Это не менее важный и деликатный процесс, чем замораживание. Клетки нужно разморозить быстро, чтобы избежать образования кристаллов льда, но при этом не допустить теплового шока. Обычно это делается в водяной бане при температуре около 37°C. После разморозки клетки промывают от криопротекторов и постепенно возвращают в нормальную среду. Это похоже на то, как космонавт возвращается на Землю после долгого пребывания в невесомости — нужно время, чтобы адаптироваться.

А знаете ли вы, что криоконсервация используется не только для хранения стволовых клеток? Этот метод применяется в самых разных областях биологии и медицины. Например, с его помощью сохраняют редкие виды растений и животных, создавая своеобразные «ноевы ковчеги» биоразнообразия. В сельском хозяйстве криоконсервация позволяет сохранять генетический материал ценных пород животных и сортов растений. А в медицине, помимо стволовых клеток, замораживают кровь, ткани и даже целые эмбрионы для процедур ЭКО.
Но вернемся к банкам стволовых клеток. Здесь криоконсервация играет ключевую роль, позволяя сохранить эти уникальные клетки в неизменном состоянии на долгие годы. Представьте, что вы можете законсервировать частичку своей молодости, чтобы использовать ее через 10, 20 или даже 50 лет! Это открывает невероятные перспективы в области регенеративной медицины и борьбы со старением.
Однако, как и любая технология, криоконсервация имеет свои ограничения и риски. Например, всегда существует вероятность механической поломки оборудования или человеческой ошибки, что может привести к размораживанию образцов. Кроме того, долгосрочные эффекты криоконсервации на клетки все еще изучаются. Некоторые исследования показывают, что после длительного хранения в замороженном состоянии клетки могут накапливать эпигенетические изменения. Это как если бы вы заснули молодым, а проснулись… не совсем молодым, хотя внешне и не изменились.
Еще один интересный аспект — это этические вопросы, связанные с криоконсервацией. Например, как долго можно хранить замороженные эмбрионы? Кому они принадлежат в случае развода или смерти родителей? Эти вопросы активно обсуждаются в обществе и законодательных органах разных стран.
Несмотря на все сложности, криоконсервация остается одной из самых перспективных технологий в области сохранения биологических материалов. Ученые постоянно работают над улучшением методов заморозки и разморозки, разрабатывают новые криопротекторы и совершенствуют оборудование. Кто знает, может быть в будущем мы сможем замораживать и размораживать целые органы или даже организмы? Пока это кажется фантастикой, но ведь и сама идея криоконсервации когда-то казалась невозможной.
В заключение хочется отметить, что криоконсервация — это не просто научный метод, а настоящий мост между настоящим и будущим. Она позволяет нам сохранить то, что имеет неоценимую ценность — потенциал жизни и здоровья. И кто знает, может быть именно сейчас, в недрах какого-нибудь банка стволовых клеток, в толще жидкого азота, уже хранится ключ к лечению болезней, которые сегодня считаются неизлечимыми. Вот такая она — магия науки, превращающая научную фантастику в реальность.
От пуповинной крови до костного мозга: источники стволовых клеток
Вы когда-нибудь задумывались, откуда берутся эти загадочные стволовые клетки, о которых так много говорят? Может, их выращивают в секретных лабораториях или добывают на далеких планетах? А вот и нет! Источники стволовых клеток гораздо ближе, чем вы можете себе представить. Они буквально окружают нас, скрываясь в самых неожиданных местах нашего организма.
Начнем с самого начала — с момента рождения. Пуповинная кровь — это настоящая сокровищница стволовых клеток. Представьте себе, что каждый раз, когда на свет появляется новый человек, вместе с ним рождается потенциальное лекарство от множества болезней. Звучит как чудо? Но это чистая правда! В пуповинной крови содержатся гемопоэтические стволовые клетки, способные превращаться во все типы клеток крови. Это как если бы у вас был универсальный конструктор для создания новой кровеносной системы.
Но как же получают эту драгоценную жидкость? Процесс на удивление прост и безопасен. После рождения ребенка и перерезания пуповины, кровь из плаценты и остатка пуповины собирают в специальный контейнер. Это занимает всего несколько минут и абсолютно безболезненно как для матери, так и для ребенка. Затем кровь отправляется в банк стволовых клеток, где ее обрабатывают и замораживают для долгосрочного хранения.
А знаете ли вы, что пуповинная кровь — это не единственное, что можно получить при рождении? Сама пуповина и плацента тоже содержат ценные стволовые клетки! В тканях пуповины находятся мезенхимальные стволовые клетки, которые могут превращаться в клетки костей, хрящей и даже сердечной мышцы. Представьте, что вы получаете не просто аптечку первой помощи, а целую передвижную клинику при рождении ребенка!

Но что, если вы уже давно вышли из пеленочного возраста? Не отчаивайтесь! Наш организм — это настоящая фабрика по производству стволовых клеток, работающая круглосуточно. Одним из главных источников стволовых клеток у взрослых является костный мозг. Да-да, та самая субстанция внутри наших костей!
Костный мозг содержит два типа стволовых клеток: гемопоэтические (те же, что и в пуповинной крови) и мезенхимальные. Их добывают путем аспирационной биопсии — процедуры, при которой специальной иглой делают прокол кости (обычно тазовой) и отсасывают небольшое количество костного мозга. Звучит страшновато? На самом деле, процедура проводится под местной анестезией и занимает около 20 минут. Это как будто вы становитесь донором крови, только вместо вены врач обращается к вашим костям.
Но костный мозг — не единственное место, где прячутся стволовые клетки у взрослых. Вы удивитесь, но их можно найти даже в… жировой ткани! Да-да, тот самый жирок, от которого мы так стремимся избавиться, может оказаться настоящим сокровищем для регенеративной медицины. Жировая ткань богата мезенхимальными стволовыми клетками, которые легко извлекаются при липосакции. Представьте себе: вы идете на процедуру похудения, а уходите с запасом «строительного материала» для ваших будущих органов и тканей!
Еще один неожиданный источник стволовых клеток — зубы мудрости. Кто бы мог подумать, что эти часто ненужные и доставляющие неприятности зубы могут быть настолько полезными? В пульпе зубов мудрости содержатся мезенхимальные стволовые клетки, которые можно извлечь при удалении зуба. Это как найти клад в старом сундуке, который вы собирались выбросить!
Но самым богатым источником стволовых клеток остаются эмбрионы на ранних стадиях развития. Эмбриональные стволовые клетки обладают уникальной способностью превращаться в клетки любого типа. Это как если бы у вас был волшебный пластилин, из которого можно слепить любую деталь человеческого организма. Однако использование эмбриональных стволовых клеток сопряжено с серьезными этическими проблемами, поэтому ученые активно ищут альтернативы.

И такая альтернатива была найдена! В 2006 году японский ученый Синъя Яманака совершил настоящий прорыв, открыв способ превращать обычные клетки кожи в так называемые индуцированные плюрипотентные стволовые клетки (ИПСК). За это открытие он получил Нобелевскую премию. Представьте, что вы можете взять обычную клетку своей кожи и «перепрограммировать» ее, превратив в универсальную стволовую клетку. Это как если бы вы могли превратить обычный кирпич в семя, из которого может вырасти целый дом!
Но давайте вернемся к банкам стволовых клеток. Какие же источники они используют чаще всего? На сегодняшний день большинство банков специализируются на хранении стволовых клеток из пуповинной крови и пуповины. Это связано с тем, что их легко и безопасно получить, а также с тем, что эти клетки обладают уникальными свойствами — они «моложе» и потенциально более эффективны, чем стволовые клетки взрослого человека.
Однако многие банки также предлагают услуги по хранению стволовых клеток, полученных из других источников. Например, некоторые клиники предлагают сохранить стволовые клетки из жировой ткани после липосакции или из пульпы зуба после удаления зуба мудрости. Некоторые банки даже работают со стволовыми клетками, полученными из менструальной крови! Кто бы мог подумать, что даже такой, казалось бы, бесполезный материал может стать источником жизни и здоровья?
Но не все так просто в мире стволовых клеток. Каждый источник имеет свои преимущества и недостатки. Например, стволовые клетки из пуповинной крови отлично подходят для лечения заболеваний крови, но их количество ограничено — вы можете получить их только при рождении ребенка. Стволовые клетки из костного мозга более доступны, но их получение связано с болезненной процедурой. ИПСК открывают огромные возможности, но их использование все еще находится на экспериментальной стадии.
Так какой же источник стволовых клеток лучше выбрать? Однозначного ответа на этот вопрос нет. Все зависит от конкретной ситуации, заболевания, которое планируется лечить, и доступных возможностей. Именно поэтому так важна работа банков стволовых клеток — они предоставляют нам выбор и возможность сохранить различные типы стволовых клеток для будущего использования.

В заключение хочется отметить, что мир стволовых клеток — это удивительное место, полное открытий и возможностей. Кто знает, может быть в будущем мы научимся получать стволовые клетки из еще более неожиданных источников? Или создадим искусственные стволовые клетки в лаборатории? Одно можно сказать точно — банки стволовых клеток будут играть ключевую роль в сохранении и использовании этого удивительного ресурса, открывая новые горизонты в лечении болезней и продлении человеческой жизни.
Технологии хранения: обеспечение жизнеспособности биоматериала
Представьте, что у вас есть машина времени, способная заморозить живые клетки и перенести их в будущее без малейших изменений. Звучит как научная фантастика? А вот и нет! Именно этим и занимаются банки стволовых клеток, используя передовые технологии хранения биоматериала. Но как же им удается сохранить эти крошечные фабрики жизни в идеальном состоянии на протяжении десятилетий?
Ключ к успеху — криоконсервация. Это не просто заморозка, а настоящее искусство балансирования на грани между жизнью и смертью клеток. Представьте, что вы пытаетесь заморозить нежный цветок так, чтобы он не потерял ни капли своей красоты и жизненной силы. Вот что такое криоконсервация стволовых клеток!
Но давайте копнем глубже. Какие же технологии используются в банках стволовых клеток для обеспечения жизнеспособности биоматериала? Начнем с самого начала — с момента забора клеток.
Первый этап — это подготовка клеток к заморозке. Здесь в игру вступают криопротекторы — вещества, защищающие клетки от повреждений при замораживании. Самый популярный из них — диметилсульфоксид (ДМСО). Этот химический хамелеон проникает внутрь клеток, замещая воду и предотвращая образование губительных кристаллов льда. Представьте, что вы одеваете каждую клетку в теплую шубу перед долгой зимней спячкой — вот что делают криопротекторы!
Но одного ДМСО недостаточно. В коктейль для криоконсервации добавляют и другие ингредиенты: декстран (для стабилизации клеточных мембран), человеческий сывороточный альбумин (для поддержания осмотического баланса) и даже антиоксиданты. Это как если бы вы не просто одели клетки в шубу, но и снабдили их полным комплектом снаряжения для выживания в экстремальных условиях.

Теперь, когда клетки готовы к путешествию во времени, начинается самое интересное — процесс замораживания. И тут на сцену выходят программируемые замораживатели. Эти высокотехнологичные устройства не просто охлаждают клетки, а делают это по строго заданному алгоритму. Почему это так важно? Дело в том, что слишком быстрое охлаждение может привести к образованию внутриклеточного льда, а слишком медленное — к обезвоживанию клеток. Нужен идеальный баланс!
Типичный протокол замораживания выглядит примерно так: сначала температура снижается со скоростью 1-2°C в минуту до -40°C, затем следует быстрое охлаждение до -80°C, и наконец, образцы погружают в жидкий азот при температуре -196°C. Это как если бы вы сначала медленно погружались в прохладную воду, затем быстро нырнули поглубже, а потом оказались в невесомости космического пространства!
Но на этом приключения наших клеток не заканчиваются. Теперь им предстоит долгое хранение в специальных криохранилищах. Представьте себе огромный термос, наполненный жидким азотом, в котором плавают контейнеры с замороженными клетками. Именно так выглядит современное криохранилище!
Температура в таких хранилищах поддерживается на уровне -196°C. При этой температуре все биологические процессы в клетках практически останавливаются. Это как если бы вы нажали кнопку «пауза» в игре жизни — клетки могут храниться в таком состоянии десятилетиями без каких-либо изменений!
Но как же обеспечивается безопасность хранения? Ведь любой сбой может привести к необратимой потере ценного биоматериала. Тут в дело вступают современные системы мониторинга и контроля. Уровень жидкого азота, температура, влажность — все эти параметры постоянно отслеживаются и регулируются автоматически. Кроме того, многие банки стволовых клеток используют резервные генераторы и дублирующие системы охлаждения на случай аварийных ситуаций. Это как если бы ваш замороженный цветок охраняла целая армия роботов-садовников!
Но вот наступает момент, когда клетки нужно разморозить и использовать. И тут начинается новый этап приключений! Разморозка — это не менее ответственный процесс, чем заморозка. Клетки нужно разморозить быстро, чтобы избежать образования кристаллов льда, но при этом не допустить теплового шока.

Обычно разморозка происходит в водяной бане при температуре 37°C (температура тела человека). Это занимает всего несколько минут. После этого клетки промывают от криопротекторов и постепенно возвращают в нормальную среду. Представьте, что вы пробуждаете спящую красавицу — нужно действовать нежно и осторожно!
Но как же убедиться, что клетки пережили это экстремальное путешествие и все еще жизнеспособны? Тут на помощь приходят различные тесты. Самый простой — это окрашивание трипановым синим. Живые клетки не пропускают этот краситель, а мертвые окрашиваются в синий цвет. Более сложные тесты включают анализ метаболической активности клеток, проверку их способности к делению и дифференцировке.
Интересно, что разные типы клеток по-разному переносят криоконсервацию. Например, гемопоэтические стволовые клетки из пуповинной крови отлично замораживаются и размораживаются, сохраняя до 90% жизнеспособности. А вот с эмбриональными стволовыми клетками дела обстоят сложнее — они более чувствительны к процессу заморозки-разморозки.
Но технологии не стоят на месте! Ученые постоянно работают над улучшением методов криоконсервации. Одно из перспективных направлений — витрификация. Это метод сверхбыстрого охлаждения, при котором вода в клетках переходит в стекловидное состояние, минуя стадию кристаллизации. Представьте, что вместо того, чтобы замораживать воду в лед, вы превращаете ее в стекло! Этот метод особенно эффективен для криоконсервации эмбрионов и яйцеклеток.
Другое интересное направление — использование природных криопротекторов. Некоторые животные, например, лягушки и тихоходки, способны переживать замораживание благодаря особым белкам-антифризам. Ученые пытаются разгадать их секреты и применить эти знания для улучшения технологий криоконсервации стволовых клеток.
А что если заглянуть еще дальше в будущее? Возможно, когда-нибудь мы научимся хранить стволовые клетки при комнатной температуре, используя технологии лиофилизации (сублимационной сушки) или инкапсуляции в специальные полимерные матрицы. Представьте, что вместо огромных криохранилищ банки стволовых клеток превратятся в обычные картотеки с аккуратно разложенными по полочкам сухими порошками или капсулами!
Но пока это все еще фантастика, а реальность такова: современные технологии хранения биоматериала в банках стволовых клеток позволяют сохранять жизнеспособность клеток на протяжении десятилетий. Это открывает невероятные перспективы в области регенеративной медицины и персонализированного лечения. Кто знает, может быть именно сейчас, в недрах какого-нибудь криохранилища, хранится ключ к лечению болезней, которые сегодня считаются неизлечимыми?
В заключение хочется отметить, что технологии хранения стволовых клеток — это не просто научное достижение, а настоящее искусство балансирования на грани возможного. Это как если бы вы пытались сохранить каплю росы на лепестке цветка, перенеся ее через годы и расстояния. И банки стволовых клеток с их передовыми технологиями — это те волшебники, которые делают это возможным, сохраняя для нас частички жизни и надежды на будущее.
Этические вопросы и законодательное регулирование банков стволовых клеток
Банки стволовых клеток — это настоящие хранилища потенциала бессмертия, где в криогенных условиях хранятся крошечные, но невероятно ценные образцы человеческих тканей. Но что же делает их такими особенными? И почему вокруг них столько шума?
Представьте себе миниатюрную фабрику, способную производить любую деталь для человеческого организма. Звучит как научная фантастика, не так ли? Однако именно так можно описать стволовые клетки — универсальные строительные блоки нашего тела. Эти удивительные клетки обладают уникальной способностью превращаться практически в любой тип ткани — от нейронов мозга до клеток сердечной мышцы. Неудивительно, что ученые видят в них ключ к лечению множества заболеваний и травм, которые раньше считались неизлечимыми.
Но откуда же берутся эти чудо-клетки? Основным источником являются пуповинная кровь и ткани новорожденных. В момент рождения ребенка эти ткани богаты юными, полными потенциала стволовыми клетками. Раньше этот бесценный материал просто выбрасывался как медицинские отходы. Теперь же родители могут сохранить его в специализированных банках стволовых клеток, создавая своего рода «биологическую страховку» для своего ребенка и всей семьи.

Процесс сбора и хранения стволовых клеток напоминает сюжет футуристического фильма. После рождения ребенка врачи собирают пуповинную кровь и ткани. Затем образцы проходят тщательную обработку в лаборатории, где из них выделяют драгоценные стволовые клетки. Эти клетки помещают в специальные криоконтейнеры и погружают в жидкий азот при температуре -196°C. В таких экстремальных условиях клетки могут храниться десятилетиями, не теряя своих уникальных свойств.
Но зачем хранить эти клетки? Потенциал их применения поистине огромен. Уже сегодня стволовые клетки используются для лечения некоторых видов рака крови, генетических заболеваний и иммунных расстройств. А в будущем? Регенерация поврежденных органов, восстановление парализованных конечностей, лечение нейродегенеративных заболеваний — все это может стать реальностью благодаря стволовым клеткам.
Этическая дилемма: дар жизни или коммерциализация рождения?
Однако, как и любая передовая технология, банки стволовых клеток сталкиваются с серьезными этическими вызовами. Критики утверждают, что эта практика превращает рождение ребенка в коммерческое предприятие, создавая неравенство в доступе к потенциально жизнесберегающим технологиям. Ведь услуги банков стволовых клеток стоят немалых денег, и далеко не каждая семья может себе это позволить.
С другой стороны, сторонники технологии аргументируют: разве не естественно для родителей желать обеспечить своему ребенку лучшее будущее? И если у них есть возможность сохранить биологический материал, который однажды может спасти жизнь их ребенка или другого члена семьи, почему бы этого не сделать?
Еще один этический вопрос касается использования эмбриональных стволовых клеток. Хотя большинство современных банков работает с клетками из пуповинной крови и тканей, исследования эмбриональных стволовых клеток продолжаются. Это вызывает острые дебаты о статусе эмбриона и границах допустимого в науке.
Законодательный лабиринт: как регулируются банки стволовых клеток?
Учитывая сложность этических вопросов, неудивительно, что законодательное регулирование банков стволовых клеток представляет собой настоящий лабиринт. Разные страны подходят к этому вопросу по-разному. Где-то деятельность таких банков строго регламентирована, а где-то существует в правовом вакууме.

В США, например, банки стволовых клеток подпадают под юрисдикцию Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA). Они должны соответствовать строгим стандартам качества и безопасности. В Европейском Союзе действует специальная директива, регулирующая работу с человеческими тканями и клетками.
В России ситуация несколько сложнее. Хотя деятельность банков стволовых клеток разрешена, специального законодательства в этой области пока нет. Работа таких учреждений регулируется общими нормами медицинского права и рядом подзаконных актов.
Одним из ключевых вопросов законодательного регулирования является вопрос собственности на сохраненные клетки. Кому они принадлежат — ребенку, от которого они были получены, его родителям или банку, который их хранит? Этот вопрос особенно актуален в случае развода родителей или когда ребенок достигает совершеннолетия.
Будущее на перепутье: куда движется индустрия банков стволовых клеток?
Несмотря на этические и правовые сложности, индустрия банков стволовых клеток продолжает активно развиваться. Исследования открывают все новые потенциальные применения стволовых клеток, что увеличивает спрос на услуги по их хранению.
Одним из перспективных направлений является создание общественных банков стволовых клеток. В отличие от частных банков, где хранятся образцы для личного использования, общественные банки собирают донорский материал, доступный для всех нуждающихся. Это может стать решением проблемы неравенства доступа к технологии.
Другой тренд — развитие технологий индуцированных плюрипотентных стволовых клеток (ИПСК). Эта технология позволяет «перепрограммировать» обычные клетки взрослого человека, превращая их в стволовые. Если эта технология станет широко доступной, это может снизить потребность в банках пуповинной крови.
Что же ждет нас в будущем? Возможно, персонализированная регенеративная медицина станет нормой, и у каждого из нас будет свой запас стволовых клеток, готовый к использованию в случае необходимости. Или, может быть, прогресс в области ИПСК сделает хранение биологических образцов ненужным. В любом случае, банки стволовых клеток уже сейчас играют важную роль в развитии медицины будущего, балансируя на грани этики, закона и научного прогресса.

Персонализированная медицина: применение сохраненных стволовых клеток
Представьте себе мир, где каждый человек имеет в своем распоряжении персональный набор «запчастей» для своего организма. Звучит как научная фантастика? А вот и нет! Банки стволовых клеток уже сегодня делают этот сценарий вполне реальным. Но как же работает эта удивительная технология?
Стволовые клетки — это своего рода биологические хамелеоны, способные превращаться практически в любой тип клеток нашего организма. Они могут стать нейронами, кардиомиоцитами, гепатоцитами — да кем угодно! И именно эта их суперспособность делает их настоящим сокровищем для персонализированной медицины.
От пуповины до криохранилища: путешествие стволовых клеток
Но откуда берутся эти чудо-клетки? Самый распространенный источник — пуповинная кровь новорожденных. В момент рождения ребенка эта кровь буквально кишит молодыми, полными потенциала стволовыми клетками. Раньше ее просто выбрасывали, а теперь — собирают и бережно хранят в специальных банках.
Процесс сбора и хранения стволовых клеток напоминает сюжет шпионского триллера. После рождения малыша врачи собирают пуповинную кровь — это нужно сделать быстро и аккуратно, чтобы не потерять ни капли драгоценного материала. Затем образец отправляется в лабораторию, где из него выделяют стволовые клетки. Эти клетки проходят тщательную проверку на жизнеспособность и отсутствие генетических аномалий.
А дальше начинается самое интересное. Клетки помещают в специальные криоконтейнеры и погружают в жидкий азот при температуре -196°C. Это настоящая криогенная капсула, в которой время для клеток словно останавливается. В таких условиях они могут храниться десятилетиями, не теряя своих уникальных свойств.
Персонализированная медицина: когда каждый пациент уникален
Но зачем нужно хранить эти клетки? Ответ прост: они могут спасти жизнь. Уже сегодня стволовые клетки успешно применяются для лечения целого ряда заболеваний. Лейкемия, лимфома, анемия — это лишь некоторые из них. А в будущем список может существенно расшириться.

Представьте, что у вас случился инфаркт. В обычной ситуации это означало бы необратимое повреждение сердечной мышцы. Но если у вас есть сохраненные стволовые клетки, врачи могут использовать их для регенерации поврежденной ткани. Это уже не фантастика — подобные эксперименты успешно проводятся на животных, а первые клинические испытания на людях показывают обнадеживающие результаты.
А как насчет нейродегенеративных заболеваний вроде Паркинсона или Альцгеймера? Стволовые клетки могут стать ключом к их лечению. Ученые работают над методиками, позволяющими превращать стволовые клетки в нейроны и использовать их для восстановления поврежденных участков мозга.
Иммунотерапия: когда твои клетки становятся лекарством
Одно из самых перспективных направлений применения сохраненных стволовых клеток — иммунотерапия рака. Суть метода в том, чтобы «научить» иммунную систему пациента распознавать и уничтожать раковые клетки. И стволовые клетки играют в этом процессе ключевую роль.
Из стволовых клеток можно вырастить Т-лимфоциты — главных «солдат» нашей иммунной системы. Затем эти лимфоциты модифицируют таким образом, чтобы они могли распознавать специфические маркеры на поверхности раковых клеток. После этого «обученные» лимфоциты вводят обратно пациенту, и они начинают охоту на раковые клетки.
Звучит как научная фантастика? А между тем, такие методы уже применяются для лечения некоторых видов лейкемии и лимфом. И результаты порой бывают просто поразительными — у пациентов, которым уже не помогала химиотерапия, опухоли буквально исчезали.
Регенеративная медицина: когда тело чинит само себя
Еще одна захватывающая область применения стволовых клеток — регенеративная медицина. Представьте, что вместо того, чтобы заменять изношенный сустав искусственным протезом, мы могли бы вырастить новый, используя собственные клетки пациента. Это не просто мечта — такие эксперименты уже проводятся.
Например, ученым уже удалось вырастить из стволовых клеток мини-органы, называемые органоидами. Эти крошечные версии печени, почек или даже мозга используются для тестирования лекарств и изучения заболеваний. А в будущем они могут стать основой для выращивания полноценных органов для трансплантации.

Но и это еще не все. Стволовые клетки могут помочь в лечении травм спинного мозга, ожогов, диабета и множества других состояний. Каждый год появляются новые исследования, расширяющие горизонты применения этой технологии.
Этические дилеммы: цена прогресса
Однако, как и любая революционная технология, применение стволовых клеток сталкивается с рядом этических проблем. Одна из них — неравенство доступа. Услуги банков стволовых клеток стоят недешево, и далеко не каждая семья может позволить себе сохранить клетки своего ребенка. Не приведет ли это к тому, что передовые методы лечения будут доступны только богатым?
Другая проблема касается использования эмбриональных стволовых клеток. Хотя большинство современных банков работает с клетками из пуповинной крови, исследования эмбриональных стволовых клеток продолжаются. Это вызывает острые дебаты о статусе эмбриона и границах допустимого в науке.
Есть и вопросы, связанные с долгосрочными последствиями применения стволовых клеток. Мы еще не знаем, как поведут себя трансплантированные клетки через 10, 20 или 50 лет. Не приведет ли их применение к непредвиденным осложнениям?
Будущее персонализированной медицины: что нас ждет?
Несмотря на эти сложности, будущее персонализированной медицины на основе стволовых клеток выглядит многообещающим. Уже сейчас разрабатываются методы, позволяющие получать стволовые клетки не только из пуповинной крови, но и из других тканей взрослого человека. Это может сделать технологию доступной для тех, кто не сохранил клетки при рождении.
Кроме того, прогресс в области генетического редактирования открывает новые возможности. Представьте, что мы можем не просто использовать стволовые клетки для лечения, но и «исправлять» в них генетические дефекты перед трансплантацией. Это может стать революцией в лечении наследственных заболеваний.
А что если в будущем у каждого из нас будет свой персональный банк стволовых клеток? Мы сможем обновлять и «ремонтировать» свой организм по мере необходимости, значительно увеличивая продолжительность и качество жизни. Звучит фантастически? Возможно. Но помните — еще сто лет назад фантастикой считались антибиотики и пересадка органов.

Банки стволовых клеток — это не просто хранилища биологического материала. Это настоящие банки надежды, где хранится потенциал для революции в медицине. И кто знает — может быть, именно там хранится ключ к долголетию и здоровью, о котором человечество мечтало веками?
Будущее банков стволовых клеток: перспективы и инновации в отрасли
Как часто вы задумываетесь о будущем? А о будущем медицины? Банки стволовых клеток — это не просто модный тренд, а настоящий прорыв в области здравоохранения. Но что ждет эту отрасль завтра? Давайте заглянем за горизонт и попробуем представить, какие инновации и перспективы могут изменить ландшафт этой захватывающей индустрии.
Искусственный интеллект на страже здоровья
Представьте себе: ваши стволовые клетки хранятся в банке, а за их состоянием следит не человек, а сверхмощный ИИ. Фантастика? Нет, уже реальность! Искусственный интеллект становится незаменимым помощником в управлении банками стволовых клеток. Он может анализировать огромные массивы данных, предсказывать потенциальные проблемы и даже рекомендовать оптимальные методы лечения на основе генетического профиля пациента.
Но это только начало. В будущем ИИ может научиться «программировать» стволовые клетки, направляя их развитие в нужное русло. Хотите новую печень? Или, может быть, сердце? ИИ сможет подготовить ваши стволовые клетки именно для этой задачи, максимизируя шансы на успешную трансплантацию.
Нанотехнологии: когда размер имеет значение
А теперь давайте уменьшимся до размеров атома. Нанотехнологии — это следующий рубеж в развитии банков стволовых клеток. Представьте себе крошечных роботов, которые могут «ремонтировать» поврежденные стволовые клетки прямо в криохранилище. Или наноустройства, способные доставлять стволовые клетки точно в нужное место в организме, минуя все барьеры.
Звучит как научная фантастика? А между тем, первые шаги в этом направлении уже делаются. Ученые разрабатывают наноматериалы, которые могут служить идеальными «лесами» для роста новых тканей из стволовых клеток. Это может произвести революцию в регенеративной медицине, позволяя выращивать сложные органы с невиданной ранее точностью.

3D-биопечать: когда органы выходят из принтера
Вы когда-нибудь задумывались, как было бы здорово просто «напечатать» новый орган? Технология 3D-биопечати делает это возможным. И стволовые клетки здесь играют главную роль. Представьте себе принтер, который слой за слоем создает живую ткань, используя стволовые клетки в качестве «чернил».
Уже сегодня ученые успешно печатают простые ткани, а в будущем эта технология может позволить создавать сложные органы, идеально подходящие конкретному пациенту. Банки стволовых клеток станут своего рода «библиотеками» биоматериалов для такой печати. Нужна новая кожа после ожога? Или, может быть, часть печени? Просто отправьте запрос в банк стволовых клеток, и ваш персональный орган будет напечатан по требованию.
Генетическое редактирование: исправляем ошибки природы
А что, если мы могли бы не просто хранить стволовые клетки, но и «улучшать» их? Технологии генетического редактирования, такие как CRISPR, открывают захватывающие перспективы. Представьте, что у вас есть генетическое заболевание. В будущем банк стволовых клеток сможет не просто хранить ваши клетки, но и исправить в них генетический дефект перед использованием.
Это может стать настоящим прорывом в лечении наследственных заболеваний. Более того, теоретически мы могли бы «улучшать» стволовые клетки, делая их более устойчивыми к болезням или старению. Конечно, это поднимает серьезные этические вопросы, но потенциал такой технологии трудно переоценить.
Персонализированные органоиды: ваш организм в миниатюре
Слышали ли вы когда-нибудь об органоидах? Это крошечные версии органов, выращенные из стволовых клеток. И они могут стать следующим большим прорывом в персонализированной медицине. Представьте, что у вас есть миниатюрная версия вашей печени или мозга, хранящаяся в банке стволовых клеток.
Зачем это нужно? Во-первых, такие органоиды можно использовать для тестирования лекарств, подбирая идеальную терапию без риска для пациента. Во-вторых, они могут служить «запасными частями» для вашего организма. Нужна трансплантация? Вот вам орган, выращенный из ваших собственных клеток — никакого отторжения, идеальная совместимость.

Криохранение 2.0: новые технологии сохранения
А теперь давайте поговорим о самом процессе хранения стволовых клеток. Сегодня мы используем жидкий азот, но что если есть способ лучше? Ученые работают над новыми методами криоконсервации, которые могут сделать процесс более эффективным и безопасным.
Одна из перспективных технологий — витрификация. Это процесс, при котором клетки превращаются в стекловидное состояние, минуя образование кристаллов льда, которые могут повредить клетки. Другое направление — использование специальных белков, известных как антифризные протеины, которые помогают клеткам лучше переносить заморозку и разморозку.
Мобильные банки: стволовые клетки всегда с вами
А что, если банк стволовых клеток мог бы уместиться у вас в кармане? Звучит невероятно, но технологии движутся именно в этом направлении. Представьте себе устройство размером со смартфон, которое может хранить и даже культивировать ваши стволовые клетки.
Такие портативные банки могли бы произвести революцию в экстренной медицине. Попали в аварию вдали от больницы? Ваши стволовые клетки всегда с вами, готовые помочь в регенерации поврежденных тканей. Или представьте космонавтов на долгой миссии — такое устройство могло бы стать для них настоящим спасением.
Искусственные стволовые клетки: когда природа встречается с технологией
А что, если мы могли бы создавать стволовые клетки «с нуля»? Звучит как научная фантастика, но исследования в этой области уже ведутся. Ученые работают над созданием синтетических стволовых клеток, которые могли бы иметь даже больше возможностей, чем природные.
Представьте себе клетки, которые можно программировать как компьютеры, задавая им конкретные функции. Или клетки, способные адаптироваться к любой ткани в организме. Это могло бы открыть совершенно новые горизонты в регенеративной медицине.
Этические вызовы: где проходит граница?
Конечно, все эти захватывающие перспективы поднимают серьезные этические вопросы. Насколько далеко мы можем зайти в модификации человеческой природы? Кто будет иметь доступ к этим передовым технологиям? Не приведет ли это к еще большему расслоению общества?
Эти вопросы потребуют серьезного обсуждения не только в научном сообществе, но и в обществе в целом. Возможно, нам потребуются новые законы и этические нормы, чтобы регулировать эту быстро развивающуюся отрасль.
Будущее банков стволовых клеток выглядит одновременно захватывающим и пугающим. Мы стоим на пороге новой эры в медицине, где границы между наукой и фантастикой становятся все более размытыми. Готовы ли мы к этому будущему? Время покажет. Но одно можно сказать наверняка: банки стволовых клеток будут играть в нем ключевую роль, храня в себе не просто клетки, а настоящий потенциал бессмертия.
