Содержание
как распознать, причины и лечение
Первый случай проявления болезни, которая еще не имела названия, упоминается в древнеегипетских папирусах в XV-XIV вв. до Р. Х.: брат царицы Нефертити скончался от укуса пчелы. Долгое время болезнь не проявляла себя и считалась редкостью. И только в наше время, с развитием цивилизации, аллергия получила широкое распространение и стала массовой проблемой. В мире аллергические реакции встречаются у 20% людей, 12 % детей страдают аллергическими заболеваниями.
Аллергия у грудничка и какой она бывает
Дети первого года жизни (груднички), как правило, больше всего подвержены пищевой аллергии. Коровье молоко, куриные яйца (желток), рыба и бобовые — это далеко не полный список самых вероятных аллергенов для детей грудного возраста. Этот список можно дополнить так называемыми облигатными аллергенами (наиболее часто вызывающими аллергию): мед, цитрусовые, орехи, шоколад, клубника, фрукты и овощи красного цвета. Хотя в этом случае эти продукты употребляются детьми более старшего возраста, но риск столкнуться с аллергеном велик.
На втором месте — реакции на бытовые аллергены. К ним можно отнести домашнюю и библиотечную пыль, бытовую химию. Средства личной гигиены, подгузники, в том числе, могут при неграмотном применении даже навредить здоровью младенца.
Менее распространены аллергические реакции на цветение, шерсть животных. В этом случае аллергические реакции могут быть вызваны цветением сорных трав, деревьев, при контакте с домашними животными, такими как кошка и собака.
Причины развития аллергии у грудничков
Основными причинами являются:
- Отягощённая наследственность.
- Неправильное питание матери во время беременности и кормления грудью.
- Неблагоприятная экологическая обстановка.
Отягощенная наследственность или наследственная предрасположенность — это наличие аллергических заболеваний у одного или обоих родителей (или его родственников). Ребенок при рождении уже находится в группе риска, и порой хватает одного неверного шага, что бы запустить механизм развития аллергической реакции.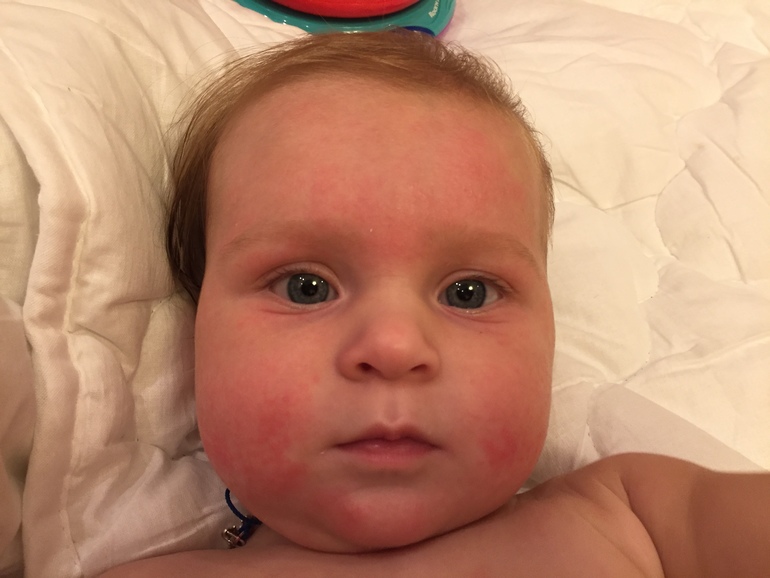
Диета будущей матери — очень важный фактор залога крепкого здоровья ребенка. Даже если у мамы нет аллергии, не стоит злоупотреблять такими продуктами, как цитрусовые, шоколад, кофе, орехи и т. д. Ребенок, еще в утробе матери, может сформировать стойкую аллергическую реакцию на многие продукты. Так же не следует увлекаться декоративной косметикой и красить волосы. Все это можно сказать и о кормящих матерях, когда через грудное молоко все напрямую передается ребенку.
Загазованность современных мегаполисов, огромное количество нитратов в овощах и фруктах, плохое качество воды — это причины, по которым многие дети уже рождаются аллергиками. Все чаще в младенческом возрасте, вследствие аллергической реакции формируется серьезное заболевание, как бронхиальная астма.
Симптомы и как распознать
Симптоматика проявления аллергии у грудничков затрагивает:
- Кожные покровы.
- Слизистые оболочки глаз.
- Органы дыхания.
На кожных покровах, как правило, следует обратить внимание на сухость кожи, шелушение, опрелости, зуд, сыпь и покраснение. Эти симптомы в комплексном проявлении врачи определяют как дерматит. Области его проявления— это кожа щек, плечи, грудная клетка, ягодицы, внешние участки рук и ног. Такие реакции возникают от 3-4 часов до 3 дней. Если не выявить причину и вовремя не начать лечение, увеличивается степень и тяжесть поражения кожных покровов, что может привести к развитию аллергических заболеваний, таких как крапивница, отек Квинке.
Эти симптомы в комплексном проявлении врачи определяют как дерматит. Области его проявления— это кожа щек, плечи, грудная клетка, ягодицы, внешние участки рук и ног. Такие реакции возникают от 3-4 часов до 3 дней. Если не выявить причину и вовремя не начать лечение, увеличивается степень и тяжесть поражения кожных покровов, что может привести к развитию аллергических заболеваний, таких как крапивница, отек Квинке.
Аллергический конъюнктивит — это реакция слизистых оболочек, которая проявляется неприятными ощущениями, обильным слезоотделением, зудом, покраснением и даже гнойными выделениями.
Реакции органов дыхания проявляют себя першением в горле, осиплостью, сухим и долго не прекращающимся подкашливанием. Клиническая картина с такими признаками может быть первым проявлением таких серьезных заболеваний, как аллергический ринит, бронхиальная астма.
Что делать, чем и как лечить
При появлении первых признаков аллергии у ребенка в первую очередь следует обратиться за консультацией к врачу аллергологу.
Медикаментозные препараты от аллергии для грудничков можно разделить на три основные группы:
- Антигистаминные препараты в виде таблеток и капель(зиртек)
- Глазные капли (кромоглин, кромогексал)
- Препараты для наружного применения — мази, гели, крема (бепантен, гистал, фенистил). В редких случаях и по назначению врача используют гормональные препараты (адвантан)
Диагностика и профилактика
Диагностировать аллергию у детей до года можно только по клиническим проявлениям и специфическому анализу венозной крови на иммуноглобулин Е. Кожные пробы делают детям только с трех лет. Когда есть необходимость проведения таких тестов, их ставят на отце или матери ребенка. Но эти исследования проводят только на пищевые аллергены и их точность не всегда оправдывает ожидания по причине того, что на результат накладывается и реакция родителя, на котором проводят исследования.
Кожные пробы делают детям только с трех лет. Когда есть необходимость проведения таких тестов, их ставят на отце или матери ребенка. Но эти исследования проводят только на пищевые аллергены и их точность не всегда оправдывает ожидания по причине того, что на результат накладывается и реакция родителя, на котором проводят исследования.
Профилактические меры в данном случае являются определяющими. Тщательное планирование беременности с изучением аллергических болезней у родителей и ближайших родственников во многом уменьшит риск возникновения аллергии у ребенка.
Питание матери во время кормления грудью должно быть ориентировано на исключение продуктов вызывающих аллергию. Когда ребенок становится чуть старше и ему вводят первый прикорм, необходимо тщательно наблюдать за реакцией организма, чтобы своевременно исключить неподходящие для вашего ребенка продукты. Так же следует воздержаться от употребления экзотических фруктов, более полезны будут фрукты той полосы, где проживает ребенок.
Применение различных средств гигиены, порошков для стирки, подгузников в наше время может не только облегчить жизнь, но и при неправильном применении навредить ребенку, вызвав у него аллергическую реакцию. Чтобы избежать неприятных последствий нужно с осторожностью применять новые средства, вводя их не более одного и наблюдая за ребенком в течение 10-14 дней.
И конечно, не стоит забывать, что при первых признаках и симптомах аллергии у грудничка, необходимо сразу проконсультироваться у врача и не заниматься самолечением.
Проявления пищевой аллергии: оценка и лечение
СКОТТ Х. ЗИХЕРЕР, доктор медициныСемейный врач. 1999;59(2):415-424
См. соответствующий информационный раздаточный материал для пациентов о пищевой аллергии, написанный автором этой статьи.
Термин «пищевая аллергия» относится к неблагоприятным иммунологическим реакциям на пищу. Пищевая аллергия обычно опосредована IgE-антителами, направленными на определенные пищевые белки, но могут играть роль и другие иммунологические механизмы. Основными органами-мишенями пищевых аллергических реакций являются кожа, желудочно-кишечный тракт и дыхательная система. Как острые реакции (крапивница и анафилаксия), так и хронические заболевания (астма, атопический дерматит и желудочно-кишечные расстройства) могут быть вызваны или усугублены пищевой аллергией. Продукты, наиболее часто вызывающие эти реакции у детей, включают молоко, яйца, арахис, сою, пшеницу, лесные орехи, рыбу и моллюсков; у взрослых это арахис, лесные орехи, моллюски и рыба. Диагноз пищевой аллергии требует тщательного поиска возможных причин, подтверждения причины (причин) с помощью поддерживающих тестов, включая специфические тесты на IgE (т.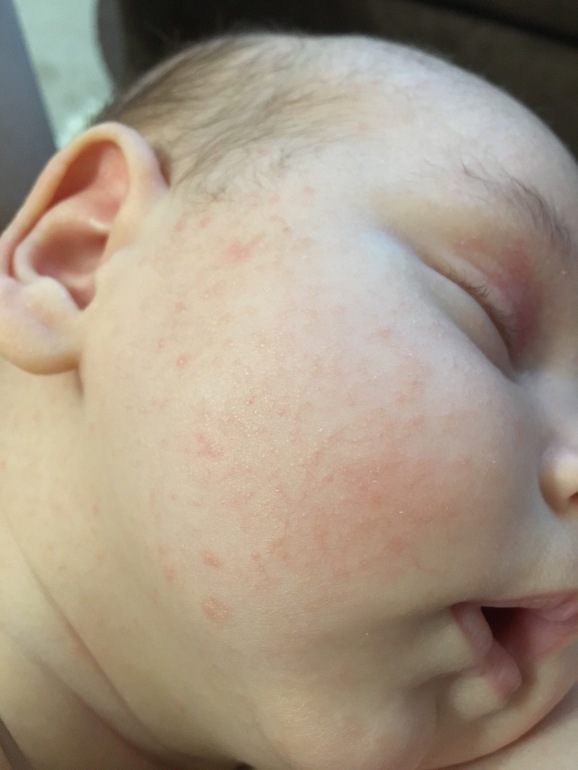
Побочные реакции на пищевые продукты могут быть токсичными или нетоксичными. 1 Токсические реакции не связаны с индивидуальной чувствительностью, но возникают у любого, кто потребляет достаточное количество испорченной пищи. Примеры токсических реакций включают реакции на гистамин при отравлении скумброидной рыбой или на бактериальные токсины при пищевых отравлениях. Напротив, нетоксические побочные реакции на пищу зависят от индивидуальной восприимчивости и либо не являются иммунно-опосредованными, т. е. пищевая непереносимость (Таблица 1) , или иммуноопосредованная, т.е. пищевая аллергия. Данная статья посвящена клиническим проявлениям пищевой аллергии.
| Желудочно-кишечные расстройства |
| Структурные аномалии: грыжа пищеводного отверстия диафрагмы, пилоростеноз, болезнь Гиршпрунга, трахеопищеводный свищ лактаза, сахаразо-изомальтазный комплекс, глюкозо-галактозный комплекс |
| Панкреатическая недостаточность : кистозный фиброз |
| Болезнь желчного пузыря |
| Язвенная болезнь |
| Злокачественные новообразования |
| Нарушения обмена веществ |
| Галактемия |
| 5 |
| Фенилкетонурия |
| Фармакологические состояния |
| Нервозность (кофеин) |
| Зуд (гистамин) |
| Головная боль (тирамин) |
| Дезориентация (алкоголь) |
| Психологические расстройства |
| Неврологические расстройства |
| Вкусовой ринит |
| Аурикулотемпоральный синдром 099 |
Аллергические реакции
Аллергические реакции на пищевые продукты являются либо IgE-опосредованными, либо не IgE-опосредованными (Таблица 2) . Роль IgE-опосредованных реакций при пищевой аллергии хорошо известна. Лица, генетически предрасположенные к атопии, вырабатывают специфические антитела IgE к определенным белкам, воздействию которых они подвергаются. 2 Эти антитела связываются с тучными клетками и другими клетками в тканях организма, а также с базофилами, циркулирующими в кровотоке. Когда пищевой белок попадает в организм, IgE распознает его на поверхности этих клеток; высвобождаются медиаторы (например, гистамин), и появляются симптомы. Симптомы IgE-опосредованных реакций обычно поражают кожу, дыхательную систему и желудочно-кишечный тракт. 3 Патогенез не-IgE-опосредованных реакций при пищевой аллергии не так четко определен, но Т-клетки и макрофаги, скорее всего, играют определенную роль. Заболевания, вызванные этими не-IgE-опосредованными иммунологическими реакциями на пищу, поражают те же системы органов, что и IgE-опосредованные формы.
Роль IgE-опосредованных реакций при пищевой аллергии хорошо известна. Лица, генетически предрасположенные к атопии, вырабатывают специфические антитела IgE к определенным белкам, воздействию которых они подвергаются. 2 Эти антитела связываются с тучными клетками и другими клетками в тканях организма, а также с базофилами, циркулирующими в кровотоке. Когда пищевой белок попадает в организм, IgE распознает его на поверхности этих клеток; высвобождаются медиаторы (например, гистамин), и появляются симптомы. Симптомы IgE-опосредованных реакций обычно поражают кожу, дыхательную систему и желудочно-кишечный тракт. 3 Патогенез не-IgE-опосредованных реакций при пищевой аллергии не так четко определен, но Т-клетки и макрофаги, скорее всего, играют определенную роль. Заболевания, вызванные этими не-IgE-опосредованными иммунологическими реакциями на пищу, поражают те же системы органов, что и IgE-опосредованные формы.
| Орган-мишень | IgE-опосредованное заболевание | Не-IgE-опосредованное заболевание | Кожа | Крапивница и ангионевротический отек | Атопический дерматит |
|---|---|---|---|---|---|
| Атопический дерматит | Герпетиформный дерматит | ||||
| Желудочно-кишечный тракт | Синдром оральной аллергии | Проктоколит | |||
| Желудочно-кишечная «анафилаксия» | Энтероколит | ||||
| Аллергический эозинофильный гастроэнтерит | Аллергический эозинофильный гастроэнтерит | ||||
| Целиакия | |||||
| Дыхательные пути | Астма | Синдром Хайнера | |||
| Аллергический ринит | |||||
| Мультисистемный | Пищевая анафилаксия | ||||
| Пищевая анафилаксия, вызванная физической нагрузкой |
URTICARIA
Кожа является распространенным органом-мишенью для аллергических реакций на пищу. Острая крапивница характеризуется зудящими, преходящими, эритематозными возвышающимися поражениями, иногда сопровождающимися локализованным отеком (ангионевротический отек). Пищевая аллергия составляет до 20 процентов случаев острой крапивницы 4 и опосредуется IgE, специфичным к пищевому белку. Поражения обычно возникают в течение одного часа после приема пищи или контакта с ней. Поскольку только 1,4% случаев хронической или персистирующей крапивницы (т. е. продолжительностью более шести недель) вызваны пищевой аллергией, 5 поиск возбудителя при начальной оценке этого состояния обычно не требуется.
Острая крапивница характеризуется зудящими, преходящими, эритематозными возвышающимися поражениями, иногда сопровождающимися локализованным отеком (ангионевротический отек). Пищевая аллергия составляет до 20 процентов случаев острой крапивницы 4 и опосредуется IgE, специфичным к пищевому белку. Поражения обычно возникают в течение одного часа после приема пищи или контакта с ней. Поскольку только 1,4% случаев хронической или персистирующей крапивницы (т. е. продолжительностью более шести недель) вызваны пищевой аллергией, 5 поиск возбудителя при начальной оценке этого состояния обычно не требуется.
АТОПИЧЕСКИЙ ДЕРМАТИТ
Атопический дерматит обычно начинается в раннем детстве и характеризуется типичным распространением (лицо, волосистая часть головы и конечности), сильным зудом и хроническим рецидивирующим течением. Это воспалительное состояние кожи часто связано с аллергическими заболеваниями (например, астмой и аллергическим ринитом) и с семейным анамнезом аллергии. 6 Имеющиеся данные свидетельствуют о том, что IgE-опосредованная пищевая аллергия играет патогенную роль в развитии атопического дерматита, особенно у детей, 6 , хотя пищевая аллергия, не опосредованная IgE, также имеет значение. 7 Клинические исследования с использованием двойных слепых плацебо-контролируемых пищевых проб показали, что 37 процентов детей с умеренным атопическим дерматитом имеют пищевую аллергию. 8 Напротив, от 6 до 8 процентов младенцев и детей в общей популяции страдают аллергией на тот или иной вид пищи. 9
6 Имеющиеся данные свидетельствуют о том, что IgE-опосредованная пищевая аллергия играет патогенную роль в развитии атопического дерматита, особенно у детей, 6 , хотя пищевая аллергия, не опосредованная IgE, также имеет значение. 7 Клинические исследования с использованием двойных слепых плацебо-контролируемых пищевых проб показали, что 37 процентов детей с умеренным атопическим дерматитом имеют пищевую аллергию. 8 Напротив, от 6 до 8 процентов младенцев и детей в общей популяции страдают аллергией на тот или иной вид пищи. 9
ГЕРПЕТИФОРМНЫЙ ДЕРМАТИТ
Герпетиформный дерматит представляет собой хроническое папуло-везикулярное заболевание кожи, при котором поражения распространяются на разгибательные поверхности локтей, коленей и ягодиц. 10 Заболевание связано со специфической не-IgE-опосредованной иммунной чувствительностью к глютену (белку, содержащемуся в пшенице, ячмене, овсе и ржи). Хотя герпетиформный дерматит связан с глютеновой болезнью, у пациентов часто не возникает сопутствующих желудочно-кишечных заболеваний.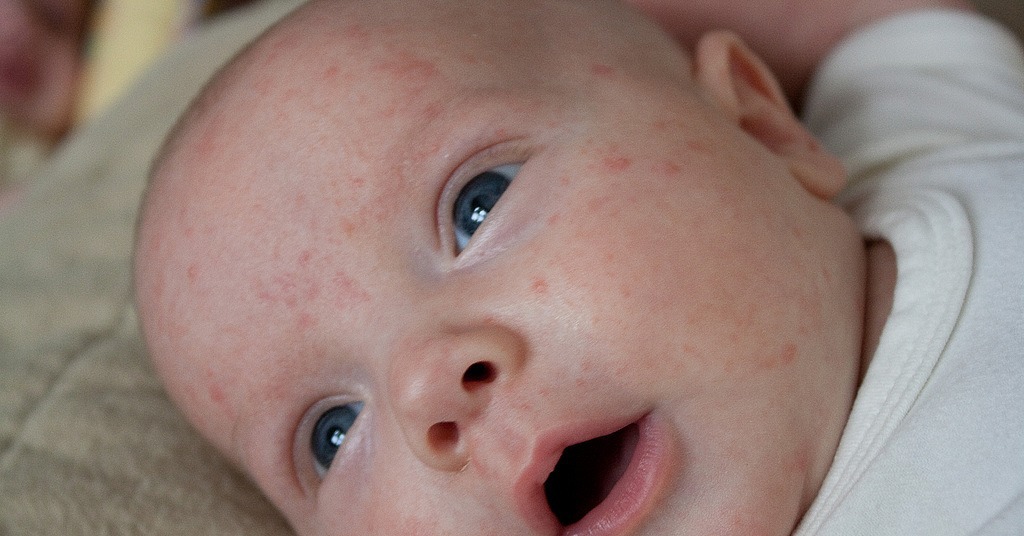 Сыпь проходит при устранении глютена из рациона.
Сыпь проходит при устранении глютена из рациона.
Желудочно-кишечный тракт
Желудочно-кишечный тракт является еще одним распространенным органом-мишенью для IgE-опосредованных реакций на пищевые продукты. Симптомы желудочно-кишечной «анафилаксии» возникают вскоре после приема пищи и включают тошноту, рвоту, боль в животе и диарею.
СИНДРОМ ОРАЛЬНОЙ АЛЛЕРГИИ
Синдром оральной аллергии характеризуется зудом и отеком слизистой оболочки полости рта, возникающими после употребления некоторых свежих фруктов и овощей. 11 Симптомы редко выходят за пределы рта. Реакция возникает в первую очередь у пациентов с аллергической чувствительностью к пыльце и вызывается антителами IgE, направленными на перекрестно реагирующие белки, обнаруженные в пыльце, фруктах и овощах. 11 У пациентов с поллинозом, вызванным пыльцой березы, могут быть симптомы синдрома оральной аллергии после употребления фундука, яблока, моркови и сельдерея, тогда как у пациентов с чувствительностью IgE к пыльце амброзии могут возникнуть реакции на дыни (например, арбуз или дыню) и бананы . Интересно, что пациенты обычно могут принимать приготовленные формы пищи без каких-либо симптомов, потому что ответственные аллергены разрушаются в процессе нагревания. Крайне важно дифференцировать симптомы синдрома оральной аллергии от ранних симптомов системной реакции на пищу.
Интересно, что пациенты обычно могут принимать приготовленные формы пищи без каких-либо симптомов, потому что ответственные аллергены разрушаются в процессе нагревания. Крайне важно дифференцировать симптомы синдрома оральной аллергии от ранних симптомов системной реакции на пищу.
ЦЕЛИАКИЯ
Ряд иммунологических реакций на пищевые белки не опосредуются IgE. Целиакия проявляется в течение нескольких месяцев стеатореей, метеоризмом и потерей веса. Гиперчувствительность к глютену вызывает заболевание, а характерным диагностическим признаком является обширное уплощение ворсинок в биоптате, взятом из слизистой оболочки тощей кишки.
АЛЛЕРГИЧЕСКИЙ ЭОЗИНОФИЛЬНЫЙ ГАСТРОЭНТЕРИТ
Хотя аллергический эозинофильный гастроэнтерит у некоторых пациентов является IgE-опосредованным заболеванием, примерно у половины пациентов не обнаруживаются специфические IgE-антитела к пищевым продуктам. У больных с аллергическим эозинофильным гастроэнтеритом отмечается выраженный рефлюкс, постпрандиальная боль в животе, рвота, раннее чувство насыщения и диарея. Диагноз предполагается при наличии воспаления и значительной эозинофильной инфильтрации пищевода, желудка или тонкой кишки. Лечение строгой избегающей диетой с использованием элементарной формулы эффективно у некоторых пациентов. 12
Диагноз предполагается при наличии воспаления и значительной эозинофильной инфильтрации пищевода, желудка или тонкой кишки. Лечение строгой избегающей диетой с использованием элементарной формулы эффективно у некоторых пациентов. 12
ДЕТСКИЙ ПРОКТОКОЛИТ
Симптомы детского проктоколита ограничены нижними отделами желудочно-кишечного тракта и носят кратковременный характер. Прием ответственной пищи (обычно белка коровьего молока или грудного молока матерей, употребляющих коровье молоко) провоцирует диарею с примесью крови в стуле, но редко возникает анемия.
ЭНТЕРОКОЛИТ И ЭНТЕРОПАТИЯ, ИНДУЦИРОВАННЫЕ ПИЩЕВЫМИ БЕЛКАМИ
Пациенты с энтероколитом, вызванным пищевыми белками, часто диагностируются в младенчестве и проявляются обильной рвотой и диареей. В тяжелых случаях эти симптомы могут привести к вялости, обезвоживанию и гипотензии (часто имитирующей бактериальный сепсис). Симптомы могут осложняться ацидозом. Энтероколит разрешается с элиминацией ответственного белка, чаще всего коровьего молока или сои.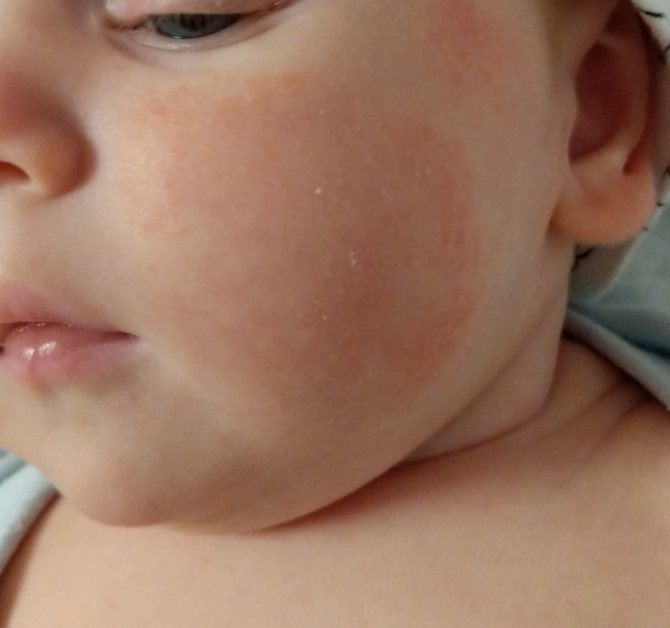 13,14
13,14
Пациенты могут также иметь менее выраженные желудочно-кишечные симптомы, вызванные пищевым белком, которые вызываются молоком, соей, яйцами, пшеницей, рисом, курицей или рыбой. Эти пациенты, классифицированные как страдающие энтеропатией, вызванной пищевыми белками, обычно не страдают колитом, и у них реже возникает рвота (30%), чем у пациентов с энтероколитом (90%). 15
Роль IgE-опосредованной или не-IgE-опосредованной чувствительности к пищевым белкам в случаях детской колики 16 и воспалительное заболевание кишечника 17 остается спорным. Хотя задержка развития у младенцев может быть связана с нарушением всасывания в результате пищевой аллергии, ограничительная диета, навязанная семьей, также может привести к плохому росту. Эта искусственная пищевая аллергия была диагностирована у 5 процентов детей с задержкой развития, которые были направлены на академическую программу лечения аллергии. 18
Дыхательные пути
РИНИТ
Верхние дыхательные пути могут быть мишенью IgE-опосредованной пищевой аллергии. Симптомы могут включать заложенность носа, ринорею, чихание и зуд. Распространенность пищевого аллергического ринита, даже среди пациентов, направленных в аллергологические клиники, по-видимому, составляет менее 1 процента, хотя от 25 до 80 процентов пациентов с документально подтвержденной IgE-опосредованной пищевой аллергией имеют назальные симптомы во время пероральной пищевой провокации. 19
Симптомы могут включать заложенность носа, ринорею, чихание и зуд. Распространенность пищевого аллергического ринита, даже среди пациентов, направленных в аллергологические клиники, по-видимому, составляет менее 1 процента, хотя от 25 до 80 процентов пациентов с документально подтвержденной IgE-опосредованной пищевой аллергией имеют назальные симптомы во время пероральной пищевой провокации. 19
Вкусовой ринит – это ринорея, вызванная острой пищей. Это не иммунологическая реакция; это опосредовано неврологическими механизмами. 20
АСТМА
Пищевая астма — это IgE-опосредованное заболевание, которое может возникнуть в результате приема пищи, вызывающей заболевание, или вдыхания паров, выделяющихся во время приготовления пищи или в производственных условиях. Распространенность пищевой астмы среди населения в целом неизвестна, но было обнаружено, что это заболевание встречается у 5,7% детей с астмой, 11% детей с атопическим дерматитом и 24% детей с пищевыми хрипами в анамнезе. . 21 Распространенность хрипов, вызванных приемом пищи, у взрослых с астмой составляет менее 2 процентов. 22
. 21 Распространенность хрипов, вызванных приемом пищи, у взрослых с астмой составляет менее 2 процентов. 22
СИНДРОМ ХЕЙНЕРА
Примером не-IgE-опосредованной неблагоприятной легочной реакции на пищу является синдром Хайнера. Этот необычный детский синдром характеризуется иммунной реакцией на белки коровьего молока с преципитацией антител (IgG) к белкам коровьего молока, что приводит к легочным инфильтратам, легочному гемосидерозу, анемии, рецидивирующей пневмонии и задержке развития.
Анафилаксия
Анафилаксия относится к тяжелой полиорганной реакции, связанной с IgE-опосредованной гиперчувствительностью. Смертельная пищевая анафилаксия, по-видимому, чаще встречается у пациентов с фоновой астмой. 23 Пациенты, перенесшие смертельную или почти смертельную анафилаксию, вызванную пищевыми продуктами, не знали, что они проглотили инкриминируемую пищу, у них были почти немедленные симптомы и отсрочено получение адреналиновой терапии. Примерно у половины пациентов период покоя предшествовал дыхательной декомпенсации. Пищевые продукты, наиболее часто вызывающие пищевую анафилаксию, — это арахис, лесные орехи (грецкий орех, миндаль, пекан, кешью, фундук, бразильский орех и т. д.) и моллюски. 23
Примерно у половины пациентов период покоя предшествовал дыхательной декомпенсации. Пищевые продукты, наиболее часто вызывающие пищевую анафилаксию, — это арахис, лесные орехи (грецкий орех, миндаль, пекан, кешью, фундук, бразильский орех и т. д.) и моллюски. 23
Пищевая анафилаксия, вызванная физической нагрузкой, бывает двух форм. 24 Анафилаксия может развиться, когда физические упражнения следуют за приемом определенной пищи, к которой обычно проявляется IgE-опосредованная чувствительность (например, сельдерей), или, что реже, может возникнуть после приема любой пищи. Употребление инкриминируемой пищи во время упражнений или упражнений без приема пищи не приводит к появлению симптомов.
Споры и пищевая аллергия
Связь пищевой аллергии с рядом клинических проявлений остается спорной. Пищевая аллергия может играть роль у меньшинства пациентов с мигренью, 25 , хотя чаще всего причиной является фармакологическая активность химических веществ, содержащихся в некоторых пищевых продуктах (например, тирамин в сырах).
Роль пищевой аллергии в расстройствах поведения у детей также неоднозначна. Пищевые красители могут воздействовать на небольшую группу детей с расстройствами поведения, но нет убедительных доказательств того, что пищевая аллергия играет непосредственную роль в этих расстройствах. 26 К сожалению, недостоверная информация в непрофессиональной прессе и использование нетрадиционных и непроверенных методов, таких как «провокация-нейтрализация», 27 для диагностики и лечения расстройств поведения может отвлечь семью пациента от более полезных методов лечения. С другой стороны, у детей с поведенческими расстройствами, которые также имеют истинную аллергию, следует проводить лечение для облегчения симптомов астмы, атопического дерматита и сенной лихорадки.
Диагностика
ПЕРВОНАЧАЛЬНАЯ ОЦЕНКА
Обследование необходимо у пациентов с общими клиническими проявлениями пищевой аллергии. Первоначальная оценка, начинающаяся с тщательного сбора анамнеза и физического осмотра, должна учитывать широкий дифференциальный диагноз, включая метаболические нарушения, анатомические аномалии, злокачественные новообразования, недостаточность поджелудочной железы, неиммунологические побочные реакции на пищевые продукты и многие другие расстройства, которые могут привести к сходным симптомам. Также следует учитывать аллергические реакции на вещества, не являющиеся пищевыми (например, на перхоть животных, плесень, пыль). Как только пищевая аллергия определена как вероятная причина симптомов, можно приступить к подтверждению диагноза и идентификации причастных продуктов.
Также следует учитывать аллергические реакции на вещества, не являющиеся пищевыми (например, на перхоть животных, плесень, пыль). Как только пищевая аллергия определена как вероятная причина симптомов, можно приступить к подтверждению диагноза и идентификации причастных продуктов.
У пациентов с острыми реакциями, такими как острая крапивница или анафилаксия, анамнез может явно указывать на конкретную пищу. У пациентов с хроническими заболеваниями, такими как атопический дерматит или астма, труднее точно определить причину заболевания. Практически любой пищевой белок может вызвать реакцию; тем не менее, лишь на небольшое количество продуктов питания приходится более 90 процентов неблагоприятных пищевых реакций, и большинство пациентов чувствительны менее чем к трем продуктам. 3,28 Наиболее распространенными продуктами, вызывающими реакции у детей, являются яйца, молоко, арахис, соя, пшеница, лесные орехи и рыба. 3,28 Взрослые чаще всего реагируют на арахис, лесные орехи, рыбу и моллюсков..jpg) 29
29
КОЖНАЯ ПРОВЕРКА ПУНКЦИЕЙ
При оценке IgE-опосредованной пищевой аллергии специальные тесты могут помочь выявить или исключить ответственные продукты. Одним из методов определения наличия специфических IgE-антител является кожная проба с уколом. Пока пациент не принимает антигистаминные препараты, для прокола кожи через глицеринированный экстракт пищи, а также через соответствующие положительные (гистамин) и отрицательные (солевой раствор-глицерин) контрольные вещества используется устройство, такое как раздвоенная игла или ланцет. Местная реакция в виде волдырей и воспалений указывает на присутствие специфических пищевых IgE-антител, а диаметр волдырей более 3 мм указывает на положительный ответ.
Прик-тесты наиболее ценны, когда они отрицательны, потому что отрицательная прогностическая ценность этих тестов очень высока (более 95 процентов). 30,31 К сожалению, положительная прогностическая ценность составляет порядка 50 процентов.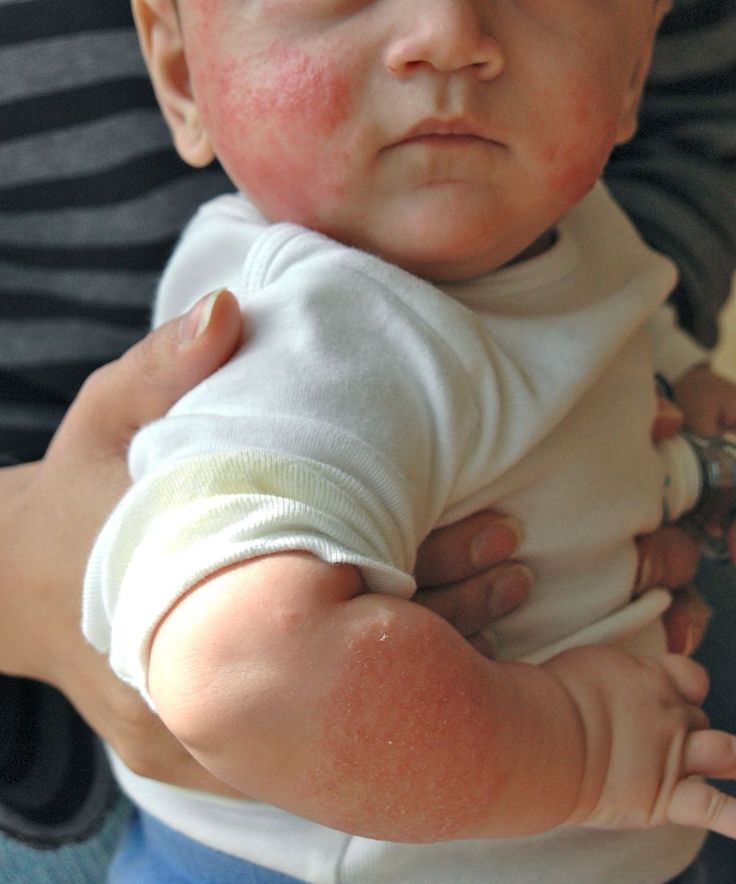 30,31 Таким образом, положительный кожный тест сам по себе не может считаться доказательством клинически значимой гиперчувствительности, в то время как отрицательный тест фактически исключает IgE-опосредованную пищевую аллергию на рассматриваемый продукт.
30,31 Таким образом, положительный кожный тест сам по себе не может считаться доказательством клинически значимой гиперчувствительности, в то время как отрицательный тест фактически исключает IgE-опосредованную пищевую аллергию на рассматриваемый продукт.
Внутрикожные кожные тесты на аллергию с пищевыми экстрактами дают неприемлемо высокий уровень ложноположительных результатов и поэтому не должны использоваться. 31 Белок в коммерческих экстрактах некоторых фруктов и овощей подвержен деградации, поэтому свежие экстракты этих продуктов более надежны. 32
ТЕСТИРОВАНИЕ IN VITRO (RAST)
Тесты in vitro на специфические IgE (радиоаллерго-госорбентные тесты [RAST]) более практичны, чем прик-тесты для скрининга пищевой аллергии в учреждениях первичной медико-санитарной помощи. Как и в случае с кожными пробами, отрицательный результат RAST-теста очень надежен для исключения IgE-опосредованной реакции на конкретный продукт, но положительный результат имеет низкую положительную прогностическую ценность. Тесты in vitro на IgE обычно менее чувствительны, чем кожные тесты; однако при использовании высокочувствительных анализов уровни специфических для пищевых продуктов IgE-антител коррелируют с клинической реактивностью к определенным пищевым продуктам (например, к молоку, яйцам, арахису, рыбе). 33 Поскольку большинство пациентов с пищевой аллергией чувствительны только к нескольким продуктам 3,28 и небольшое количество продуктов вызывает большинство реакций, 3,28 обычно нецелесообразно проводить тесты на аллергию на большое количество продуктов продуктов. В контексте подробного анамнеза выборочное тестирование с большей вероятностью выявит причинную пищу. Измерение антител иммуноглобулина G4 (IgG4), провокации-нейтрализации, цитотоксичности, прикладной кинезиологии и других недоказанных методов бесполезны. 34
Тесты in vitro на IgE обычно менее чувствительны, чем кожные тесты; однако при использовании высокочувствительных анализов уровни специфических для пищевых продуктов IgE-антител коррелируют с клинической реактивностью к определенным пищевым продуктам (например, к молоку, яйцам, арахису, рыбе). 33 Поскольку большинство пациентов с пищевой аллергией чувствительны только к нескольким продуктам 3,28 и небольшое количество продуктов вызывает большинство реакций, 3,28 обычно нецелесообразно проводить тесты на аллергию на большое количество продуктов продуктов. В контексте подробного анамнеза выборочное тестирование с большей вероятностью выявит причинную пищу. Измерение антител иммуноглобулина G4 (IgG4), провокации-нейтрализации, цитотоксичности, прикладной кинезиологии и других недоказанных методов бесполезны. 34
Если у пациента в анамнезе есть подозрения на заболевания, связанные с пищевыми продуктами, и тесты на IgE-антитела к пищевым продуктам положительны, в первую очередь следует исключить этот продукт из рациона. Дальнейшее тестирование обычно не требуется у пациентов с тяжелыми острыми реакциями. Однако, если симптомы носят хронический характер (атопический дерматит, астма) и/или причастны многие пищевые продукты, может потребоваться диагностическая пищевая провокация.
Дальнейшее тестирование обычно не требуется у пациентов с тяжелыми острыми реакциями. Однако, если симптомы носят хронический характер (атопический дерматит, астма) и/или причастны многие пищевые продукты, может потребоваться диагностическая пищевая провокация.
Пищевая провокация через рот
Двойная слепая плацебо-контролируемая пищевая провокация считается золотым стандартом диагностики пищевой аллергии. 3,30,35 Процедура трудоемкая, но ее можно модифицировать для работы в офисе. 35 Пациенты воздерживаются от подозреваемых пищевых продуктов в течение как минимум двух недель, антигистаминная терапия прекращается в соответствии с периодом полувыведения конкретного лекарства, а дозы лекарств от астмы снижаются, насколько это возможно. После получения внутривенного доступа вводят градуированные дозы либо контрольного пищевого продукта, либо плацебо. Еда спрятана либо в другую еду, либо в непрозрачные капсулы.
Требуется медицинское наблюдение и немедленный доступ к лекарствам для неотложной помощи, включая адреналин, антигистаминные препараты, стероиды и ингаляционные бета-агонисты, а также оборудование для сердечно-легочной реанимации, поскольку реакции могут быть тяжелыми.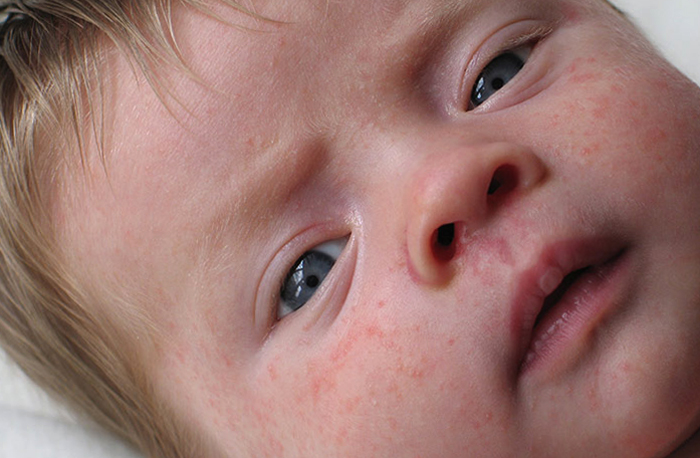 Во время провокации у пациентов часто оценивают изменения кожи, желудочно-кишечного тракта и дыхательной системы. Проблемы прекращаются, когда реакция становится очевидной, и при необходимости назначаются экстренные лекарства. Пациентов также наблюдают на предмет отсроченных реакций. Если подозревается аллергия только на некоторые продукты, для скрининга реактивности можно использовать одиночное слепое или открытое тестирование.
Во время провокации у пациентов часто оценивают изменения кожи, желудочно-кишечного тракта и дыхательной системы. Проблемы прекращаются, когда реакция становится очевидной, и при необходимости назначаются экстренные лекарства. Пациентов также наблюдают на предмет отсроченных реакций. Если подозревается аллергия только на некоторые продукты, для скрининга реактивности можно использовать одиночное слепое или открытое тестирование.
Отрицательные заражения всегда подтверждаются открытым кормлением большей порцией корма размером с еду. Оральные провокации обычно не следует проводить у пациентов с отчетливой реактивностью или тяжелой реакцией в анамнезе. Общий подход к диагностике пищевой аллергии показан в Таблице 3 .
| I. Соберите подробный анамнез и проведите полное физикальное обследование | |||||
| A. Сформулируйте подозрение на пищевую аллергию на основании анамнеза и физикальных данных | |||||
B. Исключить другие причины симптомов Исключить другие причины симптомов | |||||
| II. Оценить IgE-опосредованную пищевую аллергию с помощью кожно-пункционных проб или радиоаллергосорбентных тестов | |||||
| A. Тест отрицательный | |||||
| 410 2. Если пациент имеет в анамнезе значительную реакцию или подозревается не-IgE-опосредованная реакция, повторно введите пищу в рацион под наблюдением врача или в условиях контрольного заражения | |||||
| B. Тесты положительные | |||||
| 1. Исключить пищу | |||||
| 25 | |||||
| а. Если контрольный тест отрицательный, повторно введите корм | |||||
b. Если провокационный тест положительный, вызовите Если провокационный тест положительный, вызовите | |||||
| (1) Исключите продукты (если только несколько продуктов) | |||||
| (2) Если речь идет о нескольких продуктах, рассмотрите возможность двойной слепой плацебо-контролируемой пищевой провокации | |||||
| (a) Если контрольный тест положительный, исключить корм | |||||
| (b) Если контрольный тест отрицательный, повторно ввести корм | |||||
| III. Диагноз установлен | |||||
| A. Проинформируйте пациента о лечении и избегании | |||||
B. Повторно оценивайте через соответствующие промежутки времени, если есть вероятность переносимости Повторно оценивайте через соответствующие промежутки времени, если есть вероятность переносимости | |||||
ПРОБЛЕМЫ ПРИ НЕ-ИГЕ-ОППОСРЕДОВАННОЙ АЛЛЕРГИИ
Более трудно диагностировать не-IgE-опосредованные реакции (например, аллергический эозинофильный гастроэнтерит, энтероколит) и точно определить специфические продукты питания, поскольку для выявления этих заболеваний не используются специфические лабораторные тесты. В некоторых ситуациях (например, при аллергическом эозинофильном гастроэнтерите) для установления диагноза может потребоваться биопсия. Элиминационные диеты с постепенным повторным введением продуктов и контролируемым пероральным приемом пищи часто необходимы для выявления причинных продуктов. Необходимо соблюдать осторожность, поскольку симптомы, например, синдрома энтероколита, могут быть тяжелыми и даже привести к шоку. 13
Еще одна диагностическая трудность возникает, когда пищевые добавки (красители, ароматизаторы и консерванты) участвуют в реакциях. Документально подтверждено, что некоторые добавки вызывают те же типы реакций, что и IgE-опосредованные реакции (например, астму, крапивницу, атопический дерматит), но с гораздо меньшей распространенностью. 36,37 Поскольку эти реакции, как правило, не опосредованы IgE, для диагностики требуются пробы на элиминацию пищи и пероральные провокационные тесты.
Документально подтверждено, что некоторые добавки вызывают те же типы реакций, что и IgE-опосредованные реакции (например, астму, крапивницу, атопический дерматит), но с гораздо меньшей распространенностью. 36,37 Поскольку эти реакции, как правило, не опосредованы IgE, для диагностики требуются пробы на элиминацию пищи и пероральные провокационные тесты.
Лечение
В дополнение к медикаментозному лечению проявлений пищевой аллергии (например, местная терапия атопического дерматита, ингаляционное лечение астмы) пищевая аллергия лечится путем исключения из диеты вызывающего(их) продукта(ов). Иммунотерапия («прививки от аллергии») оказалась непрактичной, 38 , за исключением случаев, когда пыльца вызывает симптомы синдрома оральной аллергии. 39
Устранение пищевых белков является трудной задачей. Например, при безмолочной диете пациенты должны быть проинструктированы не только избегать всех очевидных молочных продуктов, но и читать этикетки пищевых продуктов на наличие ключевых слов, которые могут указывать на присутствие белка коровьего молока, включая «казеин», « сыворотка», «лактальбумин», «карамельный краситель» и «нуга». Когда используются расплывчатые термины, такие как «ароматизатор с высоким содержанием белка» или «натуральные ароматизаторы», может потребоваться позвонить производителю, чтобы определить, является ли компонентом вызывающий нарушение белок, такой как молочный белок.
Когда используются расплывчатые термины, такие как «ароматизатор с высоким содержанием белка» или «натуральные ароматизаторы», может потребоваться позвонить производителю, чтобы определить, является ли компонентом вызывающий нарушение белок, такой как молочный белок.
Пациенты и родители также должны быть осведомлены о том, что пищевой белок, в отличие от сахара или жира, является удаляемым ингредиентом. Например, безлактозное молоко содержит белки коровьего молока, а многие заменители яиц содержат белки куриных яиц. И наоборот, арахисовое масло и соевое масло, как правило, не содержат пищевого белка, за исключением тех случаев, когда метод обработки не позволяет полностью удалить белок (как в случае с маслом холодного отжима или «экструзией»).
Исключение определенных продуктов может быть сложной задачей. Например, лопатка, используемая для подачи печенья как с арахисовым маслом, так и без него, может загрязнить печенье без арахиса достаточным количеством белка, чтобы вызвать реакцию. Точно так же загрязнение может произойти, когда шоколадные конфеты без арахиса обрабатываются на том же оборудовании, которое используется для производства конфет, содержащих арахис. Скрытые ингредиенты также могут вызвать проблемы. Например, для глазирования кренделей можно использовать яичный белок, а для запечатывания концов яичных рулетиков можно использовать арахисовое масло.
Точно так же загрязнение может произойти, когда шоколадные конфеты без арахиса обрабатываются на том же оборудовании, которое используется для производства конфет, содержащих арахис. Скрытые ингредиенты также могут вызвать проблемы. Например, для глазирования кренделей можно использовать яичный белок, а для запечатывания концов яичных рулетиков можно использовать арахисовое масло.
The Food Allergy Network (телефон: 1-800-929-4040) — это непрофессиональная организация, которая предоставляет образовательные материалы для помощи семьям, врачам и школам в решении трудной задачи устранения аллергенных пищевых продуктов и в подходах к лечению случайных проглатываний. Когда из рациона исключаются несколько продуктов, целесообразно заручиться помощью диетолога в составлении сбалансированной диеты.
В дополнение к устранению пищевых продуктов, вызывающих раздражение, должен быть разработан план экстренной помощи для лечения реакций, вызванных случайным проглатыванием (Рисунок 1) . Инъекционный адреналин и пероральный антигистамин всегда должны быть легко доступны для лечения пациентов с риском развития тяжелых реакций. Особое внимание следует уделить быстрому введению адреналина при первых признаках тяжелой реакции, поскольку, как сообщается, отсроченное введение связано с фатальными и почти смертельными пищевыми аллергическими реакциями. 23 Лица, осуществляющие уход, должны быть обучены показаниям к применению и введению адреналина и антигистаминных препаратов.
Инъекционный адреналин и пероральный антигистамин всегда должны быть легко доступны для лечения пациентов с риском развития тяжелых реакций. Особое внимание следует уделить быстрому введению адреналина при первых признаках тяжелой реакции, поскольку, как сообщается, отсроченное введение связано с фатальными и почти смертельными пищевыми аллергическими реакциями. 23 Лица, осуществляющие уход, должны быть обучены показаниям к применению и введению адреналина и антигистаминных препаратов.
Заключительный комментарий
К счастью, маленькие дети часто теряют чувствительность к большинству распространенных аллергенных продуктов (яйца, молоко, пшеница, соя) через несколько лет, особенно при отказе от этих продуктов. 40 Однако положительные кожные пробы могут сохраняться, несмотря на развитие клинической толерантности. Серийные диагностические пищевые проблемы с течением времени часто помогают в лечении этих детей с пищевой аллергией. К сожалению, чувствительность к определенным продуктам, таким как арахис, лесные орехи, рыба и моллюски, редко исчезает и сохраняется во взрослом возрасте.
Частота желудочно-кишечных проявлений у детей раннего возраста с аллергией на белок коровьего молока, Египет | Бюллетень Египетской педиатрической ассоциации
- Исследования
- Открытый доступ
- Опубликовано:
- Усама М. Эль-Ашир ORCID: orcid.org/0000-0002-5844-5104 1 ,
- Амира Ф. Эль-Газзар 2 ,
- Кэролайн М. Закария 1 ,
- Фарук А. Хассанейн 1 и
- …
- Халил А. Мохамед 5 3 3 0550
Бюллетень Египетской педиатрической ассоциации том 70 , Номер статьи: 34 (2022) Процитировать эту статью
800 доступов
Сведения о показателях
Abstract
История вопроса
Известно, что коровье молоко является наиболее частым пищевым аллергеном у детей первых лет жизни.
 Исключение белка коровьего молока из рациона и повторное введение его с помощью контрольного теста являются основными методами достоверной диагностики. Шкала симптомов, связанных с коровьим молоком (CoMiSS), была разработана для поставщиков первичной медико-санитарной помощи, чтобы улучшить их знания о CMPA.
Исключение белка коровьего молока из рациона и повторное введение его с помощью контрольного теста являются основными методами достоверной диагностики. Шкала симптомов, связанных с коровьим молоком (CoMiSS), была разработана для поставщиков первичной медико-санитарной помощи, чтобы улучшить их знания о CMPA.Объектив
Это исследование было проведено для определения клинических проявлений аллергии на коровье молоко у детей раннего возраста.
Методы
Поперечное исследование было проведено в отделении гастроэнтерологии и питания Детской университетской больницы с 1 января 2020 года по 31 декабря 2020 года. исследование (28 мужчин и 12 женщин). Эти младенцы были подвергнуты подробному медицинскому и социальному анамнезу пациента, всестороннему физическому осмотру и подсчету баллов CoMiSS в качестве инструмента осведомленности для подозрения на лежащую в основе аллергию на коровье молоко. Младенцы с CoMiSS более 12 баллов и положительным повторным элиминационным тестом считались подходящими для участия в нашем исследовании.

Результаты
Это исследование показало, что наиболее частыми желудочно-кишечными проявлениями, связанными с АБКМ, были срыгивание (92%), диарея (80%), колики (75%), рвота (67,5%) и, наконец, запор, который представляет собой только ( 5%).
Заключение
Регургитация и диарея являются наиболее частыми проявлениями у детей грудного возраста с доказанной аллергией на коровье молоко по шкале CoMiSS и элиминационному повторному тесту, при этом запор является наименее распространенным проявлением у этих детей.
История вопроса
Белок коровьего молока (БКМ) является ведущей причиной пищевой аллергии у детей младше 3 лет [1, 2]. Согласно недавнему метаанализу, распространенность аллергии к белкам коровьего молока (АБКМ) составляла 6% на протяжении всей жизни. Кроме того, уровень распространенности CMPA, определяемый повторным введением белка коровьего молока, составил 0,6% [3].
 Более ранние отчеты оценивали заболеваемость в 2-3% в младенческом периоде [4]. Египетское исследование, проведенное в провинции Дамиетта, показало, что частота АБКМ в первые 2 года жизни составляет 3,4%, что подтверждается положительными тестами на элиминацию пищи и пероральную пищевую провокацию (ОФК) [5].
Более ранние отчеты оценивали заболеваемость в 2-3% в младенческом периоде [4]. Египетское исследование, проведенное в провинции Дамиетта, показало, что частота АБКМ в первые 2 года жизни составляет 3,4%, что подтверждается положительными тестами на элиминацию пищи и пероральную пищевую провокацию (ОФК) [5].Младенцы с АБКМ могут испытывать ряд симптомов от легких до тяжелых при воздействии БКМ. IgE-опосредованная иммунная система чаще участвует в немедленных (ранних) реакциях, чем в отсроченных (поздних), которые могут развиваться в течение 48 часов или даже недели после потребления аллергена. Последнее, возможно, может включать иммунные системы, которые не опосредованы IgE. У одного и того же пациента могут возникать как немедленные, так и отсроченные реакции на один и тот же аллерген. Младенцы могут испытывать ряд симптомов от легких до тяжелых при воздействии CMPA. IgE-опосредованная иммунная система чаще участвует в немедленных (ранних) реакциях, чем в отсроченных (поздних), которые могут развиваться в течение 48 часов или даже недели после потребления аллергена.
 Последнее может также включать не-IgE-опосредованные иммунные механизмы [6].
Последнее может также включать не-IgE-опосредованные иммунные механизмы [6].После OFC следует элиминационная диета, которая длится от 2 до 4 недель в соответствии со стандартной диагностической процедурой для АБКМ. В реальной клинической практике открытые провокационные пробы обычно рассматриваются как достаточные, особенно у младенцев и детей младшего возраста, хотя двойная слепая плацебо-контролируемая пищевая проба является золотым стандартом для выявления пищевой аллергии [7].
Инструмент под названием «Шкала симптомов, связанных с коровьим молоком», был разработан, чтобы помочь поставщикам первичной медико-санитарной помощи выявлять симптомы, связанные с употреблением коровьего молока, у младенцев и детей младшего возраста, поскольку не существует других надежных диагностических тестов, кроме пищевой провокации белком СМ у младенцев. сомнительно, что он страдает АБКМ. Это может улучшить способность выявлять симптомы, связанные с чувствительностью к белку коровьего молока.
 Этот инструмент будет способствовать правильному принятию решений и эффективному управлению. Это предпочтут родители, потому что это позволит избежать как гипердиагностики, так и гиподиагностики, а также снизит страдания младенца и родительское беспокойство. Слишком поздняя диагностика КМПА оказывает нежелательное влияние на физическое развитие детей [8, 9].].
Этот инструмент будет способствовать правильному принятию решений и эффективному управлению. Это предпочтут родители, потому что это позволит избежать как гипердиагностики, так и гиподиагностики, а также снизит страдания младенца и родительское беспокойство. Слишком поздняя диагностика КМПА оказывает нежелательное влияние на физическое развитие детей [8, 9].].Шкала симптомов, связанных с коровьим молоком (CoMiSS), измеряет различные симптомы, включая общие, дерматологические, желудочно-кишечные и респираторные аспекты. Его также можно адаптировать для оценки и количественной оценки реакции на симптомы во время терапевтического лечения. Оценки инструмента CoMiSS варьируются от 0 до 33. Пороговое значение CoMiSS (≥12) обеспечивает высокую чувствительность около 80–90% и умеренную специфичность в диапазоне 60–70% с AUC> 0,75 для постановки диагноза аллергии на белок коровьего молока. 10, 11].
Оценка CoMiSS показала себя как надежный инструмент для повышения осведомленности медицинских работников первичного звена о дополнительных симптомах, которые могут быть вызваны коровьим молоком.
 Результаты действительно показывают, что CoMiSS более 12 будет разумной точкой отсечения для выявления младенцев, у которых проявляются симптомы, связанные с коровьим молоком. Снижение оценки до 6 или ниже также было связано с реакцией на диету, лишенную коровьего молока. Результаты мета-анализа подтвердили гипотезу о том, что CoMiSS может быть очень чувствительным и специфическим инструментом осведомленности для медицинских работников, позволяющим распознавать младенцев, у которых могут проявляться симптомы, связанные с коровьим молоком. Полезность шкалы как диагностического инструмента все еще требует подтверждения в ходе валидационного исследования [10, 12].
Результаты действительно показывают, что CoMiSS более 12 будет разумной точкой отсечения для выявления младенцев, у которых проявляются симптомы, связанные с коровьим молоком. Снижение оценки до 6 или ниже также было связано с реакцией на диету, лишенную коровьего молока. Результаты мета-анализа подтвердили гипотезу о том, что CoMiSS может быть очень чувствительным и специфическим инструментом осведомленности для медицинских работников, позволяющим распознавать младенцев, у которых могут проявляться симптомы, связанные с коровьим молоком. Полезность шкалы как диагностического инструмента все еще требует подтверждения в ходе валидационного исследования [10, 12].Методы
Это перекрестное исследование, проведенное в Детской университетской больнице с 1 января 2020 г. по 31 декабря 2020 г. В наше исследование были включены 40 младенцев в возрасте до 1 года (28 мальчиков и 12 девочек). ), обратившихся в отделение гастроэнтерологии и диетологии с жалобами на рецидивирующие или стойкие желудочно-кишечные симптомы.

Это исследование одобрено этическим комитетом медицинского факультета (номер IRB: 17100593). Младенцы, которые соответствовали критериям отбора исследования, были приглашены для участия. Было получено согласие родителей от опекуна каждого младенца, участвующего в этом исследовании.
Все участвовавшие младенцы подвергались следующему:
- 1.
Подробный анамнез, включающий подробный анамнез питания, семейный анамнез аллергических заболеваний и подробный анализ желудочно-кишечных жалоб
- 2.
Тщательное клиническое обследование.
- 3.
Оценка
CoMiSS с использованием Бристольской диаграммы стула, показывающей семь категорий стула [10]. В наше исследование были включены дети с CoMiSS более 12 баллов.

- 4.
При подозрении на заболевание был проведен тест на пищевую провокацию. Для этих детей применялась элиминационная диета в течение 4 недель; затем, после симптоматического улучшения, этим детям проводят ОФК для подтверждения диагноза.
Статистический анализ
Данные были проанализированы с использованием программного обеспечения Statistical Package for the Social Sciences (SPSS) (версия 26).
Качественные переменные записываются как частоты и проценты, которые сравниваются с помощью критерия хи-квадрат.
Количественная мера отображается в виде среднего значения ± стандартное отклонение (SD) и сравнивается с помощью критерия Стьюдента т тест. Значение P менее 0,05 будет считаться статистически значимым.

Результаты
Между социально-демографическими характеристиками младенцев наблюдалась очень значительная разница. Что касается возраста при поступлении, то большинство исследованных нами младенцев начали предъявлять жалобы и предъявляли жалобы до 6-месячного возраста ( P = 0,0077 и <0,0001 соответственно). Мужской пол был значительно выше женского ( P = 0,0004). Более того, АБКМ чаще встречался среди детей с положительным кровным родством ( P = 0,0019). У 33 (82,5%) детей раннего возраста с семейным анамнезом аллергических заболеваний выявлена АБКМ ( P < 0,0001), как показано в табл. 1.
tableТабл. 2 и рис. 1 показывают, что наиболее частыми желудочно-кишечными проявлениями являются регургитация (92%), затем диарея (80%), колики (75%), рвота (67,5%), а наименее частыми проявлениями являются запор (5%).
Таблица 2. Желудочно-кишечные проявления в исследованных случаях
Желудочно-кишечные проявления в исследованных случаях Полная таблица
Рис. 1Частота желудочно-кишечных проявлений у детей раннего возраста с АБКМ
Изображение в натуральную величину
Из табл. наличие КМПА. 67,5% исследованных случаев были младенцами на искусственном вскармливании, а 12,5% — на грудном вскармливании ( P < 0,0001). Двадцать процентов младенцев находились на смешанном вскармливании ( P = 0,028).
Таблица 3 Анамнез питания исследованных случаевПолный размер таблицы
Хотя только 20 детей начали прикорм, АБКМ наблюдалась у детей, которые начали прикорм после 6 месяцев, больше, чем у тех, кто начал прикорм до 6 месяцев (60 против 40). %, P = 0,076).
Обсуждение
Аллергия на белок коровьего молока считается наиболее распространенным типом пищевой аллергии в младенчестве и детстве. Проблемным моментом является отсутствие специального теста для точного диагноза АБКМ.
 OFC с отменой белка коровьего молока на 4 недели, а затем повторным введением при тщательном наблюдении за исчезновением симптомов после отмены и рецидивом после повторного введения по-прежнему является золотым стандартом теста для диагностики АБКМ. Наше исследование показало, что социально-демографические характеристики в значительной степени связаны с CMPA. Мужской пол больше подвержен влиянию АБКМ, чем женский. Это согласуется с Selbuz et al. которые сообщили о значительном преобладании мужчин в CMPA среди мужской группы. Вероятно, это можно объяснить генетической предрасположенностью. Сцепленный с Х-хромосомой рецессивный признак, связанный с аллергическим заболеванием, с большей вероятностью будет проявляться у мужчин (XY) и может объяснить, почему пищевая аллергия у мужчин чаще встречается в очень молодом возрасте [13].
OFC с отменой белка коровьего молока на 4 недели, а затем повторным введением при тщательном наблюдении за исчезновением симптомов после отмены и рецидивом после повторного введения по-прежнему является золотым стандартом теста для диагностики АБКМ. Наше исследование показало, что социально-демографические характеристики в значительной степени связаны с CMPA. Мужской пол больше подвержен влиянию АБКМ, чем женский. Это согласуется с Selbuz et al. которые сообщили о значительном преобладании мужчин в CMPA среди мужской группы. Вероятно, это можно объяснить генетической предрасположенностью. Сцепленный с Х-хромосомой рецессивный признак, связанный с аллергическим заболеванием, с большей вероятностью будет проявляться у мужчин (XY) и может объяснить, почему пищевая аллергия у мужчин чаще встречается в очень молодом возрасте [13].Что касается возраста проявления, это исследование показало, что АБКМ чаще встречается у младенцев в возрасте до 6 месяцев. Младенцы обычно поступают с АБКМ в течение первых нескольких месяцев жизни.
 Наиболее вероятно, что КМПА возникает в момент введения прикорма (любого его вида) и снижается к годовалому возрасту. Дети, находящиеся на грудном вскармливании, более подвержены аллергическому проктоколиту, индуцированному пищевым белком [14], тогда как синдром энтероколита, индуцированного пищевым белком, обычно возникает при искусственном вскармливании [15].
Наиболее вероятно, что КМПА возникает в момент введения прикорма (любого его вида) и снижается к годовалому возрасту. Дети, находящиеся на грудном вскармливании, более подвержены аллергическому проктоколиту, индуцированному пищевым белком [14], тогда как синдром энтероколита, индуцированного пищевым белком, обычно возникает при искусственном вскармливании [15].Кроме того, кровное родство и положительный семейный анамнез аллергических заболеваний играют решающую роль. Наше исследование показало, что заболеваемость КМПА была выше у детей раннего возраста с положительным кровным родством и отягощенным семейным анамнезом по аллергическим заболеваниям. Этот вывод согласуется с данными различных исследований, которые показали, что семейный анамнез атопии был значительным в случаях с АБКМ, и риск атопии увеличивается, если у родителей или братьев и сестер есть атопическое заболевание. Кроме того, если оба родителя страдают атопией, риск еще выше [16, 17]. Как мы обсуждали ранее, аллергия является рецессивным признаком, сцепленным с Х-хромосомой, поэтому АБКМ была более распространена среди исследованных нами младенцев с положительным кровным родством и семейным анамнезом аллергических заболеваний.
 Это особенно важно в таких странах, как Египет, где кровное родство родителей является обычным явлением. Недавнее исследование, проведенное на Южном Синае (Египет), показало, что от 21 до 33% супружеских пар являются родственниками, а в сельской местности показатели выше, чем в городских [18].
Это особенно важно в таких странах, как Египет, где кровное родство родителей является обычным явлением. Недавнее исследование, проведенное на Южном Синае (Египет), показало, что от 21 до 33% супружеских пар являются родственниками, а в сельской местности показатели выше, чем в городских [18].Что касается частоты желудочно-кишечных проявлений, то наиболее частыми были срыгивания, затем диарея, колики, рвота, а наименее частыми проявлениями были запоры. Наше исследование соответствовало исследованиям Dominguez-Ortega et al. которые продемонстрировали, что у большинства больных детей с АБКМ были другие симптомы, затрагивающие одну или несколько систем органов, обычно желудочно-кишечный тракт и/или кожу [10]. Максуд и др. сообщили, что дети с подозрением на АБКМ обычно имеют желудочно-кишечные проявления [12]. Кроме того, Selbuz et al. сообщили о значительной разнице в клинической картине между младенцами с АБКМ(+) и (-), при этом 60,4% младенцев с АБКМ(+) сообщают о более чем 5 эпизодах регургитации в день, что позволяет предположить, что тяжесть регургитации может быть фактором при определении необходимости тестирования младенца на АБКМ [13].
 В практических рекомендациях ESPGHAN GI Committee указано, что дисфагия, частая регургитация, колики, боль в животе, рвота, анорексия, отказ от еды, диарея (с нарушением всасывания или без него или потерей белка из-за энтеропатии) и запор с перианальной сыпью или без нее являются частыми, но неспецифическими явлениями. Признаки АБКМ со стороны желудочно-кишечного тракта у младенцев и детей младшего возраста [9].].
В практических рекомендациях ESPGHAN GI Committee указано, что дисфагия, частая регургитация, колики, боль в животе, рвота, анорексия, отказ от еды, диарея (с нарушением всасывания или без него или потерей белка из-за энтеропатии) и запор с перианальной сыпью или без нее являются частыми, но неспецифическими явлениями. Признаки АБКМ со стороны желудочно-кишечного тракта у младенцев и детей младшего возраста [9].].Грудное вскармливание остается доказательством того, что это лучший вид вскармливания младенцев, его защитный эффект против АБКМ был выражен в нашем исследовании, где младенцы на искусственном вскармливании превосходили младенцев на грудном вскармливании. Jakaitis & Denning также заявили, что у младенцев, которых кормили грудным молоком, наблюдалось снижение частоты аллергических заболеваний [14]. Жирная кислота с короткой цепью, образующаяся в результате деградации олигосахаридов грудного молока колонизирующими бактериями, которая играет роль в укреплении целостности плотных соединений, может быть использована для объяснения этого защитного действия грудного молока против инфекционных заболеваний и атопических расстройств [15, 16].
 ].
].В то же время было показано, что исключительно грудное вскармливание защищает от АБКМ. Наше исследование четко показало четкую разницу между временем введения прикорма и возникновением КМПА, которая была статистически значимой. Защитный эффект исключительно грудного вскармливания был подчеркнут в предыдущих исследованиях, в которых также сообщалось, что риск аллергии на белок коровьего молока был снижен у детей, находящихся на исключительно грудном вскармливании [12, 17]. В изученных нами случаях ВМПА наблюдали у детей раннего возраста, которые начали прикорм после 6-месячного возраста. Согласно Дю Туа и соавт. В исследовании 2015 года «Изучение раннего изучения арахиса (LEAP)» и результатах исследования Inquiring About Tolerance мы обнаружили согласие с нашими выводами [18,19].,20]. Введение прикорма в возрасте от 4 до 6 месяцев является лучшим временем для снижения частоты возникновения аллергии, как это рекомендуется в большинстве международных руководств, в том числе в рекомендациях Американского и Европейского комитетов экспертов по аллергии, поскольку оба предполагают, что раннее введение прикорма введение пищи может защищать от аллергии [21, 22].

Это исследование было проведено в одной из крупнейших университетских больниц в Верхнем Египте, и при наборе наших случаев мы заметили выраженные крайности в диагностике АБКМ с явно выраженной гипердиагностикой и гиподиагностикой. Во многих случаях АБКМ был ошибочно диагностирован на основании клинических критериев персистирующих или рецидивирующих желудочно-кишечных проявлений, а иногда и в зависимости от некоторых исследований, которые оказались несущественными для диагностики АБКМ, таких как наличие скрытой крови в кале, уровень фекального кальпротектина в кале, состояние кожи. прик-тест или пищевая панель IgE сыворотки. С другой стороны, во многих из наших случаев, у которых было доказано наличие CMPA с помощью теста OFC, был ошибочно диагностирован непереносимость лактозы, персистирующий гастроэнтерит, дизентерия, стеноз привратника, ГЭРБ, функциональный запор или анальная трещина. Высокий индекс подозрительности, правильное применение CoMiSS и OFC являются краеугольными камнями для ранней диагностики и лечения АБКМ.

Заключение
Диагноз АБКМ следует рассматривать у младенцев с персистирующими или рецидивирующими проявлениями ЖКТ. Срыгивание и диарея являются наиболее распространенными проявлениями у младенцев с аллергией на коровье молоко с помощью шкалы CoMiSS и теста OFC, где запор является наименее распространенным проявлением для этих младенцев.
Доступность данных и материалов
Все данные, полученные или проанализированные в ходе этого исследования, включены в эту опубликованную статью и ее дополнительный файл.
Ссылки
Van Boxstael S, Habib I, Jacxsens L et al (2013) Вопросы безопасности пищевых продуктов в свежих продуктах: бактериальные патогены, вирусы и остатки пестицидов, указанные заинтересованными сторонами в цепочке свежих продуктов как основные проблемы. Пищевой контроль 32:190–197
Статья Google Scholar
«>
Guler N, Cokugras FC, Sapan N et al (2020) Диагностика и лечение аллергии на белок коровьего молока в Турции: рекомендации группы экспертов для конкретных регионов. Аллергол Иммунопатол (Мадр) 48:202–210
Артикул КАС Google Scholar
Kelly C, Gangur V (2009) Половое неравенство в отношении пищевой аллергии: данные из базы данных PubMed. J Allergy (Каир) 2009:159845
Google Scholar
Mennini M, Fiocchi AG, Cafarotti A et al (2020)Аллергический проктоколит, вызванный пищевыми белками, у младенцев: обзор литературы и предложение протокола ведения. World Allergy Organ J 13:100471
Артикул КАС Google Scholar
Feuille E, Nowak-Węgrzyn A (2014)Определение, этиология и диагностика синдрома энтероколита, вызванного пищевыми белками.
 Curr Opin Allergy Clin Immunol 14:222–228
Curr Opin Allergy Clin Immunol 14:222–228Статья КАС Google Scholar
Björkstén B (2005) Генетические и экологические факторы риска развития пищевой аллергии. Curr Opin Allergy Clin Immunol 5:249–253
Артикул Google Scholar
Муштак И., Чима Х.А., Малик Х.С., Вахид Н., Хашми М.А., Малик Х.С. (2017) Причины хронической неинфекционной диареи у младенцев в возрасте до 6 месяцев: редко распознаваемые объекты. J Ayub Med Coll Abbottabad 29: 78–82
PubMed Google Scholar
Ямама Г., Абдель-Рауф Э., Талаат А., Саад-Хусейн А., Хамами Х., Мегид Н.А. (2013) Распространенность кровнородственных браков на Южном Синае, Египет. J Biosoc Sci 45: 31–39
Артикул КАС Google Scholar
«>Домингес-Ортега Г., Боррелли О., Мейер Р. и др. (2014) Внекишечные проявления у детей с желудочно-кишечной пищевой аллергией. J Педиатр Гастроэнтерол Нутр 59:210–214
Артикул Google Scholar
Vandenplas Y, Mukherjee R, Dupont C, Eigenmann P, Høst A, Kuitunen M, Ribes-Koninkx C, Shah N, Szajewska H, von Berg A, Heine RG, Zhao Z-Y (2018) Протокол валидации чувствительность и специфичность Шкалы симптомов, связанных с коровьим молоком (CoMiSS), в отношении открытой пищевой провокации в одиночном слепом, проспективном, многоцентровом исследовании у младенцев. BMJ Open 8: e019968.
 https://doi.org/10.1136/bmjopen-2017-019968
https://doi.org/10.1136/bmjopen-2017-019968Артикул пабмед ПабМед Центральный Google Scholar
Maksoud HMA, Al Seheimy LAF, Hassan KAG, Salem MF, Elmahdy EAM (2019) Частота аллергии на белок коровьего молока у детей в течение первых 2 лет жизни в провинции Дамиетта. Al-Azhar Assiut Med J 17:86
Статья Google Scholar
Selbuz SK, Altuntaş C, Kansu A et al (2020) Оценка инструмента оценки осведомленности о симптомах, связанных с коровьим молоком, у маленьких турецких детей. Дж Педиатр Детское Здоровье 56:1799–1805
Артикул Google Scholar
Jakaitis BM, Denning PW (2014) Грудное молоко человека и врожденная иммунная система желудочно-кишечного тракта. Clin Perinatol 41:423–435
Статья Google Scholar
«>Ríos-Covián D, Ruas-Madiedo P, Margolles A, Gueimonde M, De Los Reyes-Gavilán CG, Salazar N (2016)Жирные кислоты с короткой цепью в кишечнике и их связь с диетой и здоровьем человека. Front Microbiol 7:185
Артикул Google Scholar
El Desouky AI, Anany HG, Mohammed ISI (2021) Оценка CoMiSS среди детей с аллергией на коровье молоко в университетской больнице Zagazig. Египет J Hosp Med 83: 838–843
Артикул Google Scholar
Логан К.
 , Флор С., Лак Г., Перкин М. (2011) Исследование EAT — раннее введение аллергенных продуктов для индукции толерантности у младенцев. Clin Exp Allergy 41:1859–1860
, Флор С., Лак Г., Перкин М. (2011) Исследование EAT — раннее введение аллергенных продуктов для индукции толерантности у младенцев. Clin Exp Allergy 41:1859–1860Google Scholar
Rosário FN (2015) Раннее введение пищи для предотвращения пищевой аллергии. Исследование LEAP (Раннее изучение арахиса). Преподобный Пол Педиатр 33: 493–494
Google Scholar
Перкин М.Р., Логан К., Маррс Т. и др. (2016) Исследование толерантности (EAT): осуществимость режима раннего введения аллергенной пищи. J Allergy Clin Immunol 137:1477–1486 e8
Статья Google Scholar
Fleischer DM, Spergel JM, Assa’ad AH, Pongracic JA (2013)Первичная профилактика аллергических заболеваний с помощью пищевых вмешательств. J Allergy Clin Immunol Pract 1:29–36
Артикул Google Scholar
«>Медицинский факультет, Детская больница Университета Асьюта, Асьют, Египет
Осама М. Эль-Ашир, Кэролайн М. Закария и Фарук А. Хассанейн 9 0504030 9 050403 9 050403 9 Здоровье и Кафедра общественной медицины, медицинский факультет, Университет Асьюта, Университет Бадр в Каире, Асьют, Египет
Амира Ф.
 Эль-Газзар
Эль-ГаззарПедиатрическое отделение, Каирский университет, Каир, Египет
Халил А. Мохамед
- Amira F. El-Gazzar
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Кэролайн М. Закария
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Farouk A. Hassanein
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Khalil A. Mohamed
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
Колетцко С., Ниггеманн Б., Арато А. и др. (2012) Подход к диагностике и лечению аллергии на белок коровьего молока у младенцев и детей: Практические рекомендации комитета ESPGHAN GI. J Pediatr Gastroenterol Nutr 55:221–229
Статья КАС Google Scholar
Gao Y, Davis B, Zhu W, Zheng N, Meng D, Walker WA (2021) Бутират короткоцепочечной жирной кислоты, метаболит грудного молока, усиливает незрелые гены барьерной функции кишечника в ответ на воспаление in vitro и in vitro виво. Am J Physiol Gastrointest Liver Physiol 320:G521–G530
Артикул КАС Google Scholar
Greer FR, Sicherer SH, Burks AW, Комитет по питанию, Секция аллергии и иммунологии (2019) Влияние раннего вмешательства в области питания на развитие атопического заболевания у младенцев и детей: роль ограничения питания матери, грудное вскармливание , гидролизные смеси и сроки введения аллергенного прикорма. Педиатрия 143:e201
Статья Google Scholar
Ссылки на скачивание
Благодарности
Нет
Финансирование
У авторов нет финансовых отношений, имеющих отношение к этой статье, чтобы раскрыть.
Информация об авторе
Авторы и организации
Авторы
- Эль-сама М. авторские публикации
Вы также можете искать этого автора в PubMed Google Scholar
Вклады
Усама М. Эль-Ашир, Амира Эль-Газзар и Фарук Хассанейн разработали исследование. Усама М. Эль-Ашир и Кэролайн М. Закария участвовали в поиске литературы, интерпретировали данные и написали рукопись. Амира Ф. Эль-Газзар провела статистический анализ и участвовала в поиске и написании литературы. Халил А. Мохамед участвовал в написании и публикации. Авторы прочитали и одобрили окончательный вариант рукописи.
Эль-Ашир, Амира Эль-Газзар и Фарук Хассанейн разработали исследование. Усама М. Эль-Ашир и Кэролайн М. Закария участвовали в поиске литературы, интерпретировали данные и написали рукопись. Амира Ф. Эль-Газзар провела статистический анализ и участвовала в поиске и написании литературы. Халил А. Мохамед участвовал в написании и публикации. Авторы прочитали и одобрили окончательный вариант рукописи.
Автор, ответственный за переписку
Переписка с Усама М. Эль-Ашир.
Декларация этики
Одобрение этики и согласие на участие
Исследование было одобрено комитетом по этике медицинского факультета Университета Асьют (IRB №: 17100593). У родителей было получено письменное информированное согласие с объяснением преимуществ исследования, ожидаемых рисков и предлагаемого лечения для каждого случая.
Согласие на публикацию
К участию приглашались младенцы, соответствующие критериям отбора исследования. Было получено согласие родителей от опекуна каждого младенца, участвующего в этом исследовании.
Конкурирующие интересы
Авторы заявляют, что у них нет конкурирующих интересов.
Дополнительная информация
Примечание издателя
Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Права и разрешения
Открытый доступ Эта статья находится под лицензией Creative Commons Attribution 4.0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или в любом формате, при условии, что вы укажете соответствующую ссылку на оригинальный автор(ы) и источник, предоставьте ссылку на лицензию Creative Commons и укажите, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons на статью, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя.
