Содержание
Желточно-кишечный проток эмбриона. Желточный мешок эмбриона человека
Обновлено: 27.10.2022
По данным публикации в журнале Ультразвука в медицине(Journal of Ultrasound in Medicine) за январь 2012 — Sonographic Evaluation of the Yolk Sac / Сонографическая оценка желточного мешка — внешняя ссылка
Вторичный желточный мешок является первой экстраэмбриональной структурой, которая становится сонографически видимой в пределах гестационного мешка(*плодного яйца). Во время эмбрионального развития желточный мешок является основным путем обмена между эмбрионом и матерью. Желточный мешок также обеспечивает пищевую, иммунологическую, метаболическую, эндокринную и кроветворную функции до тех пор, пока не будет установлена плацентарная циркуляция. Таким образом, желточный мешок имеет решающее значение в ранней эмбриональной жизни.
Желточный мешок является одной из наиболее важных концептуальных структур, оцениваемых сонографически в первом триместре. В настоящее время наиболее важным преимуществом сонографической оценки желточного мешка является подтверждение внутриутробной беременности. Была выдвинута гипотеза, что сонографические характеристики, связанные с формой, размером и внутренней структурой желточного мешка, могут быть связаны с гестационным исходом.
Была выдвинута гипотеза, что сонографические характеристики, связанные с формой, размером и внутренней структурой желточного мешка, могут быть связаны с гестационным исходом.
Эта публикация направлена на информирование врачей путем обобщения нормальных и аномальных сонографических данных желточного мешка в течение первого триместра беременности.
В исследование вошли беременные женщины, которые прошли УЗИ в первом триместре, в период с 5-й по 13-ю недели беременности. Все данные УЗИ были рассмотрены двумя радиологами, имеющими опыт в акушерской сонографии. УЗИ проводились на аппарате LOGIQ 9 с помощью многочастотного трансвагинального датчика с частотой от 5 до 8 МГц (GE Healthcare, Milwaukee, WI). Гестационный возраст в неделях определялся по КТР или диаметру плодного яйца.
На четвертой неделе эмбрионального развития стенка желточного мешка состоит из 3 тонких клеточных слоев: экто-, мезо- и эндодермы.
Начиная с пятой недели беременности, в стенке желточного мешка четко выделяются две части. Мезодермальная часть представлена кровеносными сосудами и мезенхимальной тканью, тогда как эндодермальная состоит из эндодермального эпителия и эндодермальных везикул или канальцев.
Мезодермальная часть представлена кровеносными сосудами и мезенхимальной тканью, тогда как эндодермальная состоит из эндодермального эпителия и эндодермальных везикул или канальцев.
После седьмой недели эмбрионального развития в желточном мешке начинают появляться признаки регрессии.
Желточный мешок может быть легко обнаружен на ТВУЗИ, когда средний диаметр гестационного мешка составляет от 5 до 6 мм. Общепринято, что желточный мешок должен наблюдаться, когда размер гестационного мешка более 8 мм. Желточный мешок соединен с эмбрионом желточным протоком. В норме желточный мешок выглядит как округлая структура с анэхогенным центром, окруженным однородной четко выраженной эхогенной стенкой(*проще говоря, как киста). Обычно внутренний диаметр желточного мешка составляет от 3 до 5 мм. Фактически, размер желточного мешка постепенно увеличивается с начала 5-й гестационной недели до конца 10-й гестационной недели. После этого размер желточного мешка постепенно уменьшается.
Количество желточных мешочков, присутствующих в гестационном мешочке, может помочь в определении амниональности беременности.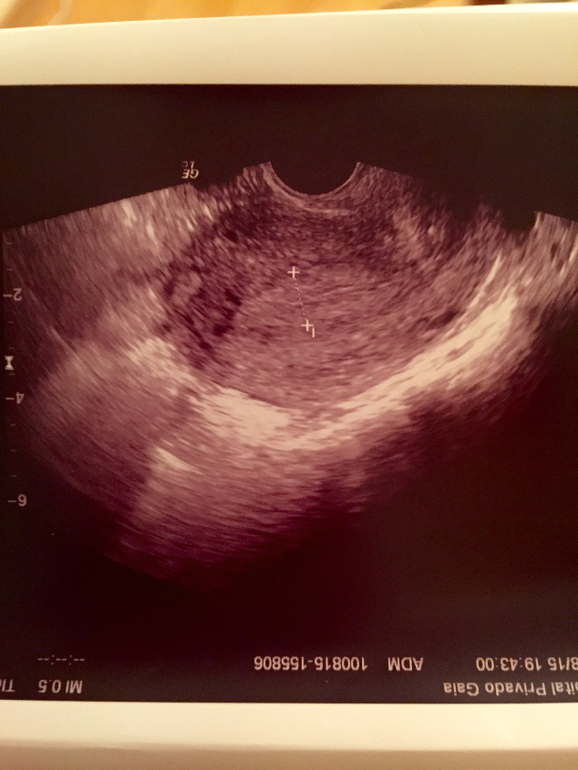 Как правило, количество желточных и амниотических мешков совпадает, если эмбрионы живы. Таким образом, в монохориальной моноамниотической беременности будет 2 эмбриона, 1 хорионический мешок, 1 амниотический мешок и 1 желточный мешок.
Как правило, количество желточных и амниотических мешков совпадает, если эмбрионы живы. Таким образом, в монохориальной моноамниотической беременности будет 2 эмбриона, 1 хорионический мешок, 1 амниотический мешок и 1 желточный мешок.
При отсутствии на этом сроке беременности желточного мешка обычно обнаруживают мертвый эмбрион. Редко можно наблюдать желточный мешок и пустой амниотический мешок без эмбриона. Последствием эмбриональной смерти, вероятно, является реабсорбция очень раннего эмбриона, амниона и желточного мешка. Однако эти утверждения в значительной степени не подтверждены, потому что, насколько это известно, нет опубликованных исследований, которые сообщали бы точный порядок процесса реабсорбции.
В серии наблюдений Levi et al. 1996г. было оценено 4 монохориальных моноамниотических беременностей с одним желточным мешком. Одна из этих беременностей была соединенной двойней, тогда как другая беременность включала внематочную двойню. Обе эти беременности были прерваны.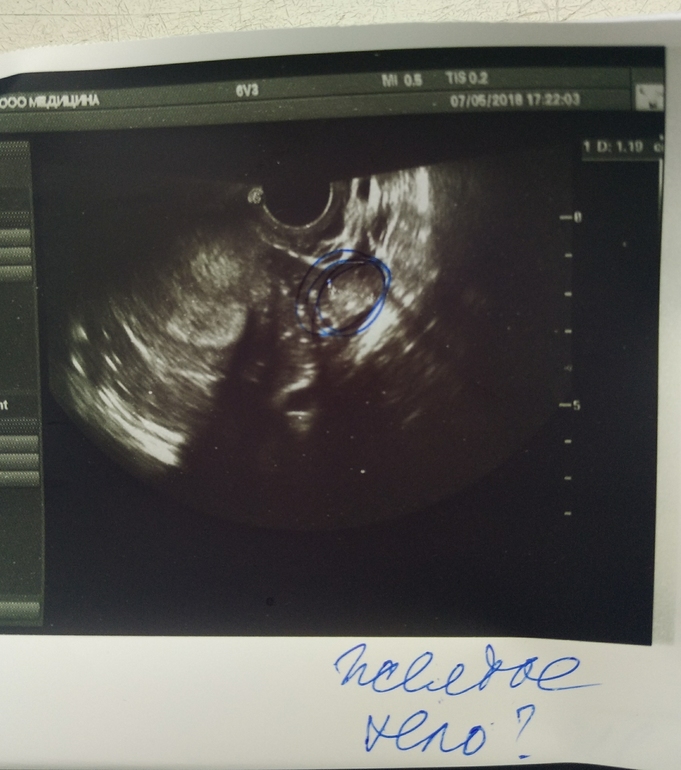 Остальные 2 беременности родились нормально на 34-й неделе беременности. Из 4 случаев у 2 был желточный мешок больше, чем обычно (> 5,6 мм), тогда как желточный мешок был нормальным в других беременностях. Эмбриональная сердечная деятельность отмечалась во всех исследованных беременностях.
Остальные 2 беременности родились нормально на 34-й неделе беременности. Из 4 случаев у 2 был желточный мешок больше, чем обычно (> 5,6 мм), тогда как желточный мешок был нормальным в других беременностях. Эмбриональная сердечная деятельность отмечалась во всех исследованных беременностях.
Аномальный желточный мешок:
— отсутствие желточного мешка
Желточный мешок выполняет важные функции для эмбрионального развития в процессе органогенеза. При трансвагинальной сонографии в обозначенные сроки беременности отсутствие желточного мешка в присутствии эмбриона всегда ненормально и в целом связано с последующей эмбриональной смертью.
— большой желточный мешок
Несмотря на отсутствие четко определенного консенсуса, большинство авторов принимают в качестве верхнего предела размера нормального желточного мешка при беременности с гестационным возрастом от 5 до 10 недель либо 5, либо 6 мм. Недавнее исследование показало, что диаметр желточного мешка более 5 мм связан с повышенным риском самопроизвольного аборта. Однако некоторые авторы упоминали о существовании очень большого желточного мешка (например, 8,1 мм) при нормальной живой беременности. В целом было высказано предположение, что аномально большой желточный мешок может указывать на плохой акушерский исход; поэтому для этих беременностей рекомендуется тщательное наблюдение с помощью УЗИ.
Однако некоторые авторы упоминали о существовании очень большого желточного мешка (например, 8,1 мм) при нормальной живой беременности. В целом было высказано предположение, что аномально большой желточный мешок может указывать на плохой акушерский исход; поэтому для этих беременностей рекомендуется тщательное наблюдение с помощью УЗИ.
— маленький желточный мешок
В литературе представлены скудные сведения о клинической значимости маленьких желточных мешков. Было заявлено, что очень маленький желточный мешок может быть нормальной находкой в ранние периоды нормального эмбрионального развития. С другой стороны, раннее опубликованное исследование, с определенными ограничениями, предполагало, что диаметр желточного мешка 2 мм или менее может быть связан с неблагоприятным исходом при беременности с гестационным возрастом от 8 до 12 недель.
Хорошо известно, что размер желточного мешка начинает уменьшаться в течение последних недель первого триместра. Этот процесс является причиной того, что при оценке размера желточного мешка следует учитывать гестационный возраст.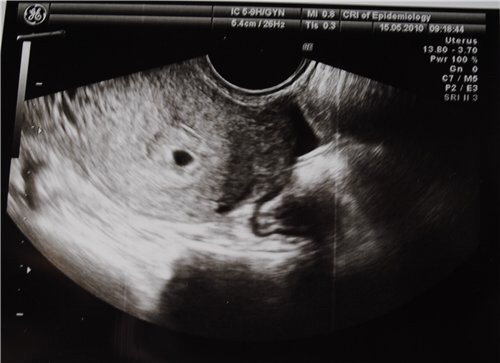 Тем не менее, было бы разумно выполнить повторные УЗИ в течение короткого периода времени, если был выявлен меньший, чем ожидалось, желточный мешок.
Тем не менее, было бы разумно выполнить повторные УЗИ в течение короткого периода времени, если был выявлен меньший, чем ожидалось, желточный мешок.
— кальцинированный желточный мешок
— гиперэхогенный желточный мешок
Эхогенность желточного мешка может повышаться и по другим причинам, отличным от кальцинирования(*на представленной в публикации эхограмме, » гиперэхогенный» желточный мешок, в отличие от рассмотренных ранее также гиперэхогенных кальцинированных ЖМ выглядит менее эхогенно и имеет гипоэхогенный компонент на месте анэхогенного). Гармоническая визуализация тканей может быть более полезной для подтверждения этого. Насколько известно, только в одном исследовании сообщалось, что эхогенный желточный мешок может быть связан с гибелью плода или аномалиями. По опыту авторов публикации, эхогенный желточный мешок не связан с аномалиями или плохим исходом беременности. В соответствующей литературе также было подчеркнуто, что эхогенный желточный мешок не предсказывает эмбриональную аномалию или смерть.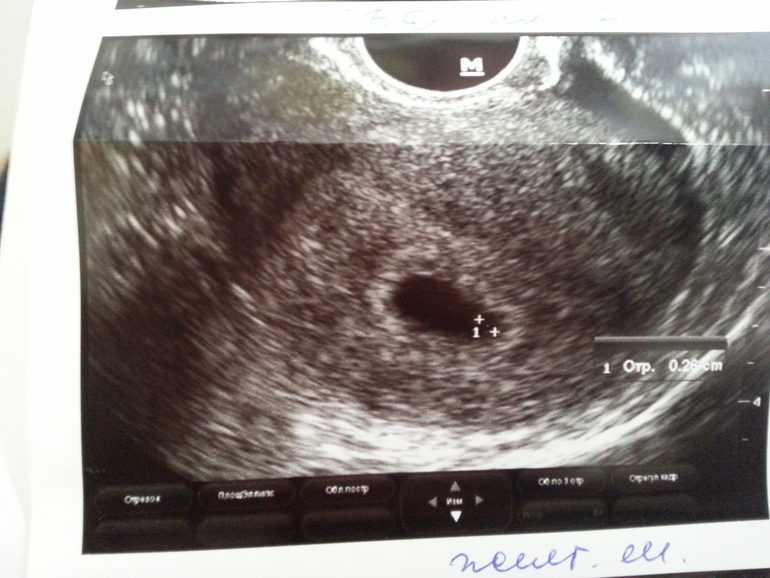 На самом деле, ожидается, что крупномасштабные проспективные исследования прояснят прогностическую значимость эхогенных желточных мешков.
На самом деле, ожидается, что крупномасштабные проспективные исследования прояснят прогностическую значимость эхогенных желточных мешков.
— неровная форма желточного мешка
Желточные мешки со сморщенными краями/ вдавленными стенками обычно идентифицируются как имеющие неправильную форму. Клиническое значение аномальной формы желточного мешка является спорным и, таким образом, все еще обсуждается(*однако на представленных эхограммах » гиперэхогенного» и кальцинированного ЖМ можно наблюдать эти характеристики). Существует ряд клинических исследований, в которых было заявлено, что персистенция неправильной формы желточного мешка может использоваться для указания на неблагоприятный гестационный исход. Тем не менее, недавно опубликованное исследование предполагает, что неправильная форма желточного мешка не связана с повышенным риском самопроизвольного аборта.
— персистирование желточного мешка
После 10-11й недели беременности желточный мешок начинает быстро сокращаться и в конечном итоге исчезает.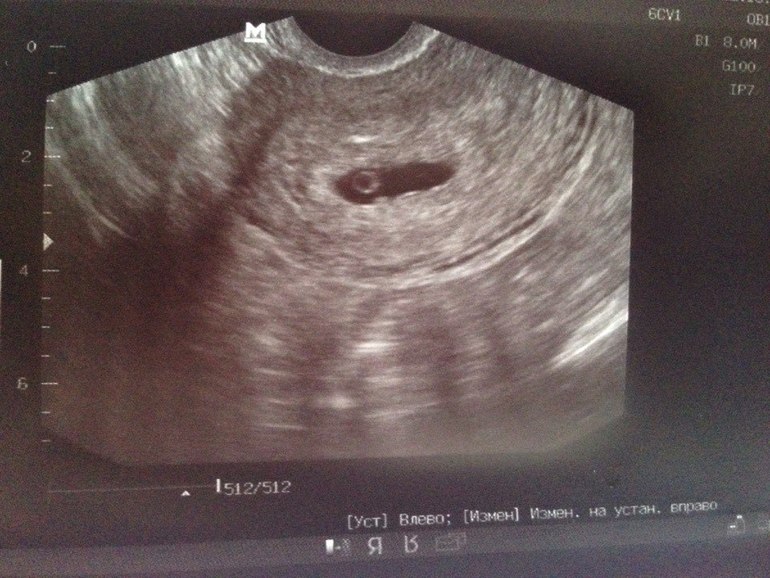 Однако иногда желточный мешок может сохраняться между амнионом и хорионом даже после 12 недель беременности. Такой персистирующий желточный мешок обычно стоит близко к месту, где пуповина входит в плаценту. Клиническое значение персистирующего желточного мешка неизвестно.
Однако иногда желточный мешок может сохраняться между амнионом и хорионом даже после 12 недель беременности. Такой персистирующий желточный мешок обычно стоит близко к месту, где пуповина входит в плаценту. Клиническое значение персистирующего желточного мешка неизвестно.
Оценка желточного мешка должна быть частью полного сонографического исследования в первом триместре. Выявленные аномалии желточного мешка могут предсказать последующую эмбриональную смерть. Поэтому точное распознавание нормальных и аномальных сонографических данных, связанных с желточным мешком, может быть использовано для прогнозирования течения беременности.
Желточный проток
канал в желточном стебельке, выстланный эктодермальным эпителием, соединяющий полость средней кишки зародыша с желточной полостью; Ж. п. у человека, не подвергшийся обратному развитию, называется дивертикулом подвздошной кишки (меккелевым дивертикулом).
1. Малая медицинская энциклопедия. — М.: Медицинская энциклопедия. 1991—96 гг. 2. Первая медицинская помощь. — М.: Большая Российская Энциклопедия. 1994 г. 3. Энциклопедический словарь медицинских терминов. — М.: Советская энциклопедия. — 1982—1984 гг .
1991—96 гг. 2. Первая медицинская помощь. — М.: Большая Российская Энциклопедия. 1994 г. 3. Энциклопедический словарь медицинских терминов. — М.: Советская энциклопедия. — 1982—1984 гг .
Смотреть что такое «Желточный проток» в других словарях:
желточный проток — (ductus vitellinus, LNE; син.: желточно кишечный проток, пупочно кишечный проток) канал в желточном стебельке, выстланный энтодермальным эпителием, соединяющий полость средней кишки зародыша с желточной полостью; Ж. п. у человека, не подвергшийся … Большой медицинский словарь
Желточный проток — (Ductus vitellointestinalis) канал, соединяющий желточный мешок (см.) с полостью кишечника зародыша … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Желточный мешок или пузырь — (Vesicula umbilicalis) мешкообразный придаток на брюшной стороне зародыша большей части позвоночных, заключающий в себе запас питательного желтка и соединенный с полостью кишечника посредством желточного протока. У тех низших позвоночных, у… … Энциклопедический словарь Ф. А. Брокгауза и И.А. Ефрона
А. Брокгауза и И.А. Ефрона
желточный стебелек — (caulis vitellinus,. LNE) трубчатое образование между средней кишкой зародыша и желточным мешком; внутри Ж. с. проходит желточный проток … Большой медицинский словарь
желточный стебелёк — ЭМБРИОЛОГИЯ ЖИВОТНЫХ ЖЕЛТОЧНЫЙ СТЕБЕЛЁК — проток между кишкой и желточным мешком … Общая эмбриология: Терминологический словарь
желточно-кишечный проток — см. Желточный проток … Большой медицинский словарь
пупочно-кишечный проток — (ductus omphaloentericus) см. Желточный проток … Большой медицинский словарь
dried yolk — желточный порошок yolk sac желточный мешок yolk duct желточный проток yolk stalk желточный проток … English-Russian travelling dictionary
Пуповина — Новорождённый после кесарева сечения. Пуповина не перерезана Пуповина, или пупочный канатик (лат. funiculus umbilicalis) особый орган, соединяющий эмб … Википедия
Общий взгляд на жизнь рыб — Рыбы образуют тот класс позвоночных животных, представители которого, все без исключения, дышат жабрами. Этими немногими словами класс рыб очерчивается гораздо резче и определеннее, чем обстоятельным и точным описанием строения их… … Жизнь животных
Этими немногими словами класс рыб очерчивается гораздо резче и определеннее, чем обстоятельным и точным описанием строения их… … Жизнь животных
Зародыш — I Зародыш (embryo; синоним эмбрион) организм на ранних стадиях развития, образовавшийся из оплодотворенной яйцеклетки. В акушерстве и гинекологии З. называют организм в течение первых 8 нед. развития. Внутриутробное развитие с 9 й по 38 39 неделю … Медицинская энциклопедия
Фото УЗИ при беременности, фото плода при УЗИ во время беременности
Фото УЗИ плода при беременности 4-5 недель
Самый ранний срок, на котором можно разглядеть с помощью трансвагинального УЗИ плодное яйцо в полости матки — это 30-й день гестации, или 4-5 акушерских недель беременности. Уровень ХГЧ крови при этом должен быть не менее 1000 мЕд/мл. В это время ещё не видно ни эмбриона, ни желточного мешка. При визуализации двух плодных яиц можно утверждать, что это дихориальная многоплодная беременность. При визуализации одного плодного яйца можно утверждать, что это монохориальная беременность.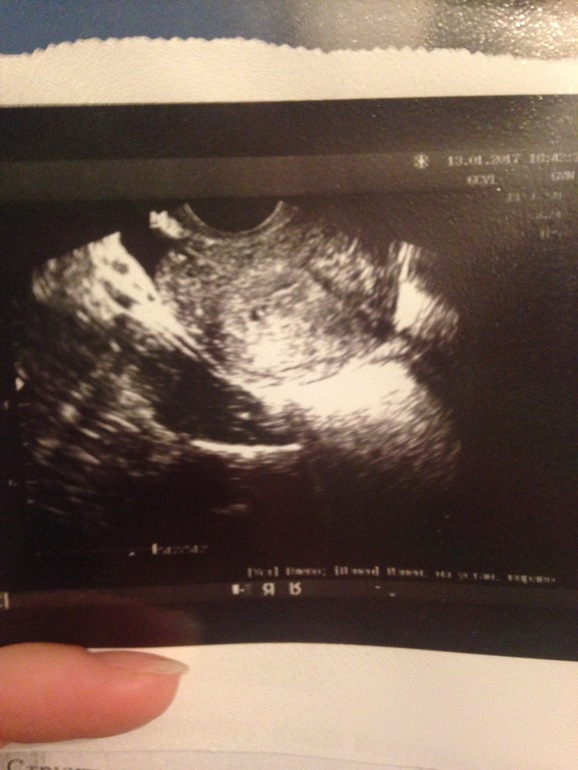 Но на этом сроке мы ещё не можем сказать сколько эмбрионов находится в каждом плодном яйце. Кроме того, во время однократного УЗИ мы ещё не можем сказать, прогрессирует ли данная беременность, так как у эмбриона ещё нет сердцебиения. Средний внутренний диаметр (СВД) плодного яйца на этом сроке 2-10 мм.
Но на этом сроке мы ещё не можем сказать сколько эмбрионов находится в каждом плодном яйце. Кроме того, во время однократного УЗИ мы ещё не можем сказать, прогрессирует ли данная беременность, так как у эмбриона ещё нет сердцебиения. Средний внутренний диаметр (СВД) плодного яйца на этом сроке 2-10 мм.
В заключении будет указано: Маточная беременность малого срока.
5-6 недель
Фото УЗИ плода при беременности 5-6 недель
На этом сроке внутри плодного яйца появляется белое колечко — это желточный мешок.
В стенке желточного мешка образуются очаги эритропоэза, которые формируют капиллярную сеть, поставляя эритробласты (ядерные эритроциты) в первичную кровеносную систему плода. Желточный мешок является источником первичных половых клеток, которые мигрируют из его стенки к закладкам гонад эмбриона. До 6-й недели после оплодотворения желточный мешок, играя роль «первичной печени», продуцирует многие важные для эмбриона белки — альфа-фетопротеин, трансферрины, альфа2-микроглобулин.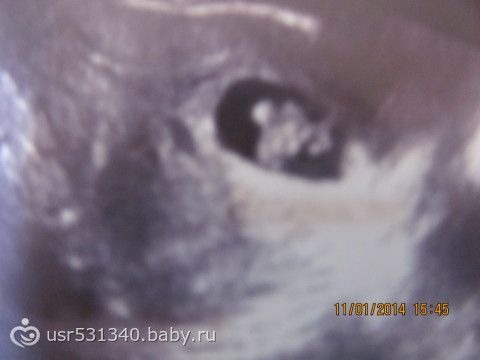 К концу I триместра беременности этот провизорный орган перестает функционировать и редуцируется.
К концу I триместра беременности этот провизорный орган перестает функционировать и редуцируется.
Нормальные размеры желточного мешка 2-6 мм. Если в плодном яйце визуализируются два желточных мешка, значит это монохориальная многоплодная беременность. Но если внутри плодного яйца виден один желточный мешок, а эмбрион ещё отчётливо не визуализируется, то это всё ещё может оказаться монохориальная моноамниотическая двойня.
Эмбрион в начале 5-й недели практически неразличим на стенке желточного мешка, но уже к концу недели копчико-теменной размер (КТР) эмбриона достигает 3 мм.
СВД плодного яйца 11-16 мм.
6 — 7 недель
Фото УЗИ плода при беременности 6-7 недель
Внутри плодного яйца мы видим «колечко с драгоценным камнем» 🙂 — это желточный мешок и уже хорошо различимый эмбрион, расположенные рядом. Сердце эмбриона начинает биться в начале 6-й акушерской недели беременности. Именно наличие пульсации сердца является достоверным ультразвуковым признаком прогрессирующей беременности.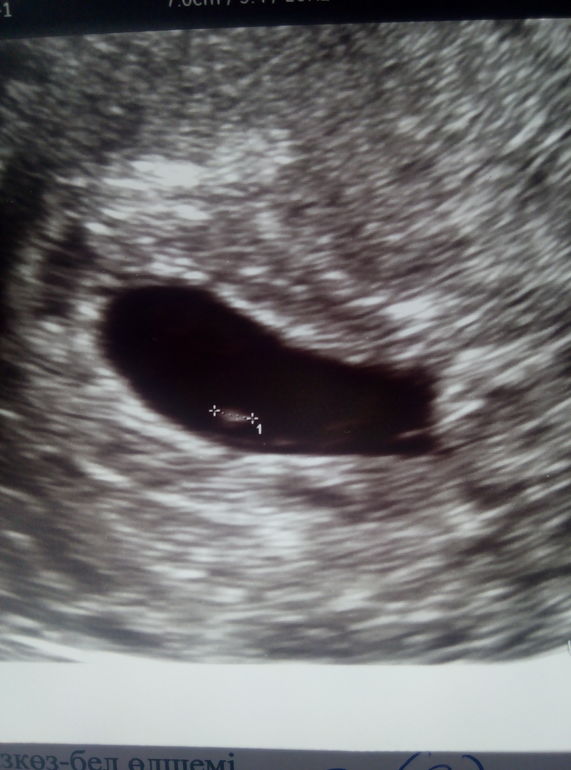 При КТР ≥6 мм и отсутствии пульсации сердца делается заключение об остановке развития данного эмбриона. Нормальная частота сердечных сокращений (ЧСС) эмбриона в самом начале 6-й недели 70-90 ударов в минуту, но уже к концу недели становится более 100 уд. в мин. На ранних сроках беременности большее значение имеет не ЧСС, а как таковое наличие или отсутствие сердечных сокращений. Иногда, при неразвивающейся беременности можно увидеть отражение пульсации сосудов матери внутри эмбриона и принять их за сердцебиение ребёнка. Но в этом случае частота пульсации будет идентична ЧСС матери.
При КТР ≥6 мм и отсутствии пульсации сердца делается заключение об остановке развития данного эмбриона. Нормальная частота сердечных сокращений (ЧСС) эмбриона в самом начале 6-й недели 70-90 ударов в минуту, но уже к концу недели становится более 100 уд. в мин. На ранних сроках беременности большее значение имеет не ЧСС, а как таковое наличие или отсутствие сердечных сокращений. Иногда, при неразвивающейся беременности можно увидеть отражение пульсации сосудов матери внутри эмбриона и принять их за сердцебиение ребёнка. Но в этом случае частота пульсации будет идентична ЧСС матери.
Наличие одного желточного мешка, одного эмбриона и одного пульсирующего сердца в подавляющем большинстве случаев говорит об одноплодной беременности. Но в очень редких случаях это могут в последствии оказаться неразделившиеся близнецы.
СВД плодного яйца 13-23 мм. КТР эмбриона 4-9 мм.
7 — 8 недель
Фото УЗИ плода при беременности 7-8 недель
Расстояние между эмбрионом и желточным мешком постепенно увеличивается и становится хорошо различим желточный проток (ductus vitellinus), соединяющий между собой желточный мешок и кишечник эмбриона. Так же, как и желточный мешок, проток на более поздних сроках запустевает и рассасывается, но если это не происходит по каким-то причинам, то у человека формируется слепое выпячивание стенки подвздошной кишки — дивертикул Меккеля.
Так же, как и желточный мешок, проток на более поздних сроках запустевает и рассасывается, но если это не происходит по каким-то причинам, то у человека формируется слепое выпячивание стенки подвздошной кишки — дивертикул Меккеля.
До этого срока хорион имеет кольцевидную форму, окружает плодное яйцо со всех сторон и пока ещё нельзя сказать к какой стенке матки прикрепился эмбрион.
В случае монохориальной двойни ещё не видно амниотических оболочек и при наличии двух желточных мешков всё ещё нельзя сказать является ли данная беременность моно или диамниотической. Если плодное яйцо содержит два желточных мешка и два плода с наличием сердечной активности, в последующем количество амниотических полостей может быть больше, чем количество плацент (монохориальная диамниотическая) или одинаковым (монохориальная моноамниотическая). В этом случае точно определить амниональность возможно после 8 недель, когда амниотические оболочки начинают четко визуализироваться.
ЧСС эмбриона 130-160 ударов в минуту.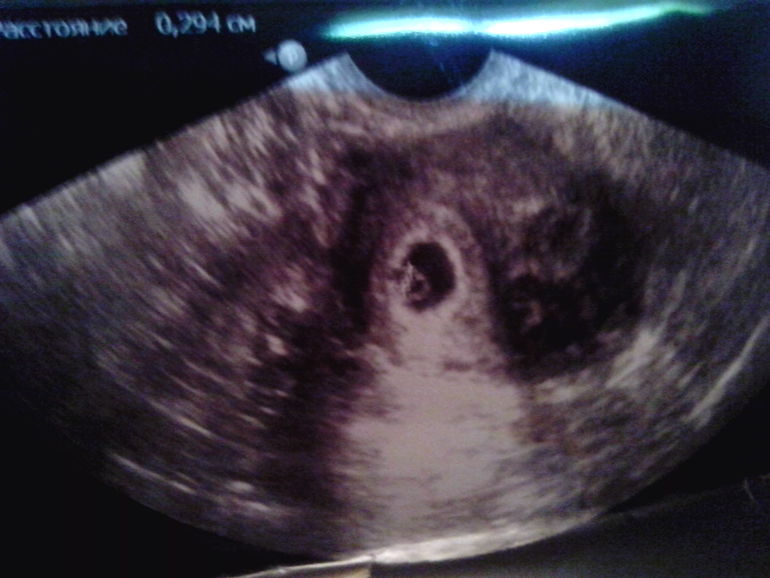
СВД плодного яйца 24-30 мм, КТР эмбриона 9-15 мм.
8 — 9 недель
Во время УЗИ у эмбриона уже можно отчётливо различить отдельные сегменты — голову, туловище, конечности. Появляется первая двигательная активность. Становятся хорошо видны амниотические оболочки и уже можно говорить о количестве амниотических пузырей при многоплодной беременности. Происходит дифференцировка хориона на гладкий, обращённый в сторону полости матки, и ветвистый, из которого впоследствии будет формироваться плацента, так что уже можно говорить о преимущественном расположении хориона по передней или задней стенке матки.
ЧСС эмбриона увеличивается до 160-180 ударов в минуту.
СВД плодного яйца 31-37 мм. КТР эмбриона 16-22 мм.
9 — 10 недель
Фото УЗИ плода при беременности 9-10 недель
Продолжается развитие эмбриона. Уже отчётливо видны ручки ножки, а на хорошем аппарате порой удаётся разглядеть даже пальчики на руках и ногах. Частота сердцебиения на этом сроке достигает 170-190 ударов в минуту.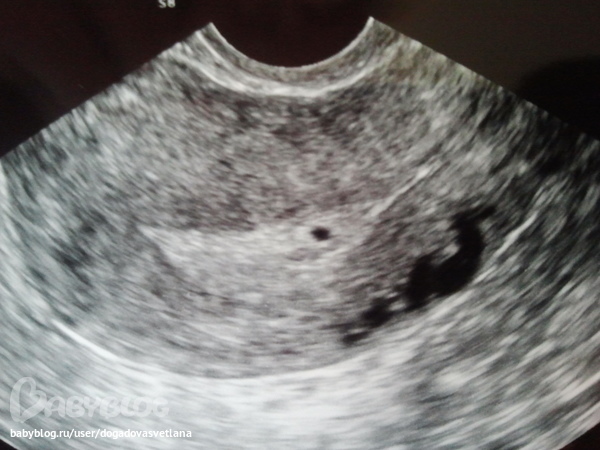 Шевеления эмбриона становятся активными, и есть работы, показывающие, что чем активнее ребёнок, тем длиннее будет пуповина (хотя тут может быть и обратная зависимость).
Шевеления эмбриона становятся активными, и есть работы, показывающие, что чем активнее ребёнок, тем длиннее будет пуповина (хотя тут может быть и обратная зависимость).
Желточный мешок
Желточный мешок — производное эмбриобласта — формируется из эндобластического пузырька в период плацентации на 15—16-й день внутриутробного развития.
Для человека желточный мешок является провизорным органом, который играет немаловажную роль в раннем развитии плодного яйца. На ранних стадиях беременности (до 6 нед) желточный мешок больше амниотической полости вместе с зародышевым диском. С 18—19-го дня после оплодотворения в стенке желточного мешка образуются очаги эритропоэза, которые формируют капиллярную сеть, поставляя эритробласты (ядерные эритроциты) в первичную кровеносную систему плода.
С 28—29-го дня после оплодотворения желточный мешок является источником первичных половых клеток, которые мигрируют из его стенки к закладкам гонад эмбриона. До 6-й нед после оплодотворения желточный мешок, играя роль «первичной печени», продуцирует многие важные для эмбриона белки — альфа-фетопротеин, трансферрины, альфа2-микроглобулин.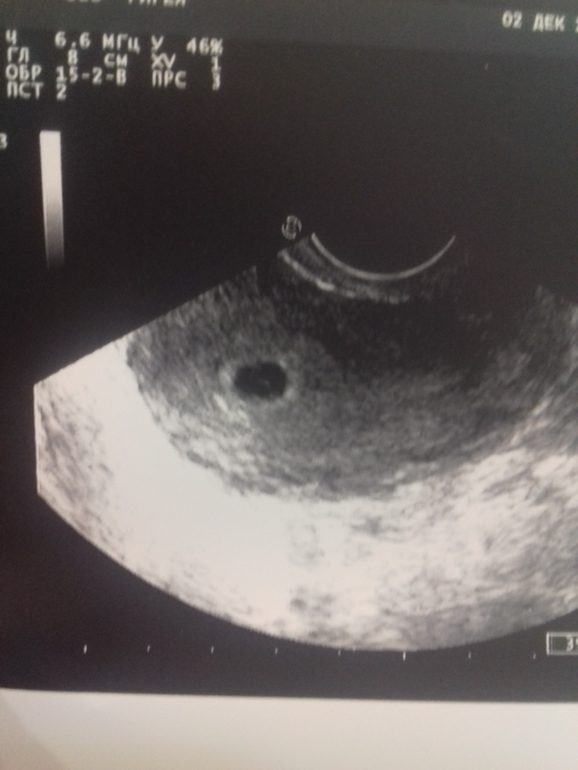
К концу I триместра внутриутробного развития желточный мешок перестает функционировать, редуцируется и остается в виде небольшого кистозного образования у основания пуповины.
Ткани желточного мешка выполняют разнообразные функции (гемопоэтическая, экскреторная, иммунорегуляторная, обменная, синтетическая) до того момента, когда начнут функционировать соответствующие органы плода. Если происходит преждевременная редукция желточного мешка, когда органы плода (печень, селезенка, ретикуло-эндотелиальная система) еще недостаточно сформированы, то исход беременности будет неблагоприятным (самопроизвольный выкидыш, неразвивающаяся беременность).
- Найти и оформить в виде сносок ссылки на авторитетные источники, подтверждающие написанное.
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое «Желточный мешок» в других словарях:
ЖЕЛТОЧНЫЙ МЕШОК — в эмбриологии вырост среднего отдела кишечника у зародышей головоногих моллюсков, большинства позвоночных животных и человека.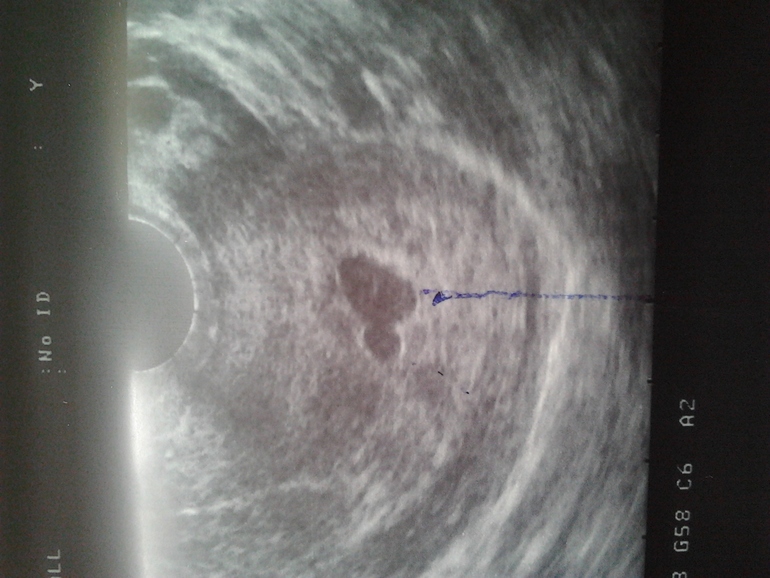 Заполнен желтком и выполняет функцию питания, дыхания и кроветворения … Большой Энциклопедический словарь
Заполнен желтком и выполняет функцию питания, дыхания и кроветворения … Большой Энциклопедический словарь
ЖЕЛТОЧНЫЙ МЕШОК — ЖЕЛТОЧНЫЙ МЕШОК, пленочное образование типа мешочка в ЯЙЦАХ большинства животных. Прикрепляется непосредственно к брюшной стороне или кишке развивающегося зародыша в яйцах птиц, рептилий и некоторых рыб. Содержит ЖЕЛТОК. Термин относится также к… … Научно-технический энциклопедический словарь
желточный мешок — Орган питания, дыхания и кроветворения у зародышей головоногих моллюсков, рыб, пресмыкающихся, птиц и млекопитающих; представляет собой вырост среднего отдела первичной кишки. [Арефьев В.А., Лисовенко Л.А. Англо русский толковый словарь… … Справочник технического переводчика
ЖЕЛТОЧНЫЙ МЕШОК — в первое время после выхода из икры личинка рыбы еще не принимает пищи, поэтому рост ее” а также расход энергии происходят за счет запаса питательных веществ, имеющихся в Ж. м. Величина Ж. м. у разных рыб различна, а поэтому различен и период, в… … Прудовое рыбоводство
желточный мешок — ЭМБРИОЛОГИЯ ЖИВОТНЫХ ЖЕЛТОЧНЫЙ МЕШОК, ЖЕЛТОЧНЫЙ ПУЗЫРЕК — провизорный орган яйцекладущих животных, птиц и млекопитающих, содержащий запас питательных веществ.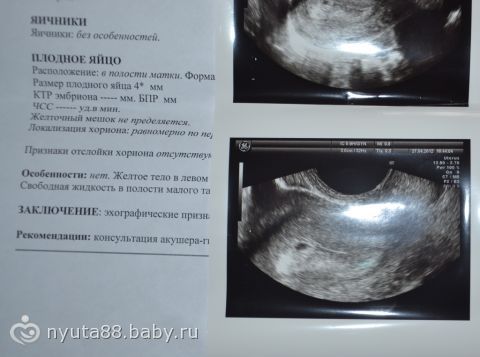 У млекопитающих в составе эмбриобласта в виде пузырька, заполненного серозной жидкостью … Общая эмбриология: Терминологический словарь
У млекопитающих в составе эмбриобласта в виде пузырька, заполненного серозной жидкостью … Общая эмбриология: Терминологический словарь
желточный мешок — (эмбриологич.), вырост среднего отдела кишечника у зародышей головоногих моллюсков, большинства позвоночных животных и человека. Заполнен желтком и выполняет функцию питания, дыхания и кроветворения. * * * ЖЕЛТОЧНЫЙ МЕШОК ЖЕЛТОЧНЫЙ МЕШОК, в… … Энциклопедический словарь
желточный мешок — yolk sac желточный мешок. Oрган питания, дыхания и кроветворения у зародышей головоногих моллюсков, рыб, пресмыкающихся, птиц и млекопитающих; представляет собой вырост среднего отдела первичной кишки. (Источник: «Англо русский толковый словарь… … Молекулярная биология и генетика. Толковый словарь.
желточный мешок — (saccus vitellinus primitivus, LNE; син. желточный пузырь) провизорный орган у зародышей позвоночных, стенка которого образована энтодермой и висцеральной мезодермой; выполняет функцию первичного кроветворения, а также является местом первичной… … Большой медицинский словарь
Желточный мешок — орган питания и дыхания у зародышей головоногих моллюсков, хрящевых и костистых рыб, пресмыкающихся, птиц, млекопитающих и человека.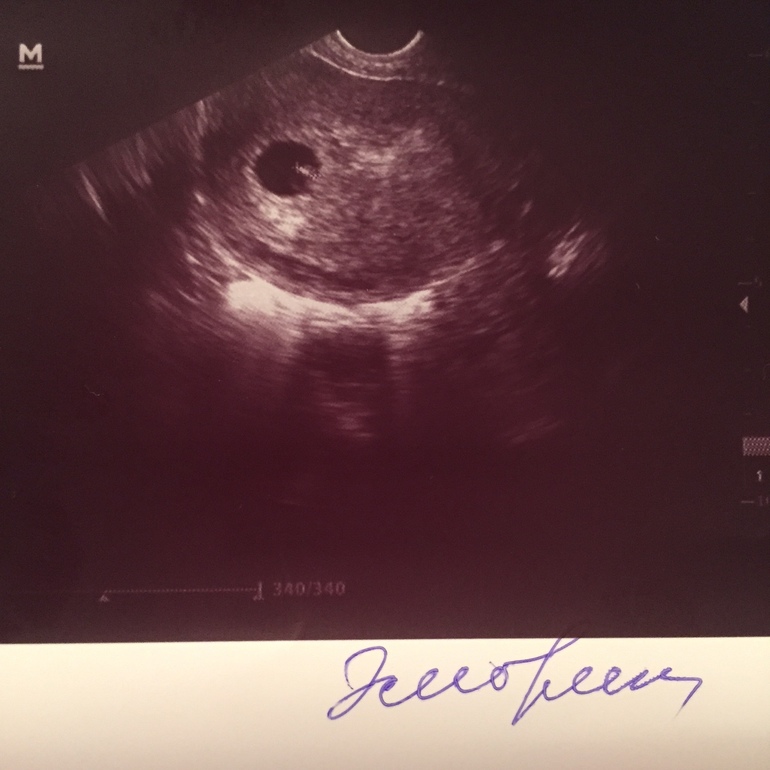 Ж. м. возникает на ранних стадиях зародышевого развития (См. Зародышевое развитие) обычно путём… … Большая советская энциклопедия
Ж. м. возникает на ранних стадиях зародышевого развития (См. Зародышевое развитие) обычно путём… … Большая советская энциклопедия
Трехмерная ультразвуковая реконструкция в I триместре беременности
Эталон новых стандартов! Беспрецедентная четкость, разрешение, сверхбыстрая обработка данных, а также исчерпывающий набор современных ультразвуковых технологий для решения самых сложных задач диагностики.
Введение
Благодаря развитию и совершенствованию технологий, средств диагностики и визуализации, в последние годы возрос интерес специалистов репродуктологии, морфологов и клиницистов к ранним стадиям эмбрионального развития человека. Еще на Всемирном конгрессе по биоэтике (1996) обсуждалась необходимость всестороннего определения статуса эмбриона человека, проблема определения возраста, с которого эмбрион человека можно рассматривать как личность, обладающую правами и защищаемую законодательством, создания соответствующих международных правил для учреждений, работающих в области репродуктивных технологий.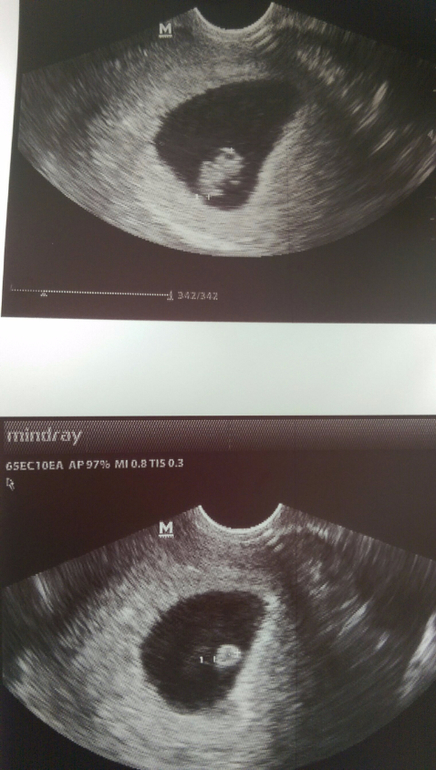 Для практикующего врача, как правило, наибольший интерес представляет возможность клинической оценки течения раннего гестационного периода и возможность прогнозирования осложнений беременности с целью своевременной коррекции и контроля состояния матери и плода.
Для практикующего врача, как правило, наибольший интерес представляет возможность клинической оценки течения раннего гестационного периода и возможность прогнозирования осложнений беременности с целью своевременной коррекции и контроля состояния матери и плода.
Современная эхография дает возможность проследить за развитием плода с самых ранних этапов внутриутробного развития. Появление ультразвуковых аппаратов, позволяющих получить трехмерное изображение исследуемого объекта, в том числе и в режиме «реального времени» расширяет возможности ультразвуковой визуализации. Благодаря трехмерному УЗИ, на ранних сроках беременности можно более точно определить эмбриональный возраст, раньше выявить грубые пороки развития, с высокой степенью точности определять объем исследуемого объекта. Важнейшее условие благоприятного течения беременности и развития плода — становление маточно-плацентарного и плодово-плацентарного кровотока. Морфологические периоды развития плаценты достаточно хорошо изучены и описаны, а применение трехмерных технологий в сочетании с режимом энергетического допплера позволяет оценивать степень развития сосудистой сети органа.
В настоящее время появились единичные работы об использовании трехмерного исследования сосудов фетоплацентарного комплекса [19, 21]. Данных об исследовании кровотока в хорионе в первом триместре беременности в доступной литературе мы не обнаружили. Цель данной работы — демонстрация возможности трехмерного ультразвукового исследования эмбриона, плода и хориона при беременности от 3 до 12 недель.
Материалы и методы
Обследовано 50 здоровых беременных без патологии эмбриона при нормальном течении данной беременности и 110 пациенток с клиническими и ультразвуковыми признаками угрозы прерывания. Определение гестационного срока производилось по дате последней менструации.
До 14-го дня после оплодотворения ведущие эмбриологи мира рассматривают эмбрион человека как проэмбрион, считая, что до этого срока он сформирован клеточными слоями, представляющими собой зародышевые оболочки, материал, не участвующий в построении в дальнейшем собственно эмбриона [1, 2, 6, 12, 13]. На 14-15 день определена ось зародышевого диска, формируется первичная полоска, гензеновский узелок, происходит закладка хорды, т.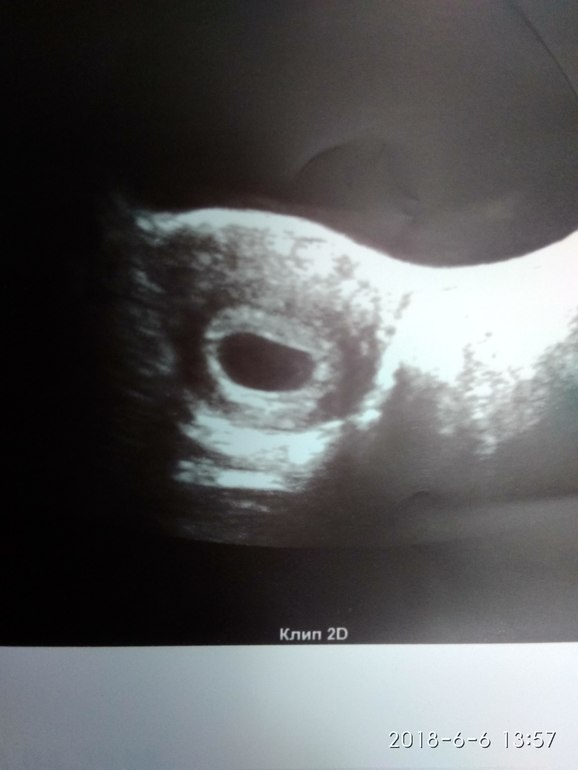 е. это срок начала формирования элементов нервной системы эмбриона человека.
е. это срок начала формирования элементов нервной системы эмбриона человека.
Визуализация эмбриона впервые возможна при трехмерном исследовании плодного яйца сроком не менее 3-4 недель, эмбриональные стадии имплантации визуализировать не удается. Дифференцировать зародыш на трехмерном УЗИ можно на стадии «первичной полоски», начиная с 9-й сомитной стадии [3], когда размер зародыша достигает 1,35 — 1,5 мм (4 недели гестации). На этом этапе можно рассмотреть амниотическую полость, зародыш в виде «рисового зернышка» и прикрепляющий стебелек. Эхографическая дифференциация головного и тазового конца, внутризародышевых структур еще невозможна (рис. 1).
Читайте также:
- Вросший ноготь: причины, симптомы и лечение
- Ранения поджелудочной железы
- Детский церебральный паралич (ДЦП)
- Мупироцин и рифампицин для лечения заболеваний уха, горла, носа
- Диплегия у ребенка. Параплегия и гемиплегия у детей
Особенности тактики ведения при шеечной беременности
Диагноз внематочной беременности с помощью ультразвукового исследования представляет известные трудности.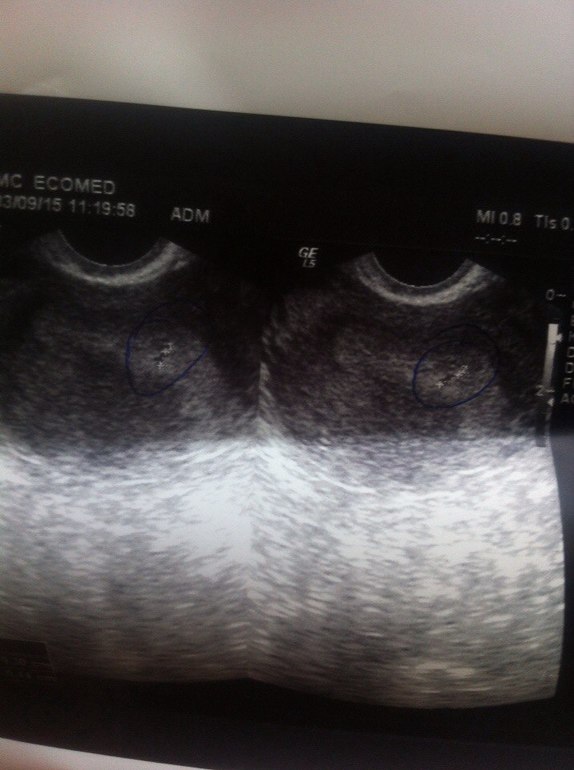
По методу локализации плодного яйца внематочная беременность бывает: трубная, шеечная, яичниковая, брюшная. На долю трубной беременности приходится до 90% случаев. Шеечная и шеечно-перешеечная беременность встречается достаточно редко. Но за последний год я наблюдала три случая шеечной беременности. Ультразвуковая диагностика этой беременности не представляет собой большой трудности. Уникальность этих случаев в том, что пациентам произведена органосохраняющая операция, тем самым сохранена их детородная функция. Как правило, при диагнозе шеечной и шеечно-перешеечной беременности производится оперативное лечение, объем операции лапаротомия тотальная гистерэктомия. В литературе встречаются единичные случаи сохранения матки при шеечной беременности, удаленной путем лазерной вапоризации.
В нашем исследовании под наблюдением находились три пациентки в возрасте 22-26 лет, поступившие по направлению из женской консультации в «Городскую больницу №4» в разное время.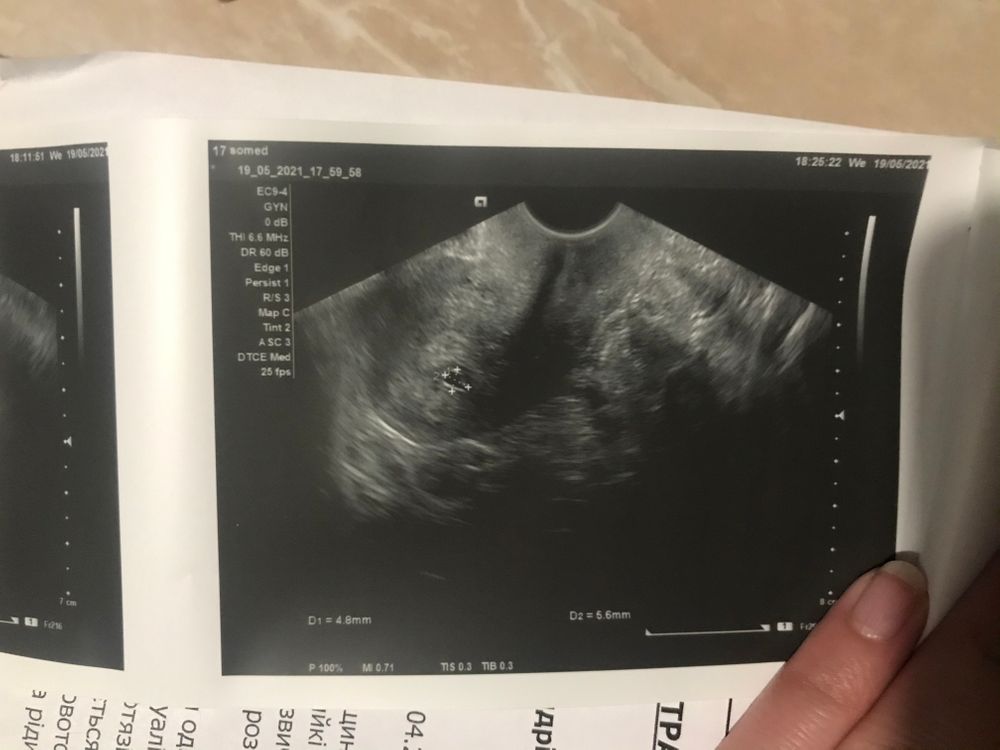 Жалобы на мажущие кровянистые выделения из половых путей и ноющие боли внизу живота на ранних сроках беременности. Пациентка Б. — хотела прервать беременность; пациентки В. и П. – сохранить. Ультразвуковое исследование осуществлено на аппарате (Philips) HDI – 1500 c использованием трансабдоминального и трансвагинального трансдьюсеров 3,5 и 5 MГц.
Жалобы на мажущие кровянистые выделения из половых путей и ноющие боли внизу живота на ранних сроках беременности. Пациентка Б. — хотела прервать беременность; пациентки В. и П. – сохранить. Ультразвуковое исследование осуществлено на аппарате (Philips) HDI – 1500 c использованием трансабдоминального и трансвагинального трансдьюсеров 3,5 и 5 MГц.
В ходе эхографического исследования пациентки Б., установлено, что тело матки нормальных размеров, миометрий с однородной структурой; эндометрий 8 мм однородный, повышенной эхогенности. Шейка матки обычных размеров, по передней стенке, ближе к внутреннему зеву визуализируется плодное яйцо в Ø 10 мм, с эмбрионом (КТР-4мм; СБ+), желточный мешок Ø 1,8 см, что соответствует 5-6 неделям беременности. Справа в яичнике желтое тело Ø 22мм. В режиме ЦДК вокруг плодного яйца хорошо выражен кровоток JR-0,58. Незаинтересованный участок шейки матки до серозного слоя 4 мм.
При эхографическом исследовании пациентки В., матка несколько больше нормы, миометрий не изменен, эндометрий 7,5 мм повышенной эхогенности.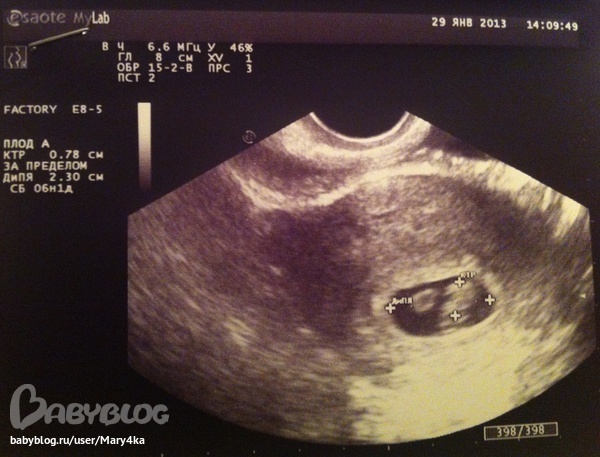 Шейка матки утолщена в среднем отделе. По передней стене в среднем отделе визуализируется плодное яйцо в Ø 14мм. С эмбрионом (КТР-4мм; СБ+), желточный мешок Ø 22мм – на 6 недель беременности.
Шейка матки утолщена в среднем отделе. По передней стене в среднем отделе визуализируется плодное яйцо в Ø 14мм. С эмбрионом (КТР-4мм; СБ+), желточный мешок Ø 22мм – на 6 недель беременности.
В режиме ЦДК – хорошо выражен кровоток в проекции плодного яйца. JR-0,52. Неизмененный участок шейки матки до наружного слоя 4 мм.
При эхографическом исследовании пациентки П., матка увеличена до 6-7 недель беременности, миометрий не изменен, эндометрий 9 мм, с участками десквамации. Шейка матки утолщена в шеечно-перешеечном отделе; там же по задней стенке визуализируется плодное яйцо Ø 16 мм на 6-7 недель беременности. Виден эмбрион без сердечной деятельности (КТР-8 мм).
В режиме ЦДК выражен кровоток вокруг плодного яйца, JR-0,6. Неизмененный участок шейки до наружного слоя 1-2 мм.
Во всех трех случаях, учитывая анамнез, жалобы, лабораторные данные, результаты ультразвукового исследования, а так же гинекологический осмотр — консилиумом принято решение консервативного ведения пациенток.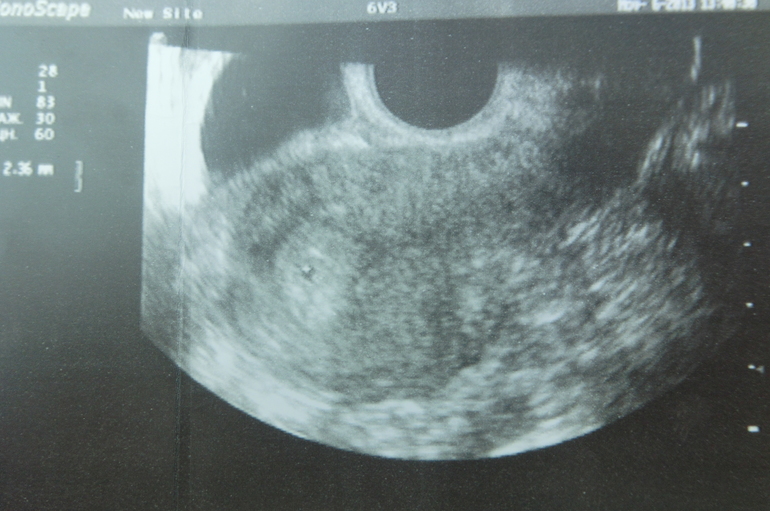 Контроль за больными осуществлялся круглосуточно.
Контроль за больными осуществлялся круглосуточно.
Новая тактика ведения заключается в химиотерапии метотрексатом (по схеме) под контролем лабораторных данных и мониторинга ультразвукового исследования, с последующим выскабливанием полости матки и цервикального канала. Для профилактики кровотечения перед выскабливанием прошивались влагалищные ветви маточной артерии.
Мониторинг ультразвуком проводился через 3-5 дней после начала лечения. Под действием метотрексата сердечная деятельность эмбрионов останавливалась, васкуляризация вокруг плодного яйца снижалась JR-0.58; 06; 0,62. Регрессия беременности так же контролировалась снижением цифр хорионического гонадотропина в крови.
После выскабливания полости матки через 3-4 дня проводилось контрольное эхографическое исследование.
У пациенток Б. и В. в месте локализации плодного яйца – участки неоднородной структуры без деформации анатомических линий шейки матки.
У пациентки П., при шеечно-перешеечной беременности (и большем сроке беременности) в проекции ранее находившегося плодного яйца – определялось ложе 18х16мм с неоднородным содержанием, в режиме ЦДК – аваскулярно.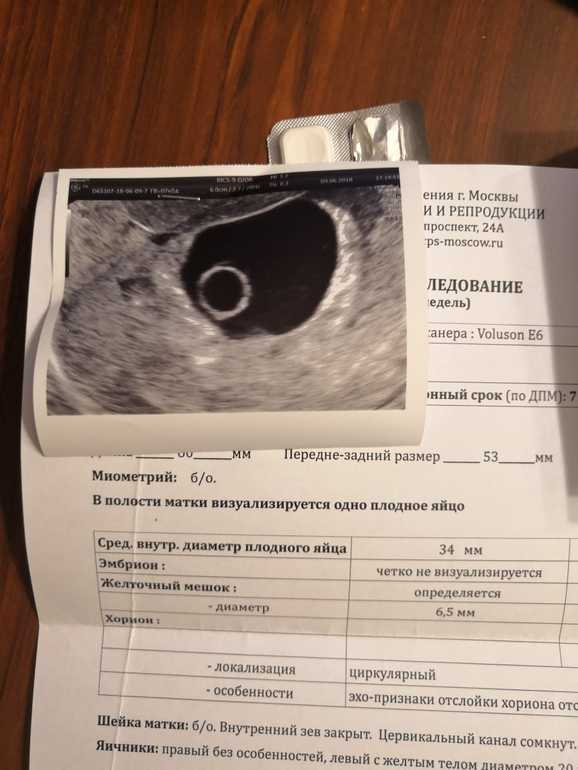
Органосохраняющие операции при шеечной беременности возможны в ранних сроках беременности. А диагностика их возможна только с помощью эхографии, которая дает врачу гинекологу всю необходимую информацию о сроке беременности, ее состоянии, локализации, кровоснабжении. Осмотр в динамике помогает определить дальнейшую тактику ведения пациентки.
ЛИТЕРАТУРА
Михельсон А.Ф., Волков А.Е. Клиническое значение ранней ультразвуковой диагностики шеечной беременности. Ультразвуковая диагностика акуш.
Иванова В.С., Егорова Ж.К. Эхографическая картина шеечно-перешеечной беременности. Ультразвуковая диагностика акуш.гинек.педит. – 1996. – сс.20-22.
Старостина Т.А., Липман А.Д. Шеечная беременность. Ультразвуковая диагностика акуш.гинек.педит. – 1997. — №2. – сс.38-42.
Белозерова Т.А., Семятов С.Д. Ультразвуковая диагностика внематочной беременности. Ультразвуковая диагностика. –1997-.№4 – сс.7-10.
Лейтис Н.А., Пак Н.В., Климатова Е.И.,
МБУЗ «Городская клиническая больница №4»
CDC — DPDx — Энтеробиоз
Возбудитель
Нематода (аскарида) Enterobius vermicularis широко известна как человеческая острица из-за длинного заостренного хвоста самки. В некоторых районах используются общие названия «морской червь» и «острица» (последнее из которых иногда также используется для обозначения Strongyloides stercoralis ) .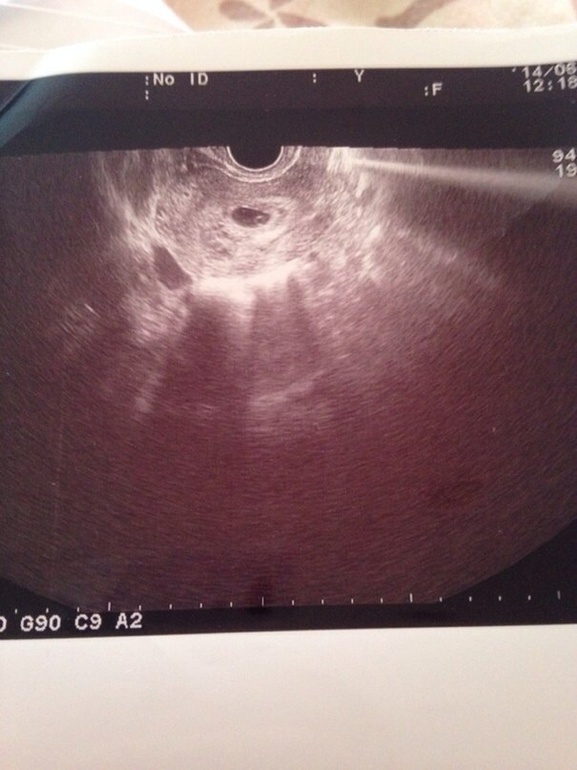 Другой предполагаемый вид остриц, Enterobius gregorii , был описан и зарегистрирован у людей в Европе, Африке и Азии. Однако дальнейшие морфологические и молекулярные данные свидетельствуют о том, что E. gregorii , вероятно, представляет собой незрелую форму E. vermicularis. Крысиная острица Syphacia obvelata также очень редко заражает людей.
Другой предполагаемый вид остриц, Enterobius gregorii , был описан и зарегистрирован у людей в Европе, Африке и Азии. Однако дальнейшие морфологические и молекулярные данные свидетельствуют о том, что E. gregorii , вероятно, представляет собой незрелую форму E. vermicularis. Крысиная острица Syphacia obvelata также очень редко заражает людей.
Жизненный цикл
Беременная взрослая самка Enterobius vermicularis откладывает яйца на перианальных складках. Заражение происходит путем самоинокуляции (попадание яиц в рот руками, оцарапанными в перианальной области) или при попадании яиц в окружающую среду (например, на загрязненные поверхности, одежду, постельное белье и т. д.). После проглатывания инфекционных яиц личинки вылупляются в тонкой кишке, а взрослые особи поселяются в толстой кишке, обычно в слепой кишке. Интервал времени от проглатывания инвазионных яиц до откладывания яиц взрослыми самками составляет около одного месяца.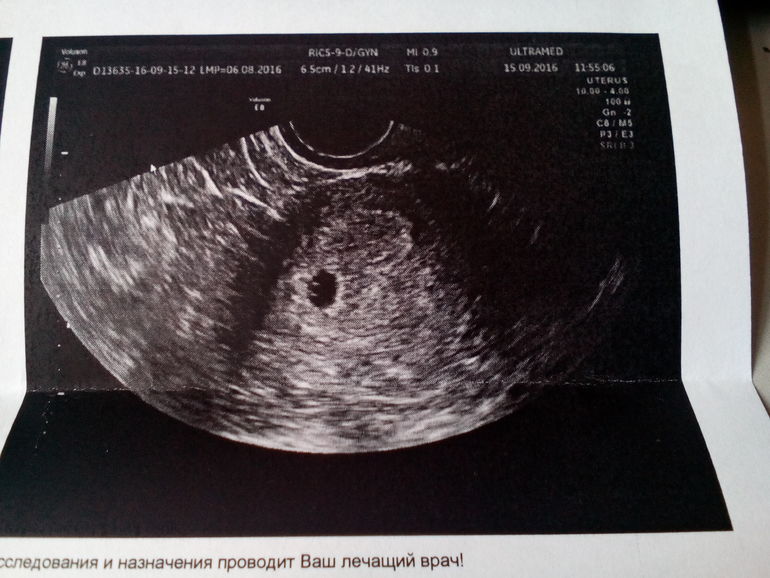 В период полной зрелости взрослые самки имеют размеры от 8 до 13 мм, а взрослые самцы от 2 до 5 мм; продолжительность взрослой жизни составляет около двух месяцев. Беременные самки мигрируют ночью вне ануса и откладывают яйца, ползая по коже перианальной области. Личинки, содержащиеся внутри яиц, развиваются (яйца становятся заразными) в течение 4–6 часов при оптимальных условиях.
В период полной зрелости взрослые самки имеют размеры от 8 до 13 мм, а взрослые самцы от 2 до 5 мм; продолжительность взрослой жизни составляет около двух месяцев. Беременные самки мигрируют ночью вне ануса и откладывают яйца, ползая по коже перианальной области. Личинки, содержащиеся внутри яиц, развиваются (яйца становятся заразными) в течение 4–6 часов при оптимальных условиях.
В редких случаях яйца могут переноситься по воздуху, вдыхаться и проглатываться. Может произойти ретроинфекция или миграция только что вылупившихся личинок из кожи анального отверстия обратно в прямую кишку, но частота, с которой это происходит, неизвестна.
Хозяева
Оксиуридовые нематоды (острицы) обычно обладают высокой специфичностью к хозяину. Люди считаются единственным хозяином для E. vermicularis, , хотя иногда сообщалось о случаях заражения шимпанзе, содержащихся в неволе .
Географическое распространение
E. vermicularis встречается во всем мире, при этом инфекции чаще всего возникают у детей школьного или дошкольного возраста и в условиях скопления людей.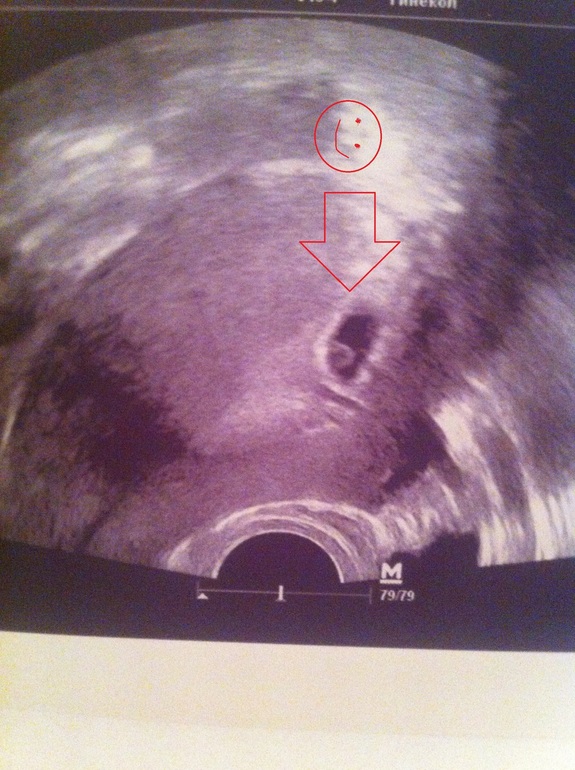
Клиническая картина
Энтеробиоз часто протекает бессимптомно. Наиболее типичным симптомом является перианальный зуд, особенно ночью, который может привести к экскориациям и бактериальной суперинфекции. Иногда может возникать инвазия женских половых путей с вульвовагинитом и тазовыми или перитонеальными гранулемами. Другие симптомы включают скрежетание зубами, энурез, бессонницу, анорексию, раздражительность и боль в животе, которые могут имитировать аппендицит. 9Личинки 0005 E. vermicularis часто обнаруживаются в аппендиксе после аппендэктомии, но роль этой нематоды в развитии аппендицита остается спорной. Сообщалось об очень редких случаях эозинофильного колита, связанного с личинками E. vermicularis .
Enterobius vermicularis яиц.
Яйца Enterobius vermicularis имеют размеры 50—60 мкм на 20—30 мкм. Они прозрачные, имеют удлиненно-овальную форму и слегка уплощены с одной стороны.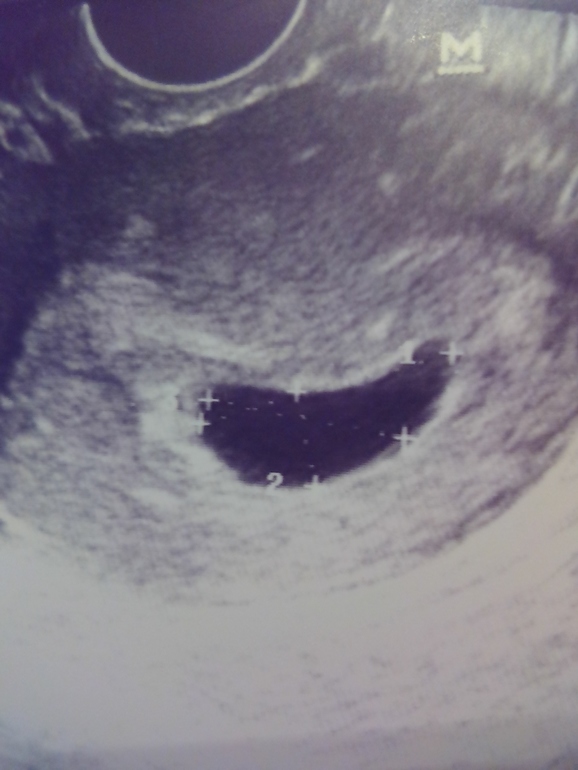 Они обычно частично зарождаются при линьке. Энтеробиоз можно диагностировать, накладывая целлюлозную ленту на анус подозрительного пациента, особенно утром перед первой дефекацией пациента. Яйца будут прилипать к ленте и их можно будет увидеть под микроскопом.
Они обычно частично зарождаются при линьке. Энтеробиоз можно диагностировать, накладывая целлюлозную ленту на анус подозрительного пациента, особенно утром перед первой дефекацией пациента. Яйца будут прилипать к ленте и их можно будет увидеть под микроскопом.
Рисунок A: Яйца E. vermicularis в препарате из целлюлозной ленты.
Рисунок B: Яйца E. vermicularis во влажном препарате.
Рисунок C: Яйцо E. vermicularis в окрашенном йодом влажном препарате из формалинового концентрата. Изображение предоставлено Лабораторией общественного здравоохранения штата Канзас.
Рисунок D: Яйцо E. vermicularis , полученное из взрослого червя, извлеченного при колоноскопии. Изображение предоставлено Бюро лабораторий Департамента здравоохранения и контроля окружающей среды Южной Каролины.
Рисунок E: Яйца E. vermicularis под УФ-микроскопом.
Рисунок F: Яйца E. vermicularis под УФ-микроскопом.
Enterobius vermicularis взрослых червей.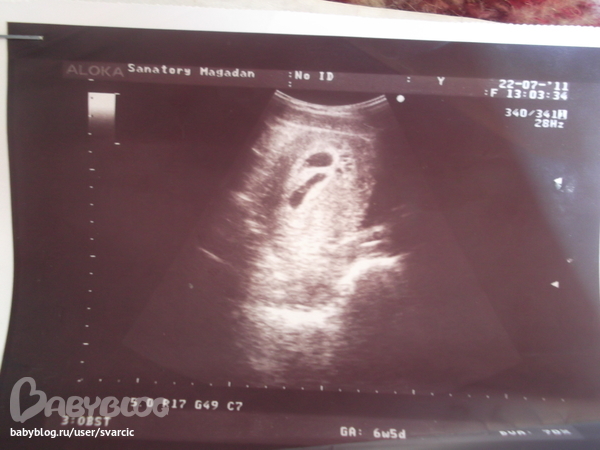
Взрослые самцы Enterobius vermicularis имеют длину до 2,5 мм и ширину 0,1–0,2 мм; взрослые самки имеют длину 8-13 мм и ширину 0,3-0,5 мм. У взрослых самцов задний конец тупой с одной спикулой; самки обладают длинным заостренным хвостом. У обоих полов имеются головные расширения.
Рисунок A: Взрослый самец E. vermicularis из мазка концентрированного формалин-этилацетата (ФЭА). Червь имел длину 1,4 мм. Изображение предоставлено Центром тропической медицины и завозных инфекционных заболеваний, Берген, Норвегия.
Рисунок B: Крупный план переднего конца червя на рисунке A. На изображении виден пищевод, разделенный на мышечную и луковичную части и разделенный коротким узким перешейком, а также головные расширения.
Рисунок C: Крупный план заднего конца червя на рисунке A. Обратите внимание на тупой конец. У этого экземпляра спикула втягивается в червя.
Рисунок D: Взрослая самка E. vermicularis , окруженная многочисленными яйцами.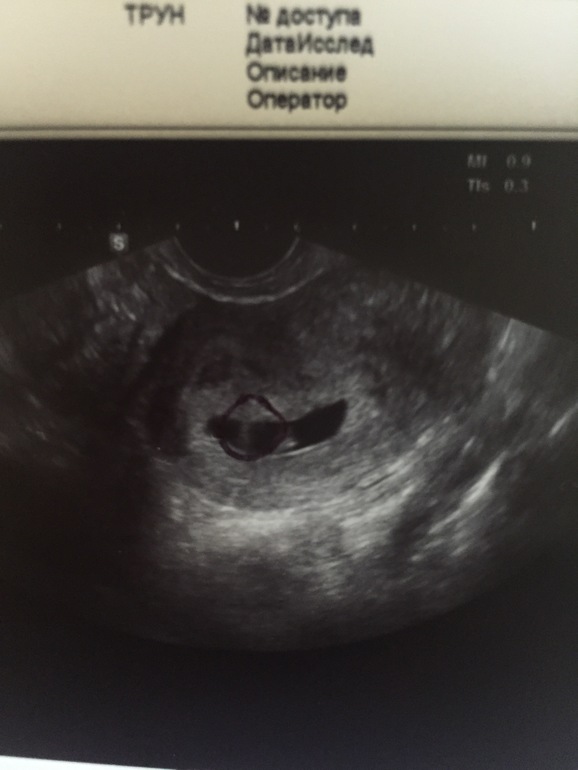
Рисунок E: Самец и самка E. vermicularis , смонтированные образцы.
Рисунок F: Задний конец самки E. vermicularis с длинным, тонким, заостренным хвостом.
Enterobius vermicularis в ткани, окрашенной гематоксилином и эозином (ГЭ)
Взрослые самцы Enterobius vermicularis имеют длину до 2,5 мм и ширину 0,1—0,2 мм; взрослые самки имеют длину 8—13 мм и ширину 0,3—0,5 мм. У взрослых самцов задний конец тупой с одной спикулой; самки обладают длинным заостренным хвостом. У обоих полов имеются головные расширения.
Рисунок A: Поперечное сечение ткани самца E. vermicularis , окрашенной H&E. Обратите внимание на наличие крыльев (синяя стрелка), кишечника (красная стрелка) и семенников (черная стрелка).
Рисунок B: Поперечное сечение взрослой самки E. vermicularis из того же образца, что и на рисунке A. Обратите внимание на наличие крыльев (синяя стрелка), кишечника (зеленая стрелка) и яичников (черные стрелки).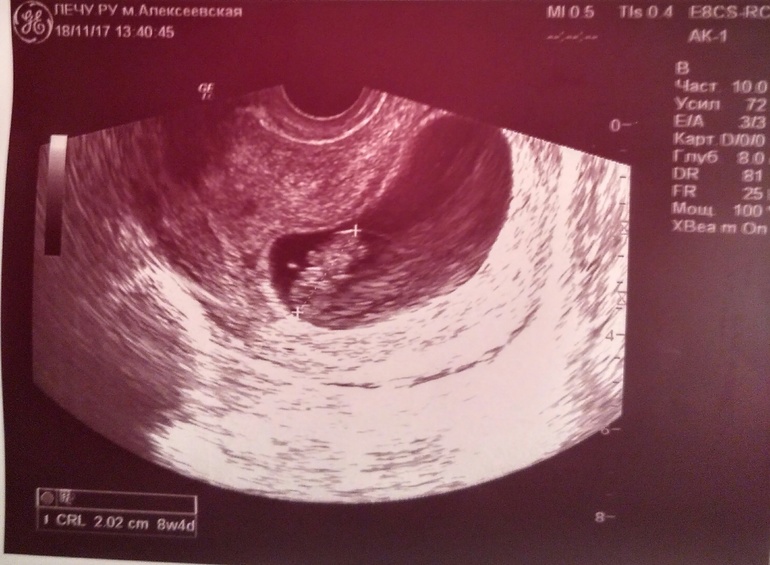
Рисунок C: Поперечный срез взрослой самки E. vermicularis , окрашенный гематоксилин-эозином, полученный во время колоноскопии. Обратите внимание на выступающие крылья (синяя стрелка) и наличие яиц (желтая стрелка). Изображение предоставлено Мемориальной больницей Шебойган, Висконсин.
Рисунок D: Продольный срез взрослой самки E. vermicularis из того же образца, что и на рисунке C. Обратите внимание на наличие большого количества яиц.
Рисунок E: Яйцо E. vermicularis в образце биопсии толстой кишки, окрашенное H&E.
Рисунок F: Яйцо E. vermicularis в образце биопсии толстой кишки, окрашенное H&E.
Лабораторная диагностика
Микроскопическая идентификация яиц, собранных в перианальной области, является методом выбора для диагностики энтеробиоза. Для улучшения чувствительности сбор следует проводить утром, перед дефекацией и умыванием, прижимая прозрачную целлюлозную ленту («Скотч-тест», тест на предметном стекле целлюлозной лентой) к перианальной коже и затем исследуя ленту, помещенную на предметное стекло микроскопа. В качестве альтернативы для сбора также можно использовать анальные тампоны или «пробирки Swube» (пластинки, покрытые клеящимся материалом). Яйца также можно обнаружить, но реже, в кале, а иногда и в моче или вагинальных мазках. Взрослые черви также являются диагностическими признаками, если их обнаруживают в перианальной области, во время аноректального или вагинального исследования. В случаях эктопической инфекции яйца можно увидеть в моче или в мазках Папаниколау из шейки матки.
В качестве альтернативы для сбора также можно использовать анальные тампоны или «пробирки Swube» (пластинки, покрытые клеящимся материалом). Яйца также можно обнаружить, но реже, в кале, а иногда и в моче или вагинальных мазках. Взрослые черви также являются диагностическими признаками, если их обнаруживают в перианальной области, во время аноректального или вагинального исследования. В случаях эктопической инфекции яйца можно увидеть в моче или в мазках Папаниколау из шейки матки.
Подробнее: Морфологическое сравнение с другими кишечными паразитами.
Лабораторная безопасность
Стандартные меры предосторожности применяются при обработке образцов стула (также образцов для анализа с помощью ленты), чтобы избежать случайного проглатывания инфицированных яиц. Поверхности должны быть тщательно очищены, так как внешняя оболочка яиц E. vermicularis является липкой.
Рекомендуемая литература
Peixoto, A., Goncalves, R., Silva, M., Gaspar, R. , Silva, R., Portugal, R. and Macedo, G., 2016. Эозинофильный илеоколит, вызванный 9Инфекция 0005 Enterobius vermicularis : редкая причина анемии. Международный журнал колоректальных заболеваний , 31(3), стр. 743-743.
, Silva, R., Portugal, R. and Macedo, G., 2016. Эозинофильный илеоколит, вызванный 9Инфекция 0005 Enterobius vermicularis : редкая причина анемии. Международный журнал колоректальных заболеваний , 31(3), стр. 743-743.
Hasegawa, H., Takao, Y., Nakao, M., Fukuma, T., Tsuruta, O. and Ide, K., 1998. Является ли Enterobius gregorii Hugot, 1983 (Nematoda: Oxyuridae) отдельным видом ? Журнал паразитологии 84, стр. 131-134.
Кук, Г.К. 1994. Инфекция Enterobius vermicularis . Гут . 35, стр. 1159-62.
Отказ имплантации при ЭКО — почему это происходит?
» Мой врач сказал, что мои эмбрионы выглядели идеально, но им не удалось имплантироваться — почему это произошло ?»
Этот вопрос волнует женщин, перенесших неудачное ЭКО, и это становится особенно мучительным сомнением, когда они сталкиваются с многочисленными неудачами ЭКО. Многие женщины, естественно, думают, что их матка дефектна или что их тело недостаточно хорошо для того, чтобы принять эмбрион, что их матка отторгает перенесенный эмбрион или что их собственное тело убивает его. Ведь оплодотворение произошло в лаборатории, эмбрион хорошо вырос в пробирке, и они даже видели свой эмбрион (помните, что перед переносом эмбрионов вы всегда должны видеть свои эмбрионы и просить фото!).
Ведь оплодотворение произошло в лаборатории, эмбрион хорошо вырос в пробирке, и они даже видели свой эмбрион (помните, что перед переносом эмбрионов вы всегда должны видеть свои эмбрионы и просить фото!).
Эмбриолог заверил их, что они выглядят идеально, и они читали множество историй успеха женщин, которые забеременели такими хорошими эмбрионами. В результате они естественным образом приходят к выводу, что хорошие эмбрионы предназначены для имплантации, а если они этого не сделали, то это явно означает, что у них проблемы с маткой или с их телом.
Это не твоя вина
Знакомо? Низкая самооценка, вызванная бесплодием, позволяет вам легко сделать такой вывод и винить себя. Плохая ситуация часто усугубляется тем, что родственники говорят вам, что эмбрион, должно быть, «выпал» из-за того, что вы недостаточно отдыхали; или что цикл не удался, потому что вы слишком напряжены или у вас слишком много «тепла тела». Вот почему многие женщины, у которых повторяется неудачная имплантация, выбирают суррогатное материнство.
Эта статья была написана, чтобы помочь вам понять, что вызывает повторную неудачу имплантации (действительно ли известна причина? и что является виновником – семя (эмбрион) или почва (матка)?
Что такое неудача имплантации при ЭКО?
Когда яйцеклетка и сперматозоид соединяются вместе, формируется эмбрион (это происходит в маточной трубе вашего тела, а в лаборатории ЭКО это происходит в чашке Петри, содержащей питательную культуральную среду). быстро и достигает матки на стадии бластоцисты (или переносится в матку на 3-й или 5-й день во время цикла ЭКО) 9.0019
Находясь в матке, бластоциста начинает сообщаться с эндометрием (слизистой оболочкой матки), секретируя белковые молекулы. Если эмбрион достаточно дееспособен и если эндометрий восприимчив, это приводит к имплантации. Имплантация — это прикрепление эмбриона на стадии бластоцисты к слизистой оболочке матки, чтобы он в дальнейшем превратился в ребенка (представьте, что семя посажено в почву).
Когда женщина подвергается трем или более неудачным попыткам ЭКО (с эмбрионами хорошего качества) или если имплантация не происходит даже после переноса более 10 «красивых» эмбрионов в течение многих циклов, то говорят, что у женщины «имплантация отказ».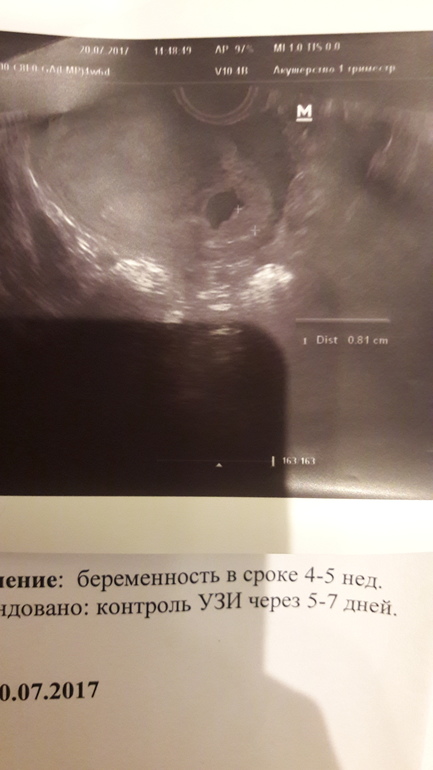 Когда эмбрион не имплантируется, может быть только две логические причины: эмбрион недостаточно хорош (генетически аномален) или эндометрий недостаточно «рецептивен» (не позволяет эмбриону имплантироваться). Итак, что на самом деле вызывает неудачу имплантации? Пожалуйста, продолжайте читать!
Когда эмбрион не имплантируется, может быть только две логические причины: эмбрион недостаточно хорош (генетически аномален) или эндометрий недостаточно «рецептивен» (не позволяет эмбриону имплантироваться). Итак, что на самом деле вызывает неудачу имплантации? Пожалуйста, продолжайте читать!
Кто виноват – семена или почва?
Представьте себе фермера, который владеет участком земли и хочет выращивать рис. Он пашет и обрабатывает землю, подготавливая ее к посеву, находит подходящий сезон и тщательно отбирает семена.
Это аналогично тому, как врач ЭКО готовит женщину к прохождению цикла ЭКО. Он делает инъекции гормонов, чтобы яйцеклетки собирались и оплодотворялись спермой ее партнера для образования эмбрионов (семян). Гормоны (эстроген и прогестерон) также используются для подготовки матки к принятию эмбриона (точно так же, как вспашка земли, внесение удобрений и т. д.). Женщина должна быть в добром здравии (аналогично ожиданию подходящего сезона для посева семян).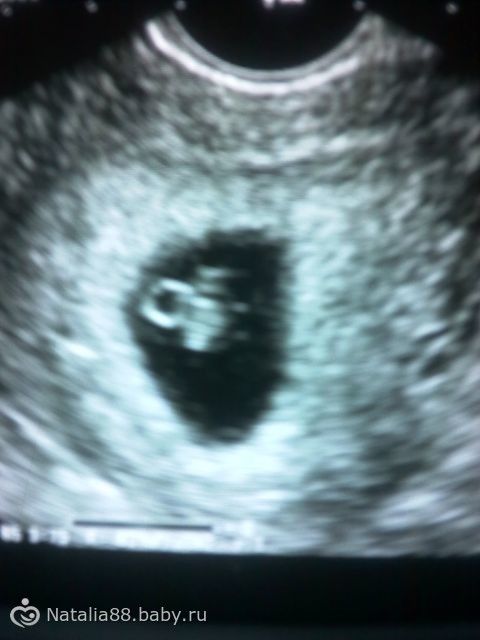
Когда фермер заботится обо всем этом и сеет семена, он ожидает, что семена прорастут и вырастут. Но что происходит, когда семена не прорастают? Это происходит по трем основным причинам:
- Низкое качество семян (эмбрионов)
- Неплодородная почва (матка)
- Недостаточно благоприятная среда (физическое здоровье будущей матери)
В редких случаях к дополнительным факторам, препятствующим росту, относятся неправильный посев (трудный или травматичный перенос эмбрионов) или внезапное изменение окружающей среды (например, инфекция в матке).
Как качество эмбриона влияет на успешную имплантацию?
Хорошо известно, что молодые женщины беременеют быстрее, чем их сверстницы старшего возраста. Это связано с тем, что яйцеклетки от пожилых женщин более склонны к генетическим дефектам, таким как анеуплоидия (наличие неправильного числа хромосом), и содержат неправильную или недостаточную генетическую информацию, необходимую для построения здорового ребенка.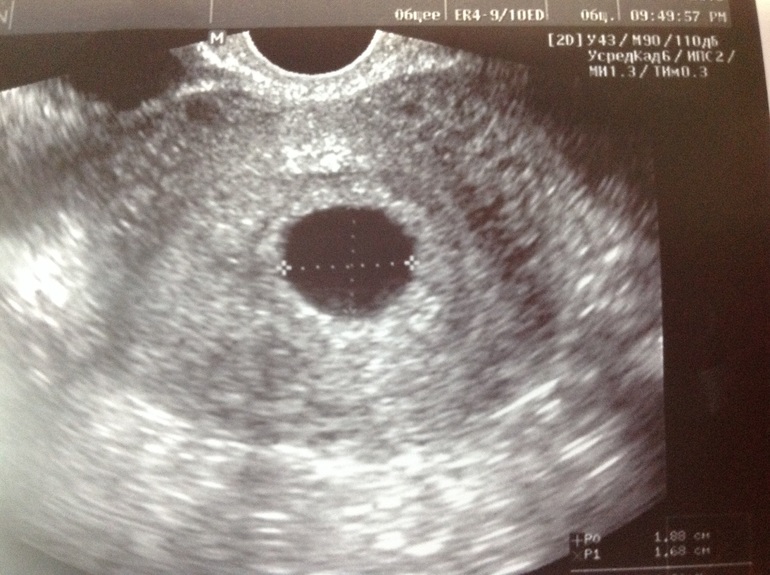
Оплодотворение таких яйцеклеток приводит к образованию генетически некомпетентных эмбрионов. Либо такие эмбрионы не приживаются, а даже если и приживаются, то беременность заканчивается выкидышем на раннем сроке. В редких случаях они также могут привести к доношенным родам, когда у новорожденного есть генетические дефекты.
С появлением комплексного хромосомного скрининга стало возможным исследовать все 24 хромосомы (22 аутосомы и 2 половые хромосомы) на наличие анеуплоидии (хотя эффективность такого метода для увеличения числа живорождений с помощью ВРТ в клинической практике до сих пор не доказано). Одно такое исследование с использованием CGH показало, что 96% анеуплоидных эмбрионов не смогли имплантироваться.
Это ясно показывает, что компетентность эмбриона играет важную роль в имплантации. Вот почему пожилым женщинам требуется больше попыток, чем их более молодым коллегам, чтобы добиться успеха в ЭКО. Когда пожилая женщина использует донорские яйцеклетки, ее шансы на успех ЭКО резко возрастают! Это неопровержимое доказательство того, что именно качество эмбриона играет главную роль в имплантации и успехе ЭКО.
Роль эндометрия в имплантации эмбриона
Важность качества почвы в сельском хозяйстве хорошо известна. Играет ли эндометрий столь важную роль в имплантации эмбриона? Что происходит, когда плодородное семя (генетически компетентный зародыш) высеивается на дефектную почву (невосприимчивый эндометрий)?
Период, в течение которого матка способна принять эмбрион (бластоцисту), называется «окном имплантации». Человеческая матка восприимчива только в течение короткого периода времени, известного как «маточная восприимчивость». У людей период восприимчивости длится с 20 по 24 день регулярного менструального цикла, т. е. через 7–11 дней после всплеска ЛГ, вызывающего овуляцию. (С помощью этого простого в использовании календаря фертильности вы можете рассчитать лучшее время для беременности.)
При ЭКО эмбрионы переносят в матку либо на 3-й день (перенос эмбрионов), либо на 5-й день (перенос бластоцисты) после забора яйцеклеток (день овуляции), что совпадает с «окном имплантации» естественного менструального цикла. При переносе замороженных эмбрионов день начала введения прогестерона принимается за первый день овуляции, и перенос эмбрионов осуществляется соответствующим образом.
При переносе замороженных эмбрионов день начала введения прогестерона принимается за первый день овуляции, и перенос эмбрионов осуществляется соответствующим образом.
Мы до сих пор не до конца понимаем имплантацию
Имплантация человеческого эмбриона — загадочный биологический феномен. В конце концов, эксперименты in vivo проводить нецелесообразно и неэтично; а исследования на животных моделях плохо переносятся на людей. Но общеизвестно, что эмбрион и эндометрий разговаривают друг с другом с помощью молекулярных сигналов, и такие перекрестные разговоры необходимы для успешной имплантации. Однако надежных молекулярных маркеров рецептивности эндометрия не выявлено. Это затрудняет определение восприимчивости эндометрия во время цикла ЭКО.
Во время ЭКО рецептивность эндометрия оценивается грубо с помощью ультразвуковых изображений. Толщина эндометрия измеряется с помощью ультразвуковых изображений, и эндометрий более 8 мм, который является трехслойным, считается оптимальным для переноса эмбриона.
Общеизвестно, что эндометрий становится восприимчивым только после воздействия прогестерона. Прогестерон вызывает необходимые изменения в эндометрии (превращает эндометрий из пролиферативной в секреторную фазу), чтобы он был готов принять эмбрион. В последнее время перенос замороженных эмбрионов становится гораздо более успешным, чем перенос свежих эмбрионов в области ЭКО. Предполагается, что высокая концентрация эстрогенов в организме во время свежего цикла ЭКО ставит под угрозу рецептивность эндометрия.
Почему у меня может быть «невосприимчивая» матка?
- Если в полости матки имеются спайки, полипы или миомы, то ее рецептивность будет нарушена.
- Если во время цикла ЭКО происходит преждевременное повышение уровня прогестерона (то есть повышение уровня прогестерона перед сбором яйцеклеток из-за преждевременной лютеинизации фолликулов), то восприимчивость матки не синхронизируется со временем переноса эмбрионов. Это может привести к неудачной имплантации.
 Эту проблему можно решить тщательным контролем цикла ЭКО.
Эту проблему можно решить тщательным контролем цикла ЭКО. - Считается, что тонкая выстилка эндометрия (выстилка менее 8 мм) недостаточно восприимчива.
- Также предполагалось, что инфекция матки предотвращает имплантацию, делая маточную среду менее оптимальной.
Существует также много недоказанных причин недостаточной восприимчивости матки, которые включают иммунологические теории, такие как наличие большого количества маточных NK-клеток, чрезмерное совпадение HLA между партнерами и проблемы со свертываемостью крови.
Какие факторы помимо эмбриона и матки могут способствовать отторжению имплантации?
Легкость, с которой матка может быть использована для переноса эмбриона, также играет ключевую роль в достижении успешной имплантации. Если доступ к матке через шейку затруднен (например, у пациенток со стенозом шейки матки), то следует использовать другие методы переноса эмбрионов, такие как ЗИФТ, чтобы ускорить имплантацию.
Можно ли лечить отторжение имплантации? Какие доказательные методы лечения доступны?
Да, это лечится, но только если известна причина. Одной и единственной известной, научно доказанной причиной неудачи имплантации являются генетически некомпетентные эмбрионы. Если вы женщина преклонного материнского возраста или у вас преждевременное старение яичников, даже если вы переносите несколько эмбрионов во время цикла ЭКО, во многих случаях они могут быть генетически аномальными и не будут успешно имплантироваться.
Одной и единственной известной, научно доказанной причиной неудачи имплантации являются генетически некомпетентные эмбрионы. Если вы женщина преклонного материнского возраста или у вас преждевременное старение яичников, даже если вы переносите несколько эмбрионов во время цикла ЭКО, во многих случаях они могут быть генетически аномальными и не будут успешно имплантироваться.
Ирония судьбы заключается в том, что многие женщины не хотят мириться с этим фактом (ведь смириться с тем, что у них не может быть генетического ребенка) и пытаются обвинить свою матку в неудачной имплантации. В результате они считают, что суррогатное материнство может помочь им зачать ребенка, что не соответствует действительности!
Врачи пользуются своим невежеством и «лечат» их множеством различных методов лечения, которые не основаны на доказательствах. Я видела так много женщин преклонного материнского возраста, подвергающих себя множеству бесполезных методов лечения и в конечном итоге добивающихся успеха, когда они, наконец, используют донорские яйцеклетки. Поэтому, если причиной неудачной имплантации является преклонный возраст матери или плохой овариальный резерв, единственным разумным решением является использование донорских яйцеклеток.
Поэтому, если причиной неудачной имплантации является преклонный возраст матери или плохой овариальный резерв, единственным разумным решением является использование донорских яйцеклеток.
Если в полости матки имеются спайки, миомы или полипы, препятствующие имплантации, их удаление поможет добиться имплантации эмбриона.
Роль толщины эндометрия в успешной имплантации остается под вопросом. У многих женщин с тонким эндометрием имплантация успешна, но научная литература показывает, что толщина эндометрия более 8 мм оптимальна для достижения имплантации.
Какие виды «недоказательной» терапии доступны для лечения неудачи имплантации?
Следующие методы лечения не имеют убедительных доказательств своей эффективности и являются весьма сомнительными:
- Использование препаратов, разжижающих кровь, таких как аспирин и гепарин.
- Причинение локального повреждения эндометрия перед переносом эмбриона для улучшения местного маточного кровотока.

- Терапия, такая как использование стероидов, внутривенных иммуноглобулинов, интралипидов и т. д., которые, как утверждается, снижают уровень NK-клеток в матке.
- Иммунотерапия отцовских лимфоцитов для «лечения» совпадения HLA между партнерами.
- Использование G-CSF (гранулоцитарно-колониестимулирующего фактора), известного как нейпоген.
- Использование эмбрионального клея (вещество, которое, как утверждается, улучшает прикрепление эмбриона к матке).
- Регулярное проделывание отверстия в блестящей оболочке эмбриона (внешней оболочке эмбриона) с целью помочь эмбриону успешно вылупиться из скорлупы. Это известно как вылупление эмбрионов с помощью лазера.
- Совместное культивирование эмбрионов с эпителиальными клетками эндометрия.
- Внутриутробное введение РВМС (мононуклеарных клеток периферической крови).
Врачи не должны предлагать такое лечение. Они должны убедиться, что пациент понимает, что вышеупомянутые методы лечения не основаны на доказательствах и не могут быть панацеей от их проблемы.
Что мне делать, если у меня повторная неудача при имплантации?
- Проверьте свой АМГ; день 3 значения ФСГ и Е2; и количество антральных фолликулов — они в норме? У вас хороший овариальный резерв? Если у вас плохой овариальный резерв или вы старше 40 лет и неоднократно терпели неудачу при имплантации, вам следует рассмотреть возможность использования донорских яйцеклеток.
- Если вы молоды и имеете хороший овариальный резерв, спросите у эмбриолога, как выглядят ваши эмбрионы – хорошего ли они качества? Если они хорошего качества (хорошо делятся в соответствии со своим возрастом), то есть вероятность, что пересаженные эмбрионы могли быть генетически нормальными (к сожалению, у нас до сих пор нет технологии, чтобы проверить все возможные генетические дефекты до переноса). ).
- У вас СПКЯ? Они извлекли много яйцеклеток (более 25 яйцеклеток) из ваших яичников? СПКЯ может быть причиной отсутствия имплантации эмбриона. Прием сенсибилизаторов инсулина, таких как метформин и миоинозитол, может решить вашу проблему.
- Если ваш врач использовал тот же протокол стимуляции яичников для извлечения яйцеклеток из ваших яичников, вы также можете попробовать другие протоколы стимуляции яичников. Было обнаружено, что протоколы мягкой стимуляции яичников лучше подходят для производства яйцеклеток и эмбрионов более высокого качества у выбранной группы пациентов с ЭКО (в основном у пациентов с плохим овариальным резервом).
- Если у вас несколько раз было неудачное ЭКО из-за переноса эмбрионов на 3-й день, попробуйте провести перенос эмбрионов на 5-й день. Тот факт, что эмбрионы развиваются до стадии бластоцисты, является хорошим признаком (хотя и не окончательным доказательством) того, что ваши эмбрионы достаточно хороши.
- Вы можете попробовать перенести замороженный эмбрион вместо свежего. Высокий уровень эстрогена в организме во время свежего цикла может повредить восприимчивость матки.
- Если у вас стеноз шейки матки и перенос эмбрионов цервикальным путем становится затруднительным, вы можете попробовать другие способы переноса эмбрионов (например, ZIFT)
- Попробуй сменить клинику — иногда помогает!
- Другим доступным вариантом является использование донорских яйцеклеток или донорских эмбрионов.
- Если в полости матки имеются спайки, полипы или миомы, их необходимо удалить. Если есть много спаек или если вы страдаете от тонкой слизистой оболочки эндометрия из-за неизлечимого синдрома Ашермана, вы можете выбрать суррогатное материнство.
Какое сообщение на вынос?
Когда эмбрион попадает в матку на стадии бластоцисты, он инициирует молекулярный перекрестный контакт с эндометрием. Возможно, он говорит: «Привет, я здесь и хочу связаться с тобой. Ты готов принять меня? Эндометрий воспринимает сигнал, посылаемый эмбрионом, и реагирует соответствующим образом. Все эти перекрестные помехи происходят за счет высвобождения соответствующих белковых молекул. Считается, что если есть какая-то проблема с этим перекрестным взаимодействием, имплантация эмбриона не удастся.
Предполагается, что эндометрий действует как биосенсор качества эмбриона. Это означает, что если в полость матки попадает генетически аномальная бластоциста, эндометрий чувствует это по сигналам, посылаемым эмбрионом, и препятствует имплантации эмбриона. Так что, если этот биосенсорный механизм неисправен у некоторых женщин, они парадоксальным образом становятся «сверхфертильными». То есть такие женщины очень легко беременеют, потому что даже генетически аномальные эмбрионы могут прикрепиться к эндометрию и установить беременность.
Так что, если этот биосенсорный механизм неисправен у некоторых женщин, они парадоксальным образом становятся «сверхфертильными». То есть такие женщины очень легко беременеют, потому что даже генетически аномальные эмбрионы могут прикрепиться к эндометрию и установить беременность.
С другой стороны, они страдают от повторяющихся биохимических беременностей или выкидышей, потому что даже если генетически аномальный эмбрион имплантируется, он не может развиться в здорового ребенка и в конечном итоге абортируется.
Есть также исследования, которые показывают, что даже если эндометрий не является оптимально восприимчивым, генетически компетентный эмбрион может модифицировать среду эндометрия, чтобы сделать ее благоприятной для успешной имплантации.
Когда вы разговариваете с опытным специалистом по ЭКО, он из своего практического опыта скажет, что, когда женщины страдают от рецидивирующей неудачи имплантации, в большинстве случаев подмена яйцеклетки может привести к успешной имплантации и беременности!
Эндометрий, по-видимому, действует как пассивный реципиент.