Содержание
Вакцинопрофилактика полиомиелита
Для профилактики полиомиелита созданы действенные вакцины: оральная полиомиелитная вакцина (ОПВ) и инактивированная (убитая) вакцина от полиомиелита (ИПВ). Чем они отличаются? Что нужно о них знать? Рассказываем в нашей статье.
Полиомиелит известен человечеству с давних времен. Поражает он преимущественно детей и может протекать очень тяжело. Одно из названий, ярко характеризующих его клиническую картину, — «детский паралич».
Полиомиелит острая нейроинфекция, при которой в результате репликации вируса происходит гибель мотонейронов и развитие вялого паралич мышц. Хоть болеют полиомиелитом преимущественно дети до 5 лет, заразится может не вакцинированный человек любого возраста. В результате перенесенного заболевания могут формироваться остаточные явления, которые проявляются нарушениями функций опорно-двигательной системы, атрофиями мышц, костными деформациями и контрактурами.
Человек, переболевший паралитической формой полиомиелита, на всю жизнь остается инвалидом.
Благодаря вакцинации Российская Федерация с 2002 г. имеет статус страны свободной от полиомиелита. Но это не исключает возможности возникновения полиомиелита в нашей стране. В качестве пояснения уместен пример, который привел П. Оффит в своей книге «Смертельно опасный выбор. Чем борьба с прививками грозит нам всем».
«В 2003 году в Нигерии распространились слухи, что вакцина от полиомиелита вызывает СПИД и приводит к бесплодию у девочек. Программы вакцинации резко забуксовали. К 2006 году полиомиелит из Нигерии появился в двадцати странах Азии и Африки, которые до этого считались свободными от полиомиелита, и более 5000 человек было тяжело и необратимо парализовано». В этой связи один из деятелей здравоохранения в США совершенно уместно отметил: «От США до полиомиелита – один авиаперелет. Стоит нам ослабить бдительность, стоит сузить охват прививок, как сразу возникнет вероятность вспышки полиомиелита».
Несмотря на эпидемиологическое благополучие внутри страны, существуют высокие риски завоза полиомиелита.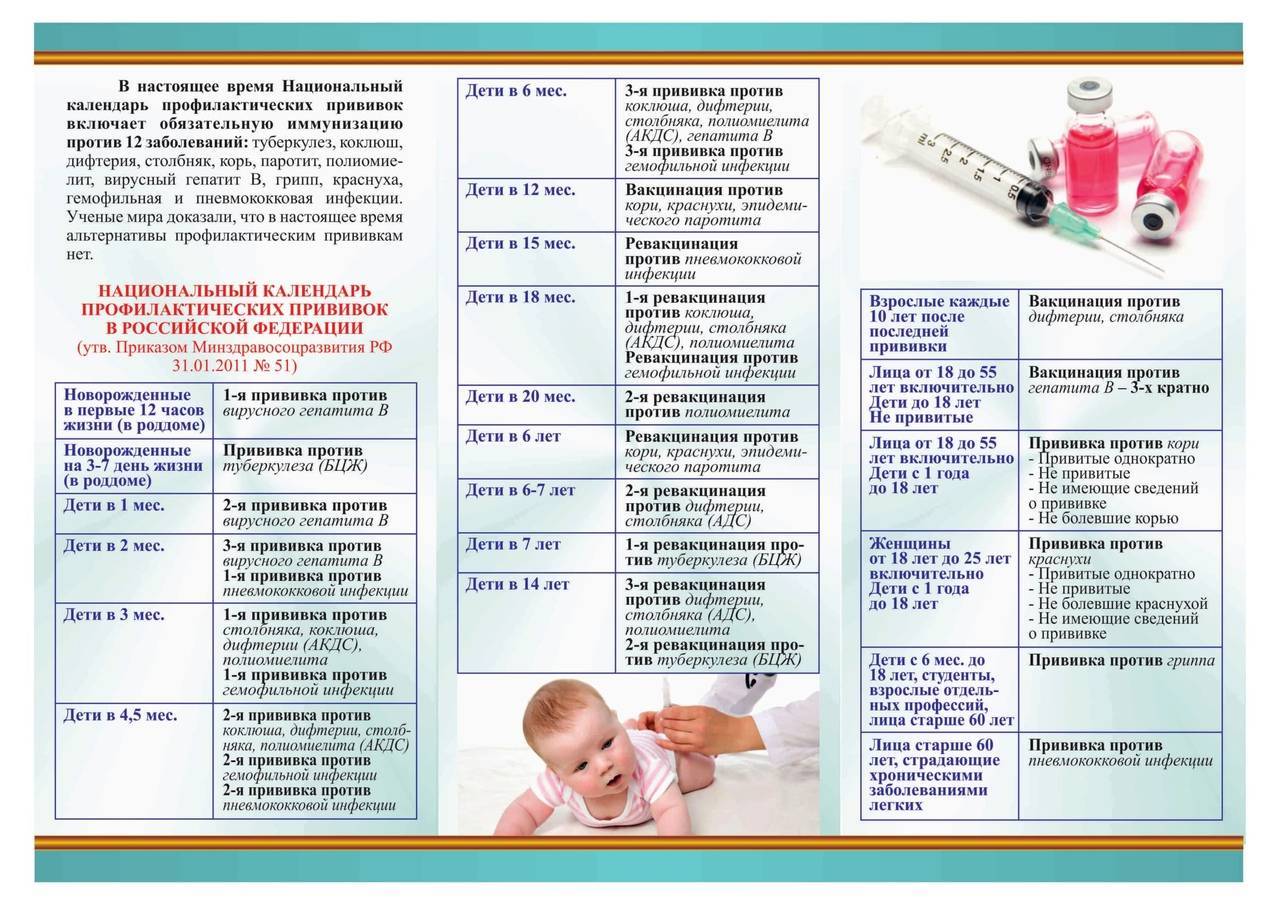 Кроме того, при снижении показателя коллективного иммунитета менее 95%, возможна передача вакцинных полиовирусов между непривитым контингентом.
Кроме того, при снижении показателя коллективного иммунитета менее 95%, возможна передача вакцинных полиовирусов между непривитым контингентом.
Для поддержания статуса страны свободной от полиомиелита, в России осуществляются действенные профилактические мероприятия: вакцинация населения в соответствии с национальным календарем профилактических прививок, контроль каждого случая острого вялого паралича, проведение противоэпидемических мероприятий при завозах инфекции, эпидемиологический надзор за полиомиелитом.
Охват иммунизацией детского населения по полиомиелиту должен быть не менее 95%.
Какие же вакцины для профилактики заражения полиомиелитом существуют и чем они отличаются?
Сегодня массово применяются две вакцины – живая оральная полиовирусная вакцина (ОПВ) и инактивированная (убитая) вакцина от полиомиелита (ИПВ). Каждая из этих вакцин имеет свои особенности.
Оральная полиомиелитная вакцина содержит ослабленные живые штаммы трех типов вируса полиомиелита.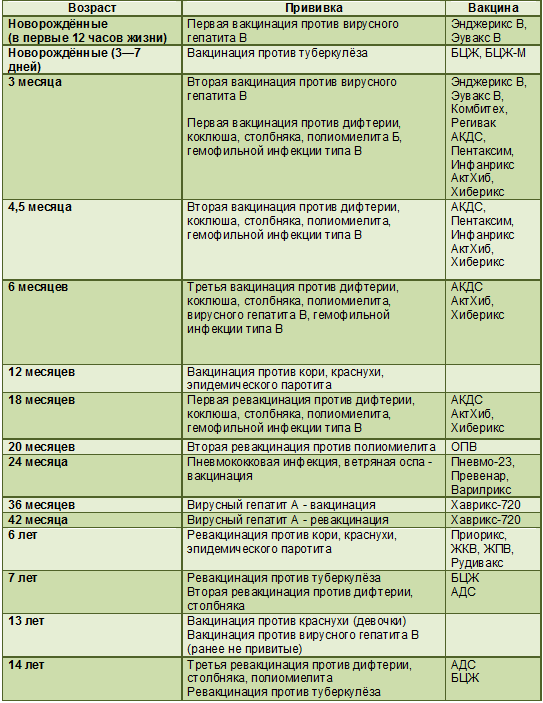 В настоящее время, применяется бивалентная оральная полиомиелитная вакцина (бОПВ).
В настоящее время, применяется бивалентная оральная полиомиелитная вакцина (бОПВ).
Основными преимуществами данной вакцины является удобная форма применения в виде капель, высокая иммуногенность, формирование местного иммунитета в кишечнике (мукозальный иммунитет) за счет перорального способа введения.
К минусам можно отнести способность ослабленных вакцинных вирусов возвращать себе патогенность и приводить к развитию постпрививочного вакциноассоциированного полиомиелита. Эти осложнения могут возникнуть у лиц с иммунодефицитными состояниями, а также в случае нарушения схемы иммунизации у лиц, получивших в качестве первой дозы вакцину ОПВ.
Различные проявления вакциноассоциированного полиомиелита наблюдаются в 1 случае на 0,7 — 2,5 миллиона привитых человек.
Оральная полиомиелитная вакцина имитирует естественное поступление вирусов в организм человека, поэтому привитый человек в течение 60 дней выделяет с фекалиями вакцинные полиовирусы. В этом случае контакт с привитым от полиомиелита может быть опасен для непривитого человека, так как он может заразиться.
В этом случае контакт с привитым от полиомиелита может быть опасен для непривитого человека, так как он может заразиться.
Вакциноассоциированный полиомиелит изменил подходы к вакцинации от полиомиелита. Согласно современным рекомендациям, вакцинация от полиомиелита начинается с ИПВ. Это позволяет исключить вероятность возникновения вакциноассоциированного полиомиелита. В перспективе — полный отказ от применения ОПВ.
Инактивированная полиомиелитная вакцина (ИПВ) — содержит убитые вирусы полиомиелита 1, 2 и 3 типа. Она считается одной из самых безопасных вакцин и имеет минимум противопоказаний.
Главное преимущество ИПВ — неспособность вызывать вакциноассоциированный полиомиелит вследствие отсутствия в своем составе живого вируса.
К недостаткам ИПВ можно отнести высокую стоимость производства, повышенные требования биологической безопасности при создании, слабый мукозальный иммунитет. Из-за этого в кишечнике человека, привитого ИПВ, вирус полиомиелита может размножаться и выделяться во внешнюю среду. Привитый человек не заболеет, но может стать источником инфекции для непривитого.
Привитый человек не заболеет, но может стать источником инфекции для непривитого.
В Российской Федерации вакцинация и ревакцинация против полиомиелита проводится в соответствии с национальным календарем профилактических прививок вакцинами, разрешенными к применению.
Вакцинация против полиомиелита проводится детям по следующей схеме: в 3 мес, 4.5 мес, 6 мес — инактивированной полиомиелитной вакциной.
Ревакцинация против полиомиелита проводится детям по следующей схеме: в 18 мес — инактивированной полиомиелитной вакциной; в 20 мес и 6 лет — оральной полиомиелитной вакциной.
Получить консультацию по поводу иммунизации против полиомиелита и сделать профилактические прививки можно в любой поликлинике по месту жительства.
Берегите себя и будьте здоровы!
Список литературы:
1. Постановление Главного государственного санитарного врача РФ от 28. 01.2021 N 4 «Об утверждении санитарных правил и норм СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней»
01.2021 N 4 «Об утверждении санитарных правил и норм СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней»
2. Стратегия ликвидации полиомиелита на 2022–2026 гг: выполнение обещания [Polio Eradication Strategy 2022–2026: delivering on a promise]. Женева: Всемирная организация здравоохранения ; 2021 г. Лицензия: CC BY-NC-SA 3.0 IGO
3. Руководство по эпидемиологии инфекционных болезней [в 2 т.]. Т.1 / Н.И. Брико, Г.Г. Онищенко, В.И. Покровский. – Москва: ООО «Издательство «Медицинское информационное агенство», 2019. – 880с.
4. Руководство для врачей/ под ред. Л.С. Намазовой-Барановой, Н.И. Брико, И.В. Фельдблюм. — Москва: ПедиатрЪ, 2021. — 648с.
5. Chumakov K., Ишмухаметов А. А. Вакцины против полиомиелита: настоящее и будущее.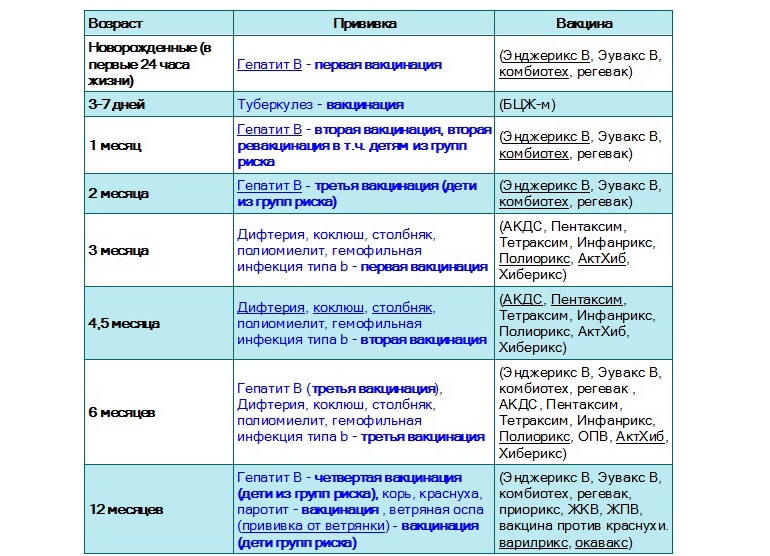 Эпидемиология и Вакцинопрофилактика. 2018; 17 (3): 4-18.
Эпидемиология и Вакцинопрофилактика. 2018; 17 (3): 4-18.
6. Намазова-Баранова Лейла Сеймуровна, Баранов Александр Александрович, Брико Николай Иванович, Иванова Ольга Евгеньевна, Полибин Роман Владимирович, Ртищев Алексей Юрьевич, Учайкин Василий Федорович, Федосеенко Марина Владиславовна, Фельдблюм Ирина Викторовна, Чуланов Владимир Петрович, Шакарян Армен Каренович, Шамшева Ольга Васильевна ПОЗИЦИЯ ЭКСПЕРТОВ СОЮЗА ПЕДИАТРОВ РОССИИ В ОТНОШЕНИИ УХУДШЕНИЯ ГЛОБАЛЬНОЙ СИТУАЦИИ С ВИРУСОМ ПОЛИОМИЕЛИТА // Детские инфекции. 2022. №4 (81). URL: https://cyberleninka.ru/article/n/pozitsiya-ekspertov-soyuza-pediatrov-rossii-v-otnoshenii-uhudsheni… (дата обращения: 13.03.2023).
7. Смертельно опасный выбор. Чем борьба с прививками грозит нам всем / П. Оффит — «Corpus (АСТ)», 2015 — (Библиотека фонда «Эволюция»)
8. https://yaprivit. ru/diseases/poliomielit/
ru/diseases/poliomielit/
Способ вакцинопрофилактики полимиелита на крайнем севере
Изобретение относится к медицине, а именно к педиатрии, и касается вакцинопрофилактики полиомиелита на Крайнем Севере. Для этого при первичной вакцинации детей в возрасте от 3 до 18 месяцев вакцину вводят не ранее чем через 60 дней после приезда их в районы Крайнего Севера из других климатических зон. Способ обеспечивает высокую эффективность вакцинации за счет учета адаптационных процессов в организме детей при смене климатических зон.
Изобретение относится к медицине, а именно к педиатрии, и может быть применено для вакцинации детей против полиомиелита в условиях Крайнего Севера.
Известен способ первичной массовой вакцинации детей против полиомиелита путем введения живой вакцины Сейбина (ЖВС) [1]. Вакцинация по известному методу выполняется в три этапа: первая прививка по достижении ребенком возраста 3 месяца; вторая прививка — в 4,5 месяца и третья прививка — в 6 месяцев.
Однако в известном способе вакцинации отсутствует региональный подход при его проведении, что приводит к снижению эффективности вакцинопрофилактики полиомиелита и необходимости повторного проведения вакцинального комплекса. Иммунизация в рамках национального календаря профилактических прививок против полиомиелита не учитывает процессов адаптации детей к условиям Крайнего Севера. Прививают всех детей в возрасте от 3 до 18 месяцев, как постоянно проживающих на Крайнем Севере, так и тех, кто приезжает в этот период из других регионов. Известно, что изменение региона проживания, даже временное, приводит к нарушению процессов адаптации организма ребенка к условиям Крайнего Севера, а формирование иммунитета у вакцинируемых в условиях Крайнего Севера протекает более длительное время, чем в условиях средних широт. Это особенно важно для детей пришлых жителей Крайнего Севера, приезжающих из других климатических зон страны.
Задачей изобретения является повышение эффективности способа вакцинации против полиомиелита.
Сущность изобретения заключается в том, что детей в возрасте от 3 до 18 месяцев, прибывающих на Крайний Север и подлежащих первичной вакцинации против полиомиелита согласно Календарю профилактических прививок, прививают живой вакциной Сейбина не ранее чем через 60 дней после приезда в районы Крайнего Севера из других климатических зон.
Подобный подход к профилактике полиомиелита позволяет учесть адаптационные процессы, происходящие в организме ребенка при смене широтных поясов.
Способ осуществляется следующим образом.
При проведении первичной вакцинации против полиомиелита детей в возрасте от 3 до 18 месяцев, прибывающих на Крайний Север из других регионов, прививают ЖВС не ранее чем через 60 дней после приезда.
Пример 1. Садырин Н. Вакцинирован ЖВС через 25 дней после приезда на Крайний Север в возрасте 5 месяцев. Последующие вакцинации выполнены в возрасте 6,5 и 8 месяцев. Через 12 месяцев после последней иммунизации антитела к вирусам полиомиелита I, II и III серотипов определялись соответственно в титрах <1:4, 1:4 и <1:4 — серонегативные.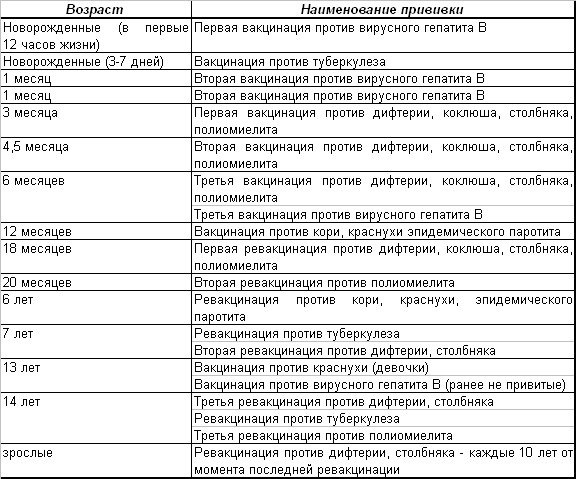 Ребенок восприимчив к вирусу полиомиелита.
Ребенок восприимчив к вирусу полиомиелита.
Пример 2. Черных И. Вакцинирован ЖВС через 30 дней после приезда на Крайний Север в возрасте 5 месяцев. Последующие вакцинации выполнены в возрасте 6,5 и 8 месяцев. Через 12 месяцев после последней иммунизации антитела к вирусам полиомиелита I, II и III серотипов соответственно определялись в титрах 1:4, <1:4 и 1:4 — серонегативные. Ребенок восприимчив к вирусу полиомиелита.
Пример 3. Борисевич С. Вакцинирован ЖВС через 35 дней после приезда на Крайний Север в возрасте 5 месяцев. Последующие вакцинации проведены в возрасте 6,5 и 8 месяцев. Через 12 месяцев после последней иммунизации антитела к вирусам полиомиелита I, II и III серотипов определялись соответственно в титрах <1:4, <1:4 и <1:4 — серонегативные. Ребенок восприимчив к вирусу полиомиелита.
Пример 4. Дроздова С. Вакцинирована ЖВС через 40 дней после приезда на Крайний Север в возрасте 4,5 месяцев. Последующие вакцинации проведены в возрасте 6 и 7,5 месяцев.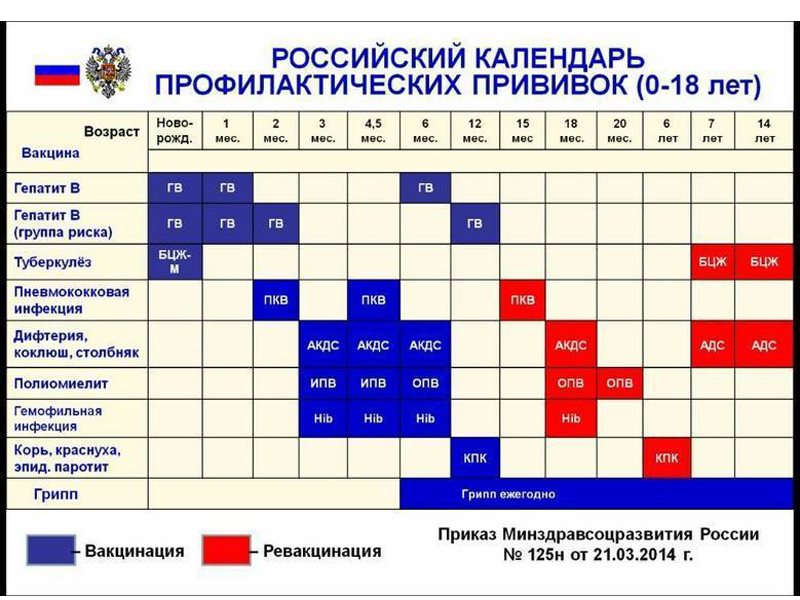 Через 12 месяцев после последней иммунизации антитела к вирусам полиомиелита I, II и III серотипов определялись соответственно в титрах 1:4, <1:4 и 1:4 — серонегативные. Ребенок восприимчив к вирусу полиомиелита.
Через 12 месяцев после последней иммунизации антитела к вирусам полиомиелита I, II и III серотипов определялись соответственно в титрах 1:4, <1:4 и 1:4 — серонегативные. Ребенок восприимчив к вирусу полиомиелита.
Пример 5. Евтухов Ж. Вакцинирован ЖВС через 50 дней после приезда на Крайний Север в возрасте 6 месяцев. Последующие вакцинации проведены в возрасте 7,5 и 9 месяцев. Через 12 месяцев после последней иммунизации антитела к вирусам полиомиелита I, II и III серотипов определялись соответственно в титрах 1:4, 1:4 и <1:4 — серонегативные. Ребенок восприимчив к вирусу полиомиелита.
Пример 6. Черткова Ю. Вакцинирована ЖВС через 55 дней после приезда на Крайний Север в возрасте 5,5 месяцев. Последующие вакцинации проведены в возрасте 7 и 8,5 месяцев. Через 12 месяцев после последней иммунизации антитела к вирусам полиомиелита I, II и III серотипов определялись соответственно в титрах <1:4, <1:4 и 1:4 — серонегативные. Ребенок восприимчив к вирусу полиомиелита.
Пример 7. Нолейкин И. Вакцинирован ЖВС через 60 дней после приезда на Крайний Север в возрасте 5 месяцев. Последующие вакцинации выполнены в возрасте 6,5 и 8 месяцев. Через 12 месяцев после последней иммунизации антитела к вирусам полиомиелита I, II и III серотипов соответственно определялись в защитных титрах 1:64, 1:64 и 1:32 — серопозитивные. Ребенок не восприимчив к вирусу полиомиелита.
Нолейкин И. Вакцинирован ЖВС через 60 дней после приезда на Крайний Север в возрасте 5 месяцев. Последующие вакцинации выполнены в возрасте 6,5 и 8 месяцев. Через 12 месяцев после последней иммунизации антитела к вирусам полиомиелита I, II и III серотипов соответственно определялись в защитных титрах 1:64, 1:64 и 1:32 — серопозитивные. Ребенок не восприимчив к вирусу полиомиелита.
Всего в условиях Крайнего Севера по предлагаемому способу привито 453 ребенка. Результат вакцинации определялся через год путем иммунологического обследования детей с разным периодом времени между приездом их на Крайний Север и вакцинацией. Титры антител оценивались в реакции цветной пробы по уровню разведения. Разведение сыворотки в титре ≤1:4 для вируса полиомиелита I, II и III серотипов рассматривалось как серонегативное — дети восприимчивы к вирусу полиомиелита. Тогда как разведение ≥1:8 оценивалось как серопозитивное — дети не восприимчивы к вирусу полиомиелита. Проведенные исследования показали, что наибольшая эффективность первичной вакцинации против полиомиелита достигалась при проведении ее в сроки не ранее 60 дней после приезда детей на Крайний Север. После прививки в другие сроки регистрировалось значительно большее число детей (в %), восприимчивых к вирусу полиомиелита.
После прививки в другие сроки регистрировалось значительно большее число детей (в %), восприимчивых к вирусу полиомиелита.
Способ создает благоприятные условия для адаптации детей при смене широтных поясов, что позволяет повысить эффективность вакцинации их на Крайнем Севере, избежать дальнейших иммунологических обследований и проведения повторных прививок.
Источники информации
1. Национальный календарь профилактических прививок. Приказ Минздрава РФ №229 от 20.06.2001.
2. Способ ревакцинации живой вакциной Сейбина на Крайнем Севере. RU 2185853 С2, 27.07.2002.
Способ вакцинопрофилактики полиомиелита путем введения живой вакцины Сейбина детям в возрасте от 3 до 18 месяцев, отличающийся тем, что при первичной вакцинации детей на Крайнем Севере вакцину вводят не ранее, чем через 60 дней после приезда их в районы Крайнего Севера из других климатических зон.
Вакцина против вирусного вектораJ & J — как она работает? Почему отличается? Как
Привет всем,
Я чувствовал, что важно сделать небольшой перерыв в написании вам, потому что я хотел, чтобы люди обработали информацию, которую я предоставил на сегодняшний день; информация, которую вы не видите или не читаете в средствах массовой информации о действующих глобальных программах вакцинации. Тема вирусных мутаций, красноречиво называемых вариантами , и полной невозможностью предоставить миру какие-либо долгосрочные данные о безопасности в отношении действующих программ вакцинации, к сожалению, все еще находится в туманной области неизвестного будущего. Напоминаем читателю, что долгосрочная безопасность всех прививок — это не вопрос дней или недель, как нас всех уверяют. Это занимает годы. Чтобы предоставить точные сроки разработки вакцины для сравнения, обратите внимание:
Тема вирусных мутаций, красноречиво называемых вариантами , и полной невозможностью предоставить миру какие-либо долгосрочные данные о безопасности в отношении действующих программ вакцинации, к сожалению, все еще находится в туманной области неизвестного будущего. Напоминаем читателю, что долгосрочная безопасность всех прививок — это не вопрос дней или недель, как нас всех уверяют. Это занимает годы. Чтобы предоставить точные сроки разработки вакцины для сравнения, обратите внимание:
- Доклинические исследования обычно проводятся в течение первых 1-2 лет , когда вакцина тестируется на животных на предмет эффективности и безопасности, включая исследования с контрольным заражением.
- Фаза I клинических испытаний следует за вторым годом и продолжается не менее 1 года, определяется как небольшие группы здоровых взрослых добровольцев, получающих вакцину для проверки ее безопасности.
- Клинические испытания фазы II начинаются через год 3 , и это когда вакцина вводится людям с характеристиками (такими как возраст и физическое здоровье), как у тех, для кого предназначена новая вакцина
- Фаза III клинических испытаний

Когда в 2019 году мир поразил COVID-19, фармацевтических компаний перешли от доклинических исследований к клиническим испытаниям фазы III в течение 1 года с перекрытием . Нормальная разработка вакцины включает каждый этап в течение 5 лет или более. Чтобы ускорить разработку вакцины против COVID-19, шаги выполняются параллельно, как показано в этой таблице.
В блоге от 17 января 2021 г., Covid-19-vaccine-safety , https://yourholisticdoc.com/blogs/yhd-blog/covid-19-vaccine-safety, я попытался объяснить, почему никогда не была вакциной против вируса короны, а также возможность осложнений, которые неизвестны у реципиентов вакцины. Я считаю, что Раскрытие информированного согласия участников испытаний вакцины о риске ухудшения клинического заболевания вакцинами против COVID-19, , опубликованное в The International Journal of Clinical Practice в октябре 2020 г., точно и кратко отражает мои опасения:
«Вакцины против SARS, MERS и RSV никогда не был одобрен, и данные, полученные при разработке и тестировании этих вакцин, предполагают серьезную механистическую озабоченность: вакцины, разработанные эмпирически с использованием традиционного подхода (состоящего из немодифицированного или минимально модифицированного вирусного шипа коронавируса для выявления нейтрализующих антител), могут быть они состоят из белка, вирусного вектора, ДНК или РНК и независимо от метода доставки могут ухудшить течение COVID-19. болезнь через антителозависимое усиление (ADE). Этот риск достаточно скрыт в протоколах клинических испытаний и формах согласия для текущих испытаний вакцины против COVID-19, поэтому маловероятно, что адекватное понимание пациентом этого риска произойдет, что исключает действительно информированное согласие субъектов в этих испытаниях».
болезнь через антителозависимое усиление (ADE). Этот риск достаточно скрыт в протоколах клинических испытаний и формах согласия для текущих испытаний вакцины против COVID-19, поэтому маловероятно, что адекватное понимание пациентом этого риска произойдет, что исключает действительно информированное согласие субъектов в этих испытаниях».
После обзора опубликованной литературы для выявления доклинических и клинических доказательств того, что вакцины против COVID-19 могут ухудшить течение заболевания при воздействии контрольного заражения или циркулирующего вируса, были сделаны следующие выводы:риск ADE должен был быть и должен быть открыто и независимо раскрыт субъектам исследования, которые в настоящее время проходят испытания вакцины, а также тем, кто набирается для испытаний и будущих пациентов после одобрения вакцины , , чтобы соответствовать стандарту медицинской этики пациента понимание для информированного согласия . (цитата: Int J Clin Pract. 28 октября 2020 г.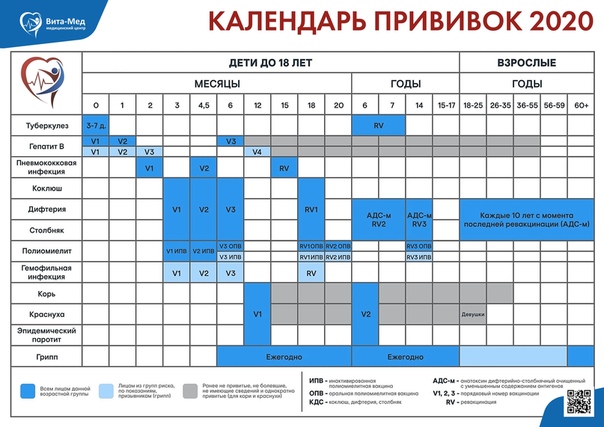 ; e13795. doi: 10.1111/ijcp.13795).
; e13795. doi: 10.1111/ijcp.13795).
Чем отличаются вакцины Pfizer, Moderna и J&J от COVID? Я описал вакцинацию мРНК в предыдущем блоге. Позвольте мне объяснить, чем J&J отличается от них, так как теперь он получил разрешение на использование в чрезвычайных ситуациях (EUA) и плохо понимается большинством людей. Вакцины этого типа использовались в ответ на недавние вспышки лихорадки Эбола. Это означает, что они использовались на людях, в отличие от технологии мРНК. В отличие от мРНК-вакцин от Pfizer и Moderna, которые связаны с наночастицами, которые доставляют мРНК в организм, вакцина J&J Viral Vector использует модифицированный, но живой вирус для проникновения в наш организм. При разработке вирусных векторных вакцин в качестве векторов использовалось несколько различных вирусов, включая грипп, вирус везикулярного стоматита (VSV), вирус кори и вирус аденовирус, вызывающий простуду. Эти векторы действуют как платформы, позволяющие белку COVID-19 проникать в наш организм, чтобы мы могли бороться с COVID в будущем, вырабатывая антитела.
Как это работает:
В вирусной векторной вакцине J&J аденовирус представляет собой вирусный вектор, который был модифицирован для доставки гена, дающего указание нашим клеткам вырабатывать антиген SARS-CoV-2. — СПИКОВЫЙ БЕЛОК. Оказавшись внутри нас, этот ген шиповидного белка COVID-19 запускает выработку антител и, как следствие, иммунный ответ. Вирус, используемый в вирусной векторной вакцине, НЕ ДОЛЖЕН представлять угрозу заболевания людей, потому что он был модифицирован или, в некоторых случаях, потому что тип вируса, используемый в качестве вектора, не может вызывать заболевание у людей. Это, конечно, подлежит обсуждению без долгосрочных исследований в моей голове.
КРАТКОЕ ОПИСАНИЕ:
В вирусной векторной вакцине J&J ген, кодирующий спайковый белок COVID-19, который обнаружен только на поверхности SARS-CoV-2, добавлен к ДНК вирусного вектора аденовируса. Вирусный вектор используется для переноса этого гена COVID-19 в наш организм. Оказавшись внутри, вирусный вектор аденовируса использует этот ген и механизм нашей клетки для производства шиповидного белка и отображения его на поверхности наших клеток.
Оказавшись внутри, вирусный вектор аденовируса использует этот ген и механизм нашей клетки для производства шиповидного белка и отображения его на поверхности наших клеток.
После появления на поверхности клетки шиповидный белок (или антиген) заставляет иммунную систему начать вырабатывать антитела и активировать Т-клетки для борьбы с тем, что она считает инфекцией. Эти антитела специфичны к вирусу SARS-CoV-2, а это означает, что иммунная система настроена на защиту от инфекции в будущем.
Called, Ad26.COV2.S, Компания Johnson & Johnson сообщила о результатах фазы 3 испытаний своей однодозовой вирусной векторной вакцины Ad26.COV2.S в конце января 2021 года. Испытание проводилось в разных географических регионах и в течение определенного периода времени. когда появилось несколько вариантов. Это важно. Из 43 783 участников, рандомизированных в соотношении 1:1 для получения плацебо или вакцины, через 28 дней после вакцинации было зарегистрировано 468 симптоматических случаев COVID-19. Следовательно, следующие статистические данные, изложенные ниже, относятся к 468 случаям COVID- через 28 дней после получения вакцины или плацебо, а не к 43 783 участникам .
Следовательно, следующие статистические данные, изложенные ниже, относятся к 468 случаям COVID- через 28 дней после получения вакцины или плацебо, а не к 43 783 участникам .
В отличие от исходов, опубликованных Pfizer и Moderna, которые сообщили, что процент добровольцев, инфицированных COVID в группе плацебо по сравнению с вакцинированным населением, составил 95% от невакцинированной группы (отсюда 95% эффективность вакцины, о которой сообщалось через 8 дней после вакцинации). дозу № 2 менее чем у 200 из 40 000 человек, включенных в каждое исследование), J&J не сообщает нам, какой процент этих двух групп действительно заразился через 28 дней после вакцинации. То, что они действительно сообщают через 28 дней, — это интенсивность заболевания, проявляющаяся у инфицированных:
«Вакцина была эффективна на 72% в США, на 61% в Латинской Америке и на 64% в Южной Африке (где циркулировал вариант B.1.351) для предотвращения инфекции COVID-19 от средней до тяжелой».
Судя по моему исчерпанному обзору литературы, J&J сообщает нам, что причина, по которой они получили EUA, заключается в том, что: 28-й день вполне мог наступить как в группе плацебо, так и в группе вакцинации, НО COVID-19 средней или тяжелой степени.симптомы инфекции были предотвращены в вакцинированной группе:
- 72% в США,
- 61% в Латинской Америке,
- 64% в Южной Африке
Я думаю, что эти статистические данные показательны и важны для нового вируса, который постоянно мутирует.
Также важно, что вакцина была на 85% эффективна в предотвращении тяжелого заболевания во всех географических регионах, и эта эффективность против тяжелого заболевания увеличивалась с течением времени, и после 49-го дня не было зарегистрировано ни одного случая у вакцинированных участников.. Кроме того, вакцина обеспечила 100% защиту от госпитализации и смерти, связанной с COVID-19, на 28-й день. дальнобойщик и пост-ковидные симптомы ИЗ-ЗА данных, которые я выделил КРАСНЫМ цветом.
Кроме того, вакцина J&J продемонстрировала стабильную защиту во всех изученных вариантах и регионах, включая Южную Африку, где почти все случаи COVID-19(95%) были вызваны заражением вариантом SARS-CoV-2 из линии B.1.351. Я считаю, что это также очень важная информация, которая доказывает мне, что со временем наука обеспечит лучшую защиту от смертей от COVID и долгосрочных последствий. Но читайте здесь между строк… через 28 дней вакцинированные пациенты заболевают COVID — просто он менее тяжелый и может иметь менее тяжелые долгосрочные последствия.
Я пообещал себе, что сделаю этот короткий и легко читаемый блог.
Возьми домой сообщения:
J&J — это тип вакцины — вирусного вектора — который в прошлом применялся для лечения людей от лихорадки Эбола — он не является на 100% экспериментальным для людей.
J&J — это однократная вакцина, которую разрабатывал и тестировал, когда в то время циркулировали мутации (для справки: вариант B. 1.1.7 (т. е. вариант для Великобритании) и вариант B.1.351 (т. е. вариант для Южной Африки). испытаний, , следовательно, J&J может лучше работать над этими вариантами в долгосрочной перспективе
1.1.7 (т. е. вариант для Великобритании) и вариант B.1.351 (т. е. вариант для Южной Африки). испытаний, , следовательно, J&J может лучше работать над этими вариантами в долгосрочной перспективе
Как и в случае с мРНК-вакцинами, Moderna и Pfizer, НЕТ ДОЛГОСРОЧНЫХ исследований безопасности. контроля (вакцина плацебо) по сравнению с вакцинированными в течение многих лет
После получения Разрешения на использование в экстренных случаях мы не сможем проводить какие-либо долгосрочные исследования вакцин, потому что с этической и моральной точки зрения недопустимо не вакцинировать население, которое было признано Разрешенным на использование в чрезвычайных ситуациях— Со временем мы теряем контроль— Я много касался этого в предыдущих блогах
Без долгосрочных исследований усиление, определяемое антителами (ADE) у вакцинированных пациентов, может привести к значительным воспалительным изменениям в организме, которые никогда не будут связаны с прививками, которые мы делаем, потому что мы не можем их контролировать.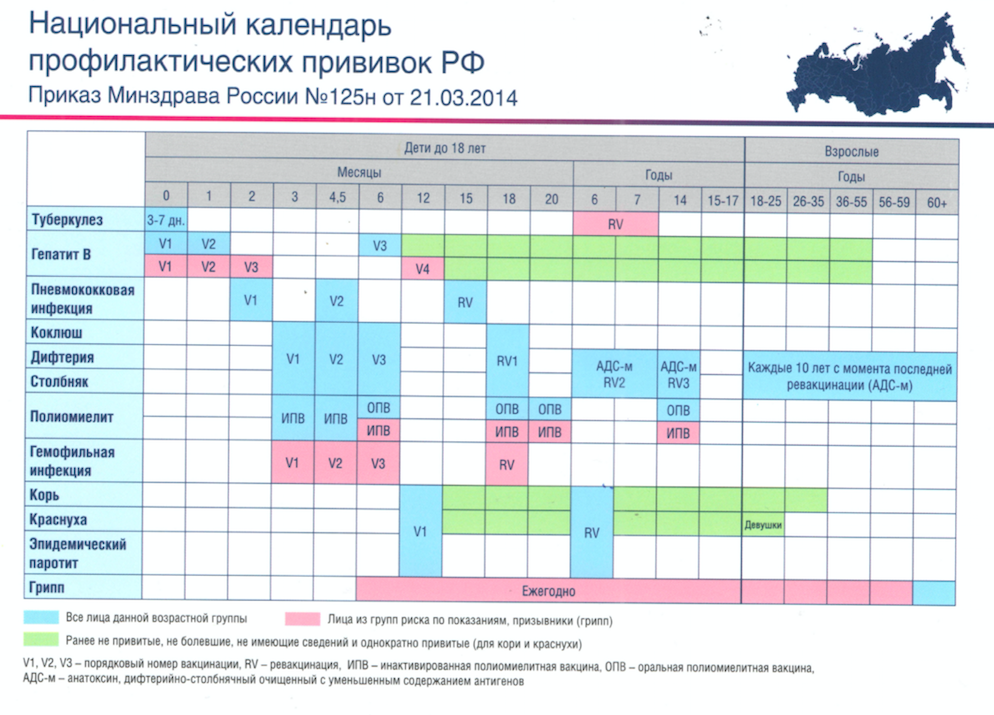 с течением времени для сравнения вакцинированных и непривитых. У нас нет данных.
с течением времени для сравнения вакцинированных и непривитых. У нас нет данных.
Всем людям во всем мире говорят, что их социальная и глобальная ответственность заключается в получении (т. никому не сказали, что они участвуют в исследовании, и они никогда не видели согласия, которым я поделился выше, в котором говорилось о возможных долгосрочных опасностях вакцины. У нас нет хороших исследований для изучения долгосрочного воздействия вакцины, потому что теперь она считается разрешенной вакциной для экстренного использования, и мы все должны внести свой вклад и пройти вакцинацию. Потеря контроля — потеря данных — никакой связи с долгосрочными последствиями вакцины.
Я так впечатлен тем, насколько хорошо пациенты, с которыми я работаю, либо бросили вызов COVID с помощью нашей программы естественной профилактики, либо очень быстро выздоровели от инфекции. Я хотел бы напомнить всем, что получение вакцины от COVID-19 еще не доказало свою эффективность, чем естественный иммунитет при заражении COVID-19.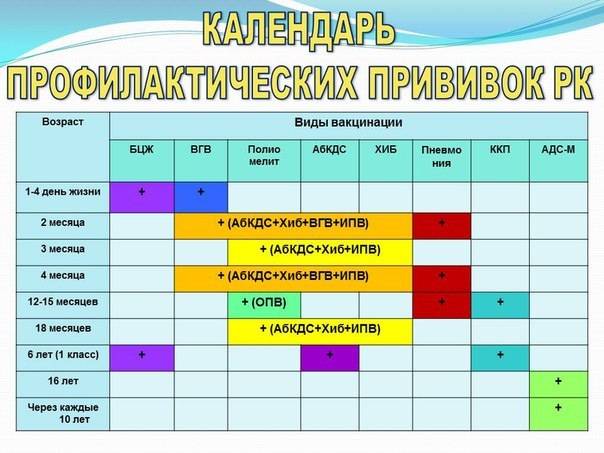 Как бы вы ни приняли решение о вакцинации против COVID-19, моя работа заключается в том, чтобы держать вас в курсе. Надеюсь, я это сделал. Пожалуйста, помните, что вся моя программа профилактики и лечения COVID-19 находится на моем веб-сайте, и ее можно найти здесь Коронавирус и программа профилактики вирусов.
Как бы вы ни приняли решение о вакцинации против COVID-19, моя работа заключается в том, чтобы держать вас в курсе. Надеюсь, я это сделал. Пожалуйста, помните, что вся моя программа профилактики и лечения COVID-19 находится на моем веб-сайте, и ее можно найти здесь Коронавирус и программа профилактики вирусов.
Я очень ценю ваши мысли и вопросы, а также ваше мнение. Поделитесь ими в блоге. Я также хотел бы получить поднятие рук в комментариях в блоге от тех, кто хочет узнать больше об Ивермектине.
Наконец, запомните код скидки 15% STAYWELL при оформлении заказа.
Как известно, я официально увлекаюсь серфингом. Это обеспечило удивительное снятие стресса от COVID! Ура, и дайте мне знать, как я могу быть полезным!
Dr. Ariane Cometa
your holistic doc
Вакцина против COVID-19 – Калифорнийские вакцины для детей (VFC)
| Оповещения: 901 75 |
|---|
Обновления вакцин
Клинические рабочие пособия
Операции провайдера
Сейчас идет набор поставщиков педиатрических услуг
|
Продвижение бивалентной вакцины:
- Рекламные ресурсы для обновленных вакцин против COVID-19
- Будьте в курсе вакцин против COVID-19 (веб-сайт CDC)
- Плакат медицинского работника (CDPH)
- Плакат для пожилых людей (CDPH)
- Наклейки «Я получил обновленный бустер COVID-19»
Инструменты, позволяющие избежать путаницы с вакцинами:
- Контрольный список введения вакцин
- Предотвращение ошибок администрирования
- Советы по совместному администрированию | Подростки
Управление вакцинами:
- Заказ вакцин | Заказ и распространение Cadence
- Получение небольших заказов от третьей стороны по распространению (TPR)
- Контрольный список управления вакцинами
- Сообщение об испорченных, просроченных или потерянных дозах (включая бустерные дозы Moderna)
- Загрузите Инструмент настройки вспомогательного набора (помогает рассчитать количество предметов для упаковки для количества перераспределяемых доз)
- Тренинги Pfizer
- Дорожная карта myCAvax
Руководство по вакцинации:
- Временные клинические рекомендации по использованию вакцин против COVID-19 (CDC)
- Рекомендация COVID-19Вакцинация: клинические темы для обсуждения для поставщиков педиатрических услуг 4/5
- Детский контрольный список COVID-19: лучшие практические стратегии высокоэффективных клиник VFC в Калифорнии
- Сравнение риска вакцинации против COVID-19 (на английском и испанском языках): Подростки | Молодежь
- Информационный бюллетень о COVID-19, миокардите и вакцинах
- Советы по снятию беспокойства во время вакцинации
- Распознавание и реагирование на анафилаксию (CDC)
- Клинические рекомендации для людей, перенесших COVID-19Вакцина за пределами США
- Укажите расовую/этническую принадлежность каждого пациента, получающего вакцину против COVID-19
- Вакцины против COVID-19 во время беременности или кормления грудью (CDC)
- COVID-19 и беременность: руководство для клиницистов (ACOG)
- Дополнительные ресурсы для пациентов
Слушай.


 05.
05.