Микробиологическое исследование, позволяющее выявить в биоматериале уреаплазмы и определить их чувствительность к антибиотикам.
При обнаружении микробиологическим методом микроорганизмов, составляющих нормальную микрофлору, или условно-патогенных микроорганизмов в титре менее диагностического не определяется чувствительность к антибиотикам и бактериофагам, так как это количество не является значимым и не требует лечения противомикробными препаратами.
Синонимы русские
Уреаплазмоз, уреаплазменная инфекция, Т-960, микоплазмоз.
Синонимы английские
Ureaplasma species culture, bacteria identification and susceptibility.
Метод исследования
Микробиологический метод.
Какой биоматериал можно использовать для исследования?
Мазок урогенитальный, эякулят, секрет простаты, среднюю порцию утренней мочи.
Как правильно подготовиться к исследованию?
- Женщинам рекомендуется сдавать урогенитальный мазок или мочу до менструации или через 2-3 дня после ее окончания.
- Мужчинам не следует мочиться в течение 3 часов до сдачи урогенитального мазка или мочи.
Общая информация об исследовании
Уреаплазмы – это микроорганизмы, способные паразитировать на мембране сперматозоидов и эпителия слизистой оболочки мочеполовых органов. Они относятся к транзиторной микрофлоре органов мочеполовой системы. От остальных микоплазм их отличает наличие уреазной активности, то есть способности расщеплять мочевину до аммиака, отчего и произошло их название. К уреаплазмам относятся U. Urealyticum и U. Parvum, термин U. species используется для обозначения обоих видов. Путь передачи – преимущественно половой, кроме того, возможен контактно-бытовой, а также вертикальный – от больной матери к ребенку во время беременности или родов.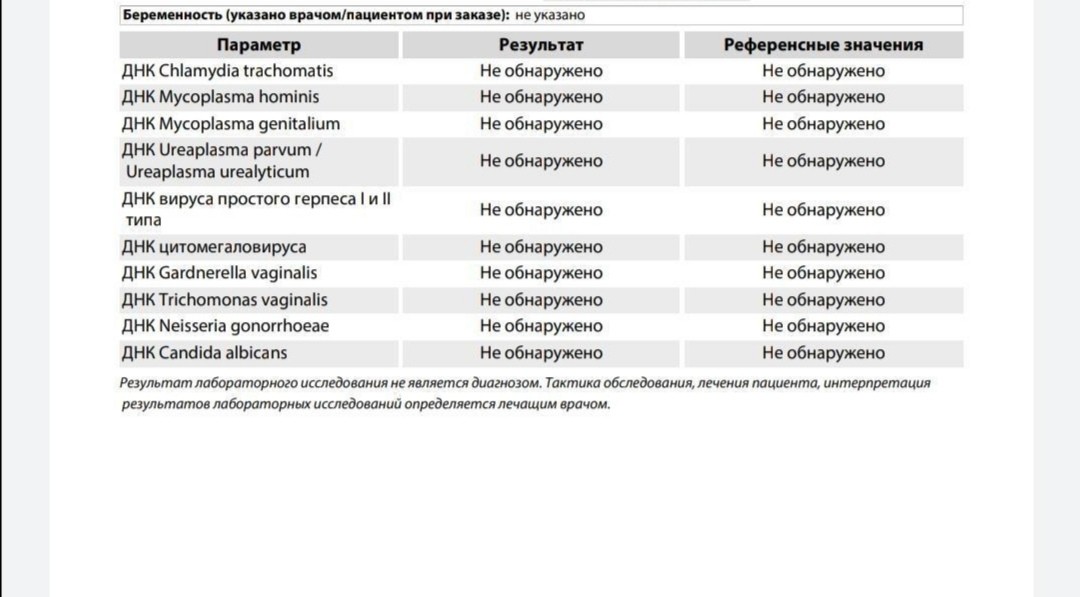
Инфицирование не обязательно ведет к заболеванию. Развитию инфекции способствуют различные иммунодефициты (в том числе дисбиоз влагалища при бактериальном вагинозе у женщин или нарушение выработки простатического антимикробного фактора у мужчин с хроническим простатитом), нарушение факторов местной защиты, а также сопутствующие инфекции (хламидиоз, гонорея, бактериальный вагиноз и т. д.).
Инкубационный период составляет 2-5 недель. Клинические симптомы уреаплазменной инфекции могут быть выражены слабо или даже отсутствовать (характерно для женщин).
У мужчин уреаплазмы способны вызывать воспаление уретры (негонококковый уретрит), мочевого пузыря (цистит), простаты (простатит), поражение яичек (орхит) и их придатков (эпидидимит), а также нарушение состава спермы – снижение подвижности и количества сперматозоидов, что грозит бесплодием. Иногда развиваются реактивные артриты и мочекаменная болезнь.
У женщин уреаплазмы могут быть причиной воспаления влагалища (вагинита), шейки матки (цервицита), а также ее новообразований. При ослаблении иммунитета возможно воспаление матки (эндометрит) и ее придатков (аднексит), что влечет за собой поражение маточных труб и развитие в них спаек. Это способствует внематочной беременности или бесплодию. Кроме того, уреаплазмы приводят к цервикальной недостаточности, выкидышам, хорионамнионитам, рождению детей с низкой массой тела (менее 2500 г), а также к бронхолегочным заболеваниям (воспалению легких, бронхолегочной дисплазии), к бактериемии и менингиту у новорождённых.
Уреаплазмы (U. species) могут рассматриваться в качестве причины воспалительных заболеваний мочеполовой системы в том случае, если при лабораторном исследовании не обнаруживаются другие патогенные микроорганизмы, способные вызвать эти заболевания. При этом используется метод культивирования на питательных средах (посев). В 80 % случаев при уреаплазменной инфекции также выявляются микоплазмы, хламидии и анаэробная флора.
Для чего используется исследование?
- Чтобы установить причину хронических воспалительных заболеваний мочеполовой системы.
- Для дифференциальной диагностики заболеваний, протекающих со сходными симптомами: хламидиоза, гонореи, микоплазменной инфекции.
- Для выбора рациональной антибактериальной терапии и оценки ее эффективности.
- Для профилактического обследования.
Когда назначается исследование?
- При подозрении на уреаплазменную инфекцию, в том числе после случайных половых связей, при симптомах воспаления мочеполовой системы.
- При планировании беременности (обоим супругам).
- При бесплодии или невынашивании беременности.
- При внематочной беременности.
- При необходимости оценить эффективность проводимой антибактериальной терапии (на 10-14-й день после отмены препарата).
Что означают результаты?
Референсные значения: нет роста.
Положительный результат
Выявление уреаплазм в большом количестве в сочетании с клиническими признаками воспаления органов мочеполовой системы при отсутствии других патогенных микроорганизмов свидетельствует о наличии уреаплазменной инфекции и о том, что именно она явилась причиной воспаления.
Небольшое количество уреаплазм при условии, что симптомы вызываемых ими заболеваний отсутствуют, расценивается как носительство.
Отрицательный результат
Отсутствие роста уреаплазм в посеве свидетельствует об отсутствии уреаплазменной инфекции.
Что может влиять на результат?
Предшествующая антибактериальная терапия.
Важные замечания
- В группу повышенного риска развития уреаплазменной инфекции входят люди с многочисленными половыми контактами, беременные женщины, курящие, женщины, принимающие оральные контрацептивы, а также люди с низким социально-экономическим статусом.
- При планировании беременности для профилактики женщине следует пройти обследование на уреаплазменную инфекцию, поскольку лечение этого заболевания антибиотиками во время беременности, особенно на раннем сроке, опасно.
 Оно неблагоприятно влияет на плод и может привести к выкидышу.
Оно неблагоприятно влияет на плод и может привести к выкидышу. - Посев на уреаплазму не позволяет определить ее тип. Отличить U. urealyticum от U. parvum возможно только при помощи ПЦР-исследования.
Также рекомендуется
- Ureaplasma species, ДНК количественно [реал-тайм ПЦР]
- Ureaplasma parvum, ДНК [реал-тайм ПЦР]
- Ureaplasma urealyticum, ДНК [реал-тайм ПЦР]
- Ureaplasma urealyticum, IgA
- Ureaplasma urealyticum, IgG, титр
- Chlamydia trachomatis, ДНК [реал-тайм ПЦР]
- Mycoplasma genitalium, ДНК [реал-тайм ПЦР]
- Mycoplasma hominis, ДНК [реал-тайм ПЦР]
- Спермограмма
- Микроскопическое исследование секрета предстательной железы (микрофлора)
- Микроскопическое исследование отделяемого мочеполовых органов мужчин (микрофлора)
- Микроскопическое исследование отделяемого мочеполовых органов женщин (микрофлора), 3 локализации
Кто назначает исследование?
Акушер-гинеколог, уролог, венеролог, педиатр-неонатолог, инфекционист.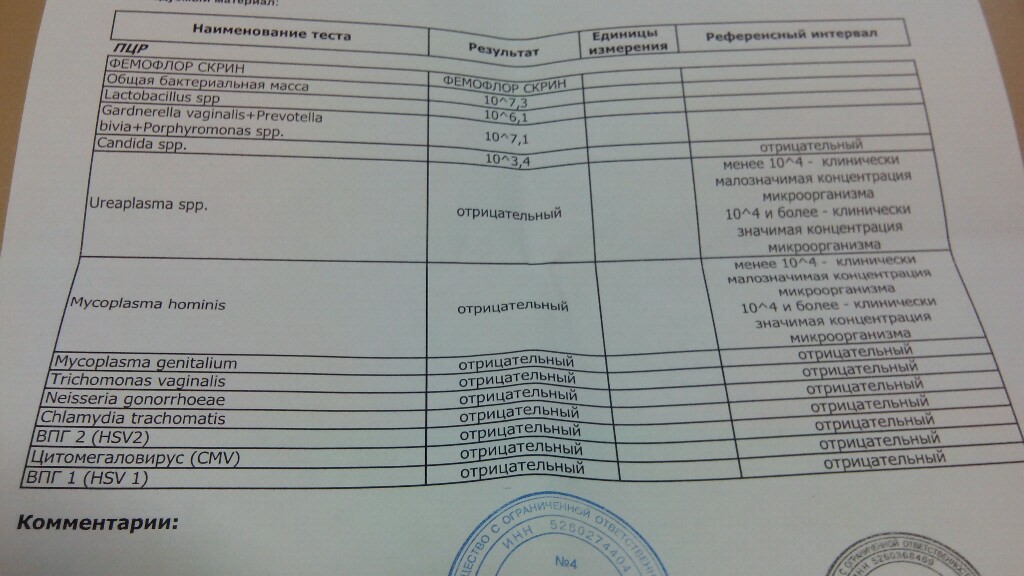
Литература
- Карамова А. Э. Значение Ureaplasma urealyticum и Mycoplasma genitalium как возбудителей воспалительных заболеваний урогенитального тракта / А. Э. Карамова, А. В. Поляков, И. В. Хамаганова // Клин. микробиол. антимикроб. химиотер. – 2004. – Т. 6, № 4. – C. 365-370.
- Халдин А. А. Урогенитальный хламидиоз и уреаплазмоз: вопросы диагностики и новые возможности терапии / А. А. Халдин // Инфекции и антимикробная терапия. – 2004. – № 3. – С. 93-95.
- Kenny G. E. Genital Mycoplasmas: Mycoplasma genitalium, Mycoplasma hominis, and Ureaplasma Species. In: Principles and practice of infectious disease / G. L. Mandell, Bennett J. E., Dolin R (Eds) ; 6th ed. – Churchill Livingstone, Philadelphia, PA 2005. – 2701 p.

- Ureaplasma urealyticum intrauterine infection: role in prematurity and disease in newborns / G.H. Cassell [et al.] // Clin. Microbiol. Rev. – 1993. – Vol. 6, N 1. – P. 69-87.
- Larsen B. Mycoplasma, Ureaplasma, and adverse pregnancy outcomes: a fresh look / B. Larsen, J. Hwang // Infectious Diseases in Obstetrics and Gynecology. Electronic journal. – Vol. 2010. – Article ID 521921.
Современный взгляд на проблему уреаплазменной инфекции uMEDp
В статье приводятся основные характеристики уреаплазм, рассматриваются методы диагностики, лечения и профилактики уреаплазменной инфекции. Отмечается необходимость своевременного выявления как специфических, так и неспецифических возбудителей с целью назначения оптимальной антибактериальной терапии. Особое внимание уделено антибиотику группы макролидов – джозамицину, который рекомендован ведущими российскими экспертами в качестве препарата первого ряда для лечения уреаплазменной и микоплазменной инфекции и при своевременном назначении позволяет добиться полного излечения в 97,5% случаев.
В последние десятилетия значительно возросла частота уреаплазменной и микоплазменной инфекции, которая у женщин чаще всего поражает мочеполовую систему. Однако специалисты до сих пор сомневаются, можно ли считать уреаплазмоз отдельным заболеванием, так как его возбудитель обнаруживается во влагалище у здоровых женщин в 60%, а у новорожденных девочек – в 30% случаев [1, 2].
Основные характеристики класса Mollicutes
Первые представители класса Mollicutes
 позволило доказать, что микоплазмы являются самостоятельной группой, получившей название класс Mollicutes [3, 4].
позволило доказать, что микоплазмы являются самостоятельной группой, получившей название класс Mollicutes [3, 4].Класс Mollicutes – это прокариоты без клеточной стенки, не способные синтезировать a-Е-диаминопимелиновую кислоту, в результате чего они осмотически неустойчивы и проявляют пластичность и разнообразие форм. Для представителей класса Mollicutes (микоплазмы, ахолеплазмы, спироплазмы, уреаплазмы, анаэроплазмы) характерен ряд особенностей, уникальных для прокариот:
- чрезвычайно простая организация клетки, имеющая минимальное количество органелл;
- отсутствие клеточной стенки;
- самое низкое соотношение Г+Ц (гуанин + цитозин) пар оснований в их ДНК, наименьший среди прокариот размер генома (0,5–1,0 MДa).
На твердой питательной среде эти микроорганизмы образуют колонии с плотным врастающим в агар центром и более светлой периферией, размер колоний
варьирует от 50 до 500 мкм. Поверхностную часть колонии обычно составляют более крупные клетки, а центральную, более глубинную часть – мелкие, оптически более плотные [2, 5].
Поверхностную часть колонии обычно составляют более крупные клетки, а центральную, более глубинную часть – мелкие, оптически более плотные [2, 5].
Размножение микоплазм происходит путем обычного деления клеток, распада нитей на кокковидные клетки, при этом процесс деления микоплазм в общем не отличается от такового у других бактерий.
Будучи факультативными паразитами, микоплазмы зависят от хозяина по широкому спектру питательных веществ, поэтому растут на комплексной среде, в которой роль большинства компонентов определить сложно.
В качестве источника энергии Mollicutes используют способность к гидролизу аргинина и переработке глюкозы. Последний процесс идет по типу гликолиза, и его результатом является продукция молочной кислоты. Ureaplasma spp. гидролизует мочевину с образованием аммиака и углекислого газа.
Для роста и размножения все Mollicutes нуждаются в многокомпонентных средах, содержащих стеролы, предшественники нуклеиновых кислот, как минимум 12 аминокислот и витамины группы В [3, 4].
Уреаплазмы, как представители микоплазм, принадлежат к царству Procariotae, отделу Tenericutes, классу Mollicutes, они входят в порядок Mycoplasmatales, семейство Mycoplasmataceae и объединяются в род Ureaplasma. В этот род входят U. urealyticum и U. diversum. При этом паразитом человека является U. urealyticum, а U. diversum выявляют у крупного рогатого скота и других животных [2, 6].
Ureaplasma urealyticum впервые была выделена M. Shepard в 1954 г. от больного негонококковым уретритом. Своеобразие биологии уреаплазм выражается также в их относительно быстром росте. Кривая роста уреаплазм совпадает с таковой у микоплазм в латентной фазе и ранней логарифмической фазе, однако стационарная фаза достигается за 16–18 часов. Оптимум рН ростовой среды для уреаплазм ниже, чем для большинства микоплазм, и составляет 6,0–6,5. На плотной среде уреаплазмы лучше культивируются в атмосфере газовой смеси, состоящей из 95% N2 и 5% СО2 либо 5% О2, 10% СО2 и 85% N2.
Согласно электронно-микроскопическим наблюдениям клетки U. urealyticum можно разделить на 3 типа: малые (120–150 нм) – с гомогенной цитоплазмой и множеством рибосом; средние (500–750 нм) – с рибосомами по периферии; большие – с оптически более плотной негомогенной цитоплазмой и выраженным нуклеоидом.
Уреаплазмы не редуцируют тетразол и не обладают каталазной активностью. Они отличаются от других представителей Mollicutes способностью синтезировать как насыщенные, так и ненасыщенные жирные кислоты. Уреаплазмы продуцируют пигмент гипоксантин – продукт пуринового обмена, обладают растворимым бета-гемолизином, активным в отношении эритроцитов кролика и морской свинки.
С помощью специфических антисывороток удалось выделить 14 серотипов U. urealyticum. Эти серотипы можно объединить в 2 биовара – Parvo и T-960. К биовару Parvo относятся серотипы 1, 3, 6 и 14; к биовару T-960 – 2, 4, 5, 7–13 [1, 4]. В настоящее время интенсивно исследуется роль биоваров в развитии патологических проявлений уреаплазменной инфекции. Предполагается, что биовар Parvo является более патогенным, чем биовар T-960.
Предполагается, что биовар Parvo является более патогенным, чем биовар T-960.
В настоящее время считается, что патогенные свойства уреаплазм проявляются при определенных состояниях организма, которые характеризуются снижением сопротивляемости к действию патогенных агентов и определяются их способностью прикрепляться к эпителию слизистых оболочек, образованием эндо- и экзотоксинов и других токсически действующих химических соединений. Факторами патогенности для U. urealyticum являются:
1. Адгезины – поверхностные компоненты клеток, функция которых – связывание клеток микроорганизма с клетками-мишенями макроорганизма. Они играют решающую роль в развитии начальной стадии процесса. Адгезия микоплазм к клеткам-мишеням происходит в 2 этапа: 1-й – этап неспецифического взаимодействия; 2-й – этап лиганд-рецепторного взаимодействия (функцию лиганда выполняет адгезин, функцию рецептора – соответствующие структуры мембраны клетки-мишени гликопротеиновой природы). Адгезины могут обладать антигенными свойствами и быть видо- и серотипоспецифичными. Получены сведения об адгезии уреаплазм к человеческим эпителиальным клеткам, эритроцитам и сперматозоидам. Последние исследования показывают наличие у уреаплазм нескольких адгезинов.
Получены сведения об адгезии уреаплазм к человеческим эпителиальным клеткам, эритроцитам и сперматозоидам. Последние исследования показывают наличие у уреаплазм нескольких адгезинов.
2. Протеаза IgA человека. Обнаружено, что протеазы U. urealyticum расщепляют IgA человека на 2 фрагмента, по массе соответствующих Fc- и Fab-фрагментам. В результате воздействия протеаз иммуноглобулины теряют способность связывать антигены уреаплазм и предотвращать развитие инфекции.
3. Фосфолипазы. В мембране уреаплазм были обнаружены фосфолипазы А1, А2 и С, причем активность фосфолипазы А2 от 60 до 300 раз выше, чем у фосфолипазы А1. Предполагается, что эти фосфолипазы при инфицировании плода и плаценты гидролизуют фосфолипиды мембраны клеток плаценты, что приводит к увеличению количества свободной арахидоновой кислоты и к активации синтеза простагландинов.
4. Уреаза. Как уже было отмечено выше, U. urealyticum обладают уреазной активностью. При гидролизе мочевины образуется аммиак, который оказывает токсический эффект на клетки-мишени.
Для уреаплазменной инфекции характерна длительная персистенция. U. urealyticum может вызвать острую инфекцию, однако в большинстве случаев наблюдаются латентные формы инфекции. Специфическая терапия способствует купированию клинических признаков, однако элиминации возбудителя часто не происходит, при этом острая форма инфекции переходит в латентную. Персистирующие уреаплазмы могут активироваться под влиянием различных факторов (присоединение инфекции другой этиологии, изменение иммунного статуса организма). Факторами риска инфицирования U. urealyticum являются молодой возраст, низкий социально-экономический статус, раннее начало половой жизни, большое количество половых партнеров, использование оральных контрацептивов, беременность [5].
Статистически достоверных данных о распространенности U. urealyticum в разных странах мира среди различных групп населения очень мало, однако известно, что частота колонизации уреаплазмами мочеполовых органов у женщин значительно выше (до 60%), чем у мужчин. Отдельные исследования позволяют сделать вывод о наличии U. urealyticum у клинически здоровых лиц. Уреаплазмы входят в состав индигенной (облигатной) микрофлоры влагалища с детского возраста. Доказано, что колонизационная частота зависит от сексуальной активности женщины, в подростковом периоде жизни частота выявления возрастает с 8–10% у девушек с отсутствием половых контактов в анамнезе до 23–55,4% после начала половой жизни.
Отдельные исследования позволяют сделать вывод о наличии U. urealyticum у клинически здоровых лиц. Уреаплазмы входят в состав индигенной (облигатной) микрофлоры влагалища с детского возраста. Доказано, что колонизационная частота зависит от сексуальной активности женщины, в подростковом периоде жизни частота выявления возрастает с 8–10% у девушек с отсутствием половых контактов в анамнезе до 23–55,4% после начала половой жизни.
Среди гинекологических больных U. urealyticum выявляется в 49–55% случаев, это может быть связано с наличием клинической симптоматики у женщин и более частым скрининговым обследованием [7, 8]. Уреаплазменная инфекция может сопровождаться воспалительными процессами гениталий, приводящими к бесплодию, прерыванию беременности, преждевременным родам, пренатальной патологии плода, а также вызывать уретриты, простатиты и бесплодие у мужчин [9].
Уреаплазмоз входит в число тех инфекций, на которые женщине следует обследоваться до предполагаемой беременности. Даже незначительное количество микроорганизмов в мочеполовом тракте здоровой женщины во время беременности может активизироваться и привести к развитию уреаплазменной инфекции. В то же время впервые обнаруженный уреаплазмоз во время беременности не является показанием для прерывания беременности, так как уреаплазма не обладает тератогенным действием. Однако уреаплазмоз может быть причиной различных осложнений во время беременности. По данным литературы, заболеваемость новорожденных в неонатальном периоде в результате внутриутробного инфицирования составляет от 5,3 до 32,6%. У новорожденных детей, чаще недоношенных, развиваются острые пневмонии, хронические заболевания легких с бронхолегочной дисплазией, воспалительные заболевания верхних дыхательных путей, конъюнктивиты, менингиты, сепсис [8].
Даже незначительное количество микроорганизмов в мочеполовом тракте здоровой женщины во время беременности может активизироваться и привести к развитию уреаплазменной инфекции. В то же время впервые обнаруженный уреаплазмоз во время беременности не является показанием для прерывания беременности, так как уреаплазма не обладает тератогенным действием. Однако уреаплазмоз может быть причиной различных осложнений во время беременности. По данным литературы, заболеваемость новорожденных в неонатальном периоде в результате внутриутробного инфицирования составляет от 5,3 до 32,6%. У новорожденных детей, чаще недоношенных, развиваются острые пневмонии, хронические заболевания легких с бронхолегочной дисплазией, воспалительные заболевания верхних дыхательных путей, конъюнктивиты, менингиты, сепсис [8].
Следует подчеркнуть, что уреаплазмы редко существуют в виде моноинфекции. Наиболее частыми являются ассоциации с факультативно-анаэробными микроорганизмами, несколько реже – с хламидиями, еще реже – с вирусами. Чаще всего (73–79%) U. urealyticum встречается в ассоциации с Gardnerella vaginalis, реже – с Chlamydia trachomatis (25–30%), M. hominis (21,4%) и другими возбудителями. Частое (до 75–80% случаев) выявление уреаплазм одновременно с анаэробной микрофлорой, возможно, обусловлено способностью G. vaginalis выделять янтарную кислоту, которая используется другими условно-патогенными микроорганизмами. В свою очередь уреаплазмы, активно использующие для своей жизнедеятельности кислород, способствуют усиленному размножению анаэробных бактерий [1, 4]. Частая ассоциация уреаплазм с другими микроорганизмами затрудняет решение вопроса об их роли как основного этиологического фактора или сопутствующего агента, усиливающего патологический процесс.
Чаще всего (73–79%) U. urealyticum встречается в ассоциации с Gardnerella vaginalis, реже – с Chlamydia trachomatis (25–30%), M. hominis (21,4%) и другими возбудителями. Частое (до 75–80% случаев) выявление уреаплазм одновременно с анаэробной микрофлорой, возможно, обусловлено способностью G. vaginalis выделять янтарную кислоту, которая используется другими условно-патогенными микроорганизмами. В свою очередь уреаплазмы, активно использующие для своей жизнедеятельности кислород, способствуют усиленному размножению анаэробных бактерий [1, 4]. Частая ассоциация уреаплазм с другими микроорганизмами затрудняет решение вопроса об их роли как основного этиологического фактора или сопутствующего агента, усиливающего патологический процесс.
Факт передачи уреаплазменной инфекции половым путем не вызывает сомнений. Кроме того, возможен вертикальный механизм передачи, который может привести в некоторых случаях к развитию внутриутробной инфекции плода и заражению контактно-бытовым путем.
Считается, что инкубационный период уреаплазмоза длится около одного месяца. Однако все зависит от исходного состояния здоровья заразившегося человека. Уреаплазма, оказавшись в половых путях или в мочеиспускательном канале, может никак себя не проявлять в течение многих лет. Устойчивость половых органов к воздействию микроорганизмов обеспечивают физиологические барьеры, при этом основным фактором защиты является нормальная микрофлора. Когда нарушается соотношение различных микроорганизмов, уреаплазма начинает быстро размножаться.
По длительности заболевания различают свежий урогенитальный уреаплазмоз (с давностью заражения до 2 месяцев), который может быть острым, подострым, вялотекущим, и хронический (с давностью заражения свыше 2 месяцев), для которого характерно малосимптомное течение. Учитывая частое бессимптомное носительство данной инфекции, с практической точки зрения достаточно трудно определить давность заражения. Диагноз свежего урогенитального уреаплазмоза наиболее достоверен в том случае, когда при исследовании отделяемого из половых путей в течение последних 2 месяцев возбудитель не обнаруживался, а после начала клинических проявлений стал диагностироваться. Кроме того, данный диагноз также может быть правомерен при появлении симптомов воспалительного процесса после начала половой жизни (смены полового партнера, при сексуальном насилии и т.п.) в сочетании с обнаружением возбудителя в диагностически значимых титрах [1, 3].
Кроме того, данный диагноз также может быть правомерен при появлении симптомов воспалительного процесса после начала половой жизни (смены полового партнера, при сексуальном насилии и т.п.) в сочетании с обнаружением возбудителя в диагностически значимых титрах [1, 3].
Диагностика уреаплазменной инфекции базируется на данных лабораторных методов обследования с учетом анамнеза и клинической симптоматики.
При анализе анамнестических данных учитывается возраст пациентки, наличие заболеваний, передающихся половым путем, возраст начала половой жизни, количество половых партнеров и применяемый метод контрацепции. При этом гинекологический анамнез часто отягощен наличием бесплодия и воспалительных заболеваний органов мочеполовой системы, акушерский анамнез – неблагоприятными исходами беременностей, а также высокой частотой инфекционных осложнений.
Следует отметить, что уреаплазмоз проявляется незначительными симптомами, которые мало беспокоят больных, а в большинстве случаев заболевание вообще не проявляется. Пациентки жалуются на появляющиеся время от времени прозрачные выделения из влагалища, мало отличающиеся от нормальных. У некоторых женщин может возникать чувство жжения при мочеиспускании. Если имеется значительное снижение иммунитета, то уреаплазма может продвигаться выше по половым путям, вызывая эндометрит или сальпингоофорит.
Пациентки жалуются на появляющиеся время от времени прозрачные выделения из влагалища, мало отличающиеся от нормальных. У некоторых женщин может возникать чувство жжения при мочеиспускании. Если имеется значительное снижение иммунитета, то уреаплазма может продвигаться выше по половым путям, вызывая эндометрит или сальпингоофорит.
Для достоверной лабораторной диагностики уреаплазмоза сегодня применяют комбинацию из нескольких методов [1, 3, 10]:
1. Полимеразная цепная реакция (ПЦР). Очень быстрый метод, на его проведение необходимо 5 часов. Если ПЦР показывает наличие уреаплазмы в организме больного, это значит, что имеет смысл продолжать проведение диагностики. Отрицательный результат ПЦР почти на 100% означает отсутствие уреаплазмы в организме человека. Однако ПЦР не позволяет определить количественные характеристики возбудителя, поэтому положительный результат при ПЦР не является показанием к назначению лечения, а сам метод не может использоваться для контроля сразу после лечения.
2. Бактериологический (культуральный) метод диагностики. Материал из влагалища, шейки матки, мочеиспускательного канала помещается на питательную среду, где в течение нескольких суток (обычно 48 часов) выращиваются уреаплазмы. Это единственный метод, позволяющий определить количество уреаплазм, что очень важно для выбора дальнейшей тактики. Так, при титре менее 104 КОЕ/мл пациентка считается носителем уреаплазм и лечения чаще всего не требует. Титр более 104 КОЕ/мл требует назначения лекарственной терапии. Этот же метод используется для определения чувствительности уреаплазм к тем или иным антибиотикам перед их назначением, что необходимо для правильного подбора антибактериальной терапии. Обычно такое исследование занимает около 1 недели.
3. Серологический метод (выявление антител). Выявление антител к антигенам уреаплазм применяется при определении причин бесплодия, выкидыша, воспалительных заболеваний в послеродовом периоде.
4. Метод прямой иммунофлюоресценции (ПИФ) и иммунофлюоресцентный анализ (ИФА). Они довольно широко распространены из-за относительно невысокой стоимости и простоты исполнения, но точность их невелика (около 50–70%).
Они довольно широко распространены из-за относительно невысокой стоимости и простоты исполнения, но точность их невелика (около 50–70%).
Показаниями к терапии инфекций, вызванных Ureaplasma spp., являются:
- клинические и лабораторные признаки воспаления органов мочеполовой системы;
- предстоящие инвазивные манипуляции в области органов мочеполовой системы;
- отягощенный акушерско-гинекологический анамнез;
- осложненное течение настоящей беременности.
Лечение уреаплазмоза, как правило, проводится амбулаторно. Поскольку возбудитель данного заболевания очень легко приспосабливается к различным антибиотикам, порой даже несколько курсов лечения не приносят результата. Помочь в выборе препарата может микробиологическое исследование на уреаплазмы с определением чувствительности к антибиотикам. У небеременных женщин используют препараты тетрациклинового ряда (тетрациклин, доксициклин), фторхинолоны (офлоксацин, пефлоксацин) и макролиды (азитромицин, джозамицин, кларитромицин). При беременности можно применять лишь некоторые из макролидов, а препараты тетрациклинового ряда и фторхинолоны противопоказаны [11, 12]. В последнее время в литературе появились данные о снижении чувствительности генитальных микоплазм к фторхинолонам и тетрациклинам, в связи с чем их применение не рекомендуется. Эффективность местной терапии и иммунотерапии в настоящее время не доказана [13].
При беременности можно применять лишь некоторые из макролидов, а препараты тетрациклинового ряда и фторхинолоны противопоказаны [11, 12]. В последнее время в литературе появились данные о снижении чувствительности генитальных микоплазм к фторхинолонам и тетрациклинам, в связи с чем их применение не рекомендуется. Эффективность местной терапии и иммунотерапии в настоящее время не доказана [13].
Антибиотиком, получившим наиболее широкое распространение для лечения урогенитального уреаплазмоза, в настоящее время является джозамицин (Вильпрафен®). Вильпрафен® рекомендован ведущими российскими экспертами в качестве препарата первого ряда для лечения уреаплазменной и микоплазменной инфекции. В исследованиях in vitro джозамицин демонстрирует наивысшую активность в отношении уреаплазм в сравнении с другими макролидами. Кроме того, следует отметить, что джозамицин (Вильпрафен®) является единственным разрешенным препаратом для приема во время беременности [11, 14].
Вильпрафен® – это антибиотик группы макролидов, механизм действия которого связан с нарушением синтеза белка в микробной клетке вследствие обратимого связывания с 50S-субъединицей рибосомы. В терапевтических концентрациях, как правило, он оказывает бактериостатическое действие, замедляя рост и размножение бактерий, а при создании в очаге воспаления высоких концентраций оказывает бактерицидный эффект.
В отличие от многих других антибиотиков Вильпрафен® хорошо проникает внутрь клеток и создает высокие внутриклеточные концентрации, что имеет важное значение при лечении инфекций, вызванных внутриклеточными патогенами. Существенным является также то, что данный антибиотик способен проникать внутрь фагоцитарных клеток, таких как макрофаги, фибробласты, полиморфноядерные гранулоциты, и с ними транспортироваться в воспалительный очаг [14, 15].
После приема внутрь Вильпрафен® быстро абсорбируется из желудочно-кишечного тракта, при этом максимальная концентрация достигается через 1–2 ч после приема. Через 45 мин после приема дозы 1 г средняя концентрация джозамицина в плазме составляет 2,41 мг/л. Связывание с белками плазмы не превышает 15%. Прием препарата с интервалом в 12 ч обеспечивает сохранение эффективной концентрации джозамицина в тканях в течение суток. Равновесное состояние достигается через 2–4 дня регулярного приема. Кроме того, он хорошо проникает через биологические мембраны и накапливается в различных тканях: в легочной, лимфатической ткани небных миндалин, органов мочевыделительной системы, коже и мягких тканях [13, 14].
Через 45 мин после приема дозы 1 г средняя концентрация джозамицина в плазме составляет 2,41 мг/л. Связывание с белками плазмы не превышает 15%. Прием препарата с интервалом в 12 ч обеспечивает сохранение эффективной концентрации джозамицина в тканях в течение суток. Равновесное состояние достигается через 2–4 дня регулярного приема. Кроме того, он хорошо проникает через биологические мембраны и накапливается в различных тканях: в легочной, лимфатической ткани небных миндалин, органов мочевыделительной системы, коже и мягких тканях [13, 14].
Рекомендуемая схема лечения джозамицином: 500 мг 3 р/сут 7–10 дней. Данный препарат характеризуется доказанной эффективностью в отношении хламидийных, уреаплазменных и микоплазменных инфекций урогенитального тракта, а также благоприятным профилем безопасности (отсутствием патологического влияния на моторику и микрофлору кишечника, минимальным риском лекарственных взаимодействий).
На время лечения необходимо воздерживаться от половых сношений (в крайнем случае обязательно пользоваться презервативом), соблюдать диету, исключающую употребление острой, соленой, жареной, пряной и другой раздражающей пищи, а также алкоголь. Через две недели после окончания антибактериальной терапии проводится первый контрольный анализ. Если его результат отрицательный, через месяц выполняется еще один контрольный анализ.
Через две недели после окончания антибактериальной терапии проводится первый контрольный анализ. Если его результат отрицательный, через месяц выполняется еще один контрольный анализ.
Методы профилактики уреаплазмоза не отличаются от методов профилактики заболеваний, передающихся половым путем. Прежде всего это использование презерватива при половых контактах и избегание случайных половых связей [1, 5].
Таким образом, выбор антибиотика при уреаплазменной инфекции должен основываться на результатах микробиологических исследований отделяемого женских половых органов. Совершенствование диагностических тестов по выявлению как специфических, так и неспецифических возбудителей позволит добиться максимальных результатов антибактериальной терапии у данной категории пациентов. Своевременное назначение Вильпрафена позволяет добиться излечения уреаплазмоза в 97,5% случаев. Высокая клиническая эффективность Вильпрафена обусловливает высокую значимость этого антибиотика для лечения заболеваний, передаваемых половым путем.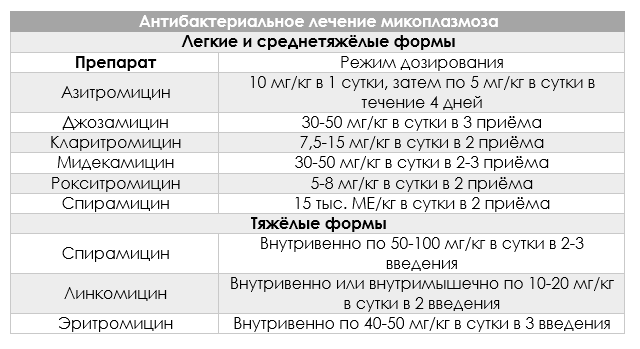
— Объяснение тестов на патологию
Крысы COVID-19 являются примером таких типов тестов, но нас интересуют многие другие, представленные на рынке.
Университет Вуллонгонга проводит небольшое исследование о них, и мы хотели бы услышать от вас, использовали ли вы их или рассматривали возможность использования.
Просто заполните краткий опрос по адресу:
https://uow.au1.qualtrics.com/jfe/form/SV_eeodpzn8lgSsAbI
Отсюда мы можем пригласить вас принять участие в платном собеседовании.
За дополнительной информацией обращайтесь к доктору Патти Ши: [email protected]
Найдите объяснение своего теста на патологию
Ключевое слово:
Название теста Тесты…Все тесты и синонимыТест не указан?1,5-AG1,5-ангидроглюцитол17-гидроксипрогестерон5HIAAАцетилхолиновый рецептор мочиАтБкислотная культура быстрых палочекАКТГАктивированное частичное тромбопластиновое времяAFBAЛанинаминотрансфераза (АЛТ)АльбуминСоотношение альбумин/креатинин в моче Альдостерон и ренинМутация ALK (генная перестройка)Щелочная фосфатаза (ALP)Альфа-1-антитрипсинАльфа-фетопротеин (АФП)Альфа-гал антителаАминокислотыАммиакАмилазаАНЦА/МПО/PR3 АнтителаАнгиотензинпревращающий ферментАнтенатальная группа и скринингУровни анти-ХаАнти-бета2 гликопротеин 1Идентификация антителАнтимюллеров гормонАнтинуклеарные антителаАнтифосфолипидные антителаАнтистрептолизин О ТитрАнтит rombinАполипопротеин А-IAполипопротеин ВАполипопротеин Е генотипированиеАрбовирусное тестированиеАСОТАспартатаминотрансфераза (AST)ASTАутоантителаB12Культура бактериальной раныB-клеточный иммуноглобулин Реаранжировка гена BCR-ABL1Бета-2 гликопротеин 1 АнтителаБета-2-микроглобулинБета-2-трансферринБикарбонатБилирубинПосев кровиАнализ мазка кровиГазы кровиГруппа кровиСкрининг группы крови на антителаАнализ биологических жидкостейМаркеры костейБиопсия костного мозгаBordetella pertussisBRAF V 600 MutationBrain натрийуретический пептид (BNP или NT-proBNP )BRCA1 и BRCA2C diffCA 15-3CA 19-9CA-125ЦерулоплазминКальцитонинКальцийКальпротектин фекалийКарбамазепинКарциноэмбриональный антиген (СЕА)Оценка сердечного рискаКардиолипин AbКатехоламины, плазма и мочаCBCCBC, CBE, CBPCD4 countCentromere AbИсследование спинномозговой жидкостиСкрининг шейки матки Тест на мутацию гена CFChlamydia trachomatisChlorideCholesterolCholinesteraseChromogranin AХромосомные исследованияCK-MBClostridium difficileCO2Факторы свертывания Анализы на целиакиюКомплементМедьКортизолCOVID-19C-пептидC-реактивный белокC-реактивный белок высокий чувствительностьКреатинкиназаКреатининКреатинин мочиКроссматчКриоглобулинПосев и чувствительность, мочаЦиклический цитруллинированный пептид AbЦиклоспоринЦистатин CЦитомегаловирусD-димерДегидроэпиандростерона сульфат (ДГЭАС)Аутоантитела, связанные с диабетомДифференциал — лейкоцитыДигоксинПрямой антиглобулиновый тестдвухцепочечная ДНК AbСкрининг злоупотребления наркотикамиE/L Тестирование мутаций FTeGFREGFRЭлектролитыЭлектрофорезЭкстренная помощь и тестирование на передозировку Антитела к вирусу Эпштейна-БаррСкорость оседания эритроцитовЭритропоэтинЭтанолEUCEExtractable Nuclear Antigen Antibody PanelFactor V Leiden and PT 20210 Мутация Фекальная эластазаСемейная гиперхолестеринемия (СГ) генетическое тестированиеFBC, FBE, FBPФерритинФибриногенFMR1 МутацииФолатФолликулостимулирующий гормон (ФСГ)Фрагильный ген XСвободные легкие цепиСвободный T3Свободный T4Свободный тироксин (FT4)Свободный трийодтионин (FT3)ФруктозаминПолный анализ кровиГрибковые тестыГамма-глутамилтрансферазаГастринГенетическое тестированиеПолногеномный микрочиповый анализГГТГлюкозаГлюкоза -6-фосфатдегидрогеназаГликоМаркаОкрашивание по ГрамуГормон ростаГематокритГемоглобинВарианты гемоглобинаГаптоглобинHbA1chCGHDL-холестеринHelicobacter pyloriВирус гепатита АВирус гепатита ВВирус гепатита СHER2Наследственные патогенные варианты при колоректальном раке и раке эндометрияHerpes simplex 1 и 2 Мутации вируса простого герпеса 1 и 2HFEВИЧ антиген/антителоВИЧ генотип pic резистентностьВИЧ p24 Ag Вирусная нагрузка ВИЧТестирование HLAHLA-B27Статус гена HLAB5701 Домашние тестыГомоцистеинСтатус рецепторов гормоновХорионический гонадотропин человекаЧеловек вирус папилломыИФР-1Иммуноглобулин Е общийИммуноглобулиныИммунофенотипированиеИммунореактивный трипсинСкрининг на инфекционный мононуклеозТесты на гриппИнгибинINRIИнсулинИонизированный кальцийЖелезоИсследования железаМутация IRTJAK2 Функциональные тесты почекАнализ почечных камней ипазаЛипидыЛипопротеин (а)Электрофорез липопротеиновЛитийФункциональные тесты печениПеченочная панельВолчаночный антикоагулянтЛютеинизирующий гормон (ЛГ)Серология болезни ЛаймаМагнийСкрининг материMCHMCHCMCVКорь и эпидемический паротит тестыРтутьМезотелинМетанефрин в моче 24 часаМетанефриныСкрининг на метициллин-устойчивый золотистый стафилококкМикроальбуминМикрочиповый тестМикросателлитная нестабильность (MSI)Митохондрии AbMPL МутацияMTHFR МутацияМикофенилатМикоплазмаМиоглобинNeisseria gonorrhoeaeНикотин/котининНИПТ — неинвазивное пренатальное тестированиеСкрытая кровь в фекалияхЭстрадиол Органические кислотыОсмоляльностьЯйцеклетки и паразитыЯйцеклетки, кисты и паразитыМазок ПапаниколауPAPP-AПарацетамолПаратиреоидный гормонПарвовирус B19PDGFRA-FIP1L1 генная перестройка Анализ перикардиальной жидкостиАнализ перитонеальной жидкостиФармакогеномные тестыФенобарбФенобарбиталФенитоинФосфатФосфорСвободный от плазмы метанефринПодсчет тромбоцитовТест тромбоцитов Функциональный анализ плевральной жидкостиPMP22 GeneПорфириныКалийПреальбуминТест на беременностьПрокальцитонинПрогестеронПролактинПростатспецифический антиген ( ПСА)Электрофорез белков и иммунофиксацииПротеин С и белок SПротеин мочиПротромбиновое времяPSEN1PTPTHRAS Мутация генаRASTRBCRDWПодсчет эритроцитовСкрининг эритроцитов на антителаЭроцитарные индексыГен ренинаRETПодсчет ретикулоцитовРевматоидный факторТестирование на риккетсиозыRSVКраснуха тест на вирусСалицилатАнализ спермыСеротонин в цельной кровиГлобулин, связывающий половые гормоны (ГСПГ)Серповидноклеточная анемияСиролимусГладкие мышцы AbSMRPSНатрийТестирование гена соматической опухолиПосев мокротыПосев на стрептококковую ангинуТестирование на чувствительностьТест хлорида потаТест хлорида потаТест SynacthenСиновиальная жидкостьСерология сифилисаT3T4ТакролимусРеаранжировка гена Т-клеточного рецептораТестостеронТерапия Мониторинг тиковТиопуринметилтрансферазаТироглобулинАнтитела щитовидной железыТест функции щитовидной железыТиреостимулирующий гормон (ТТГ)Тест TORCHОбщий белокToxoplasma gondiiТрансферринТрансферрин и Обнаружение TIBC Trichomonas vaginalisТриглицериды (натощак или случайным образом)Тропонин (I или T)Трипсин в фекалияхТрипсиногенТриптазаТуберкулезные скрининговые тестыОпухолевые маркерыU&EUНевалидированные тестыМочевинаМочевая кислотаАнализ мочиПосев мочиПосев мочиM/C/SВальпроатВанкомицинВирус ветряной оспы Мутация гена VHLВитамин B12 и фолиевая кислотаВитамин D 25 OHvon Willebrand Factor Подсчет лейкоцитов Полный геном или полный экзом Тестирование в детском возрасте СиндромыЦинковый протопорфирин
Состояние/заболевание
Состояния.
