Содержание
Nestogen-1 сухая молочная смесь 600г (0+)
Смесь Nestogen 1 была специально разработана для обеспечения сбалансированного здорового питания и комфортного пищеварения малыша. Смесь Nestogen 1 с пребиотиками и уникальными лактобактериями L.reuteri способствует улучшению моторики кишечника, формированию регулярного мягкого стула, полезной микрофлоры и предотвращению колик. Здоровая кишечная микрофлора необходима для поддержания, развития и укрепления иммунитета.
Лютеин и омега-3 ПНЖК способствуют развитию мозга. Смесь содержит сбалансированный комплекс витаминов и минеральных веществ для гармоничного роста и развития.
Смесь Nestogen 1 отличается преобладанием белков молочной сыворотки для улучшения качества белка и обеспечению комфортного пищеварения. Смесь Nestogen 1 предназначена для кормления здоровых детей с рождения в случаях, когда грудное вскармливание невозможно, и является молочной составляющей рациона ребенка.
Состав: Обезжиренное молоко, деминерализованная молочная сыворотка, лактоза, мальтодексин, смесь растительных масел (низкоэруковое рапсовое, подсолнечное, подсолнечное высокоолеиновое, кокосовое), молочный жир, пребиотики (галактоолигосахариды (ГОС) и фруктоолигосахариды (ФОС)), цитрат кальция,эмульгатор ( соевый лецитин), цитрат калия, цитрат натрия, фосфат калия, хлорид магния, витаминный комплекс(С (L-аскорбат натрия,У(DL-альфа-токоферолла ацетат), PP (никотинамид),D-пантотенат кальция,аскорбилпальмитат ©, DL-альфа-токоферолла ацетат (Е), никотинамид (PP), D-пантотенат кальция, B1 (тиамина мононитрат), А (ретинола ацетат), B6 (пиридоксин гидрохлорид), B2 (рибофлавин), фолиевая кислота (B9),R (фитоменадион), Д-биотин,Д3 (холекальциферол), B12 (цианкобламин)),хлорид калия, хлорид натрия, рыбий жир, культура лактобактерий L. 6 КОЕ/г), таурин,инозит, сульфат железа, сульфат цинка,нуклеотиды, L-карнитин, сульфат меди, сульфат марганца, йодид калия, лютеин, селенат натрия.
6 КОЕ/г), таурин,инозит, сульфат железа, сульфат цинка,нуклеотиды, L-карнитин, сульфат меди, сульфат марганца, йодид калия, лютеин, селенат натрия.
Важное примечание: Идеальной пищей для грудного ребенка является молоко матери. Перед тем как принять решение об искусственном вскармливании с использованием детской смеси, обратитесь за советом к медицинскому работнику. Возрастные ограничения указаны на упаковке товаров в соответствии с законодательством РФ. Продукт изготовлен из сырья, произведенного специально одобренными поставщиками, без использования генетически модифицированных ингредиентов, консервантов и красителей. Переход на новую смесь должен осуществляться постепенно.
Примечание: Для сохранения живых бактерий вскипяченную воду следует остудить примерно до температуры тела (37 ?С) и затем добавить сухую смесь. Для приготовления смеси необходимо использовать мерную ложку, заполненную без горки. Разведение неправильного количества порошка большего или меньшего по сравнению с количеством, указанным в таблице может привести к обезвоживанию организма ребенка или нарушению его питания. Указанные пропорции нельзя изменять без совета медицинского работника. В этом возрасте питание ребенка становится более разнообразным (постепенно вводятся каши, овощи, фрукты, мясо и рыба). Проконсультируйтесь с медицинским работником, прежде чем вводить прикорм в меню ребенка. Если раннее введение продуктов прикорма рекомендовано вашим доктором, то уменьшите количество потребления детской смеси согласно рекомендации.
Указанные пропорции нельзя изменять без совета медицинского работника. В этом возрасте питание ребенка становится более разнообразным (постепенно вводятся каши, овощи, фрукты, мясо и рыба). Проконсультируйтесь с медицинским работником, прежде чем вводить прикорм в меню ребенка. Если раннее введение продуктов прикорма рекомендовано вашим доктором, то уменьшите количество потребления детской смеси согласно рекомендации.
NESTOGEN 1 Prebio, 0-6 мес., картон 1050г
Смесь Nestogen 1 была специально разработана для обеспечения сбалансированного здорового питания и комфортного пищеварения малыша. Смесь Nestogen 1 с пребиотиками и уникальными лактобактериями L.reuteri способствует улучшению моторики кишечника, формированию регулярного мягкого стула, полезной микрофлоры и предотвращению колик. Здоровая кишечная микрофлора необходима для поддержания, развития и укрепления иммунитета.
Лютеин и омега-3 ПНЖК способствуют развитию мозга. Смесь содержит сбалансированный комплекс витаминов и минеральных веществ для гармоничного роста и развития.
Смесь Nestogen 1 отличается преобладанием белков молочной сыворотки для улучшения качества белка и обеспечению комфортного пищеварения. Смесь Nestogen 1 предназначена для кормления здоровых детей с рождения в случаях, когда грудное вскармливание невозможно, и является молочной составляющей рациона ребенка.
!Переход на новую смесь должен осуществляться постепенно!
ВНИМАНИЕ! Товар представлен в старом и новом дизайнах упаковок, вариант в поставке не гарантирован!
Состав смеси в новом дизайне упаковки: Обезжиренное молоко, деминерализованная молочная сыворотка, лактоза, мальтодексин, смесь растительных масел (низкоэруковое рапсовое, подсолнечное, подсолнечное высокоолеиновое, кокосовое), молочный жир, пребиотики (галактоолигосахариды (ГОС) и фруктоолигосахариды (ФОС)), цитрат кальция,эмульгатор ( соевый лецитин), цитрат калия, цитрат натрия, фосфат калия, хлорид магния, витаминный комплекс(С (L-аскорбат натрия,У(DL-альфа-токоферолла ацетат), PP (никотинамид),D-пантотенат кальция,аскорбилпальмитат (С), DL-альфа-токоферолла ацетат (Е), никотинамид (PP), D-пантотенат кальция, B1 (тиамина мононитрат), А (ретинола ацетат), B6 (пиридоксин гидрохлорид), B2 (рибофлавин), фолиевая кислота (B9),R (фитоменадион), Д-биотин,Д3 (холекальциферол), B12 (цианкобламин)),хлорид калия, хлорид натрия, рыбий жир, культура лактобактерий L. 5 КОЕ/г), таурин, сульфат железа, инозит, сульфат цинка, L-картнитин, сульфат меди, сульфат марганца, йодид калия, селенат натрия.
5 КОЕ/г), таурин, сульфат железа, инозит, сульфат цинка, L-картнитин, сульфат меди, сульфат марганца, йодид калия, селенат натрия.
ВАЖНОЕ ПРИМЕЧАНИЕ. Идеальной пищей для грудного ребенка является молоко матери. Перед тем как принять решение об искусственном вскармливании с использованием детской смеси, обратитесь за советом к медицинскому работнику. Возрастные ограничения указаны на упаковке товаров в соответствии с законодательством РФ. Продукт изготовлен из сырья, произведенного специально одобренными поставщиками, без использования генетически модифицированных ингредиентов, консервантов и красителей.
Переход на новую смесь должен осуществляться постепенно.
Примечание: Для сохранения живых бактерий вскипяченную воду следует остудить примерно до температуры тела (37 ̊С) и затем добавить сухую смесь. Для приготовления смеси необходимо использовать мерную ложку, заполненную без горки. Разведение неправильного количества порошка большего или меньшего по сравнению с количеством, указанным в таблице может привести к обезвоживанию организма ребенка или нарушению его питания. Указанные пропорции нельзя изменять без совета медицинского работника. В этом возрасте питание ребенка становится более разнообразным (постепенно вводятся каши, овощи, фрукты, мясо и рыба). Проконсультируйтесь с медицинским работником, прежде чем вводить прикорм в меню ребенка. Если раннее введение продуктов прикорма рекомендовано вашим доктором, то уменьшите количество потребления детской смеси согласно рекомендации.
Указанные пропорции нельзя изменять без совета медицинского работника. В этом возрасте питание ребенка становится более разнообразным (постепенно вводятся каши, овощи, фрукты, мясо и рыба). Проконсультируйтесь с медицинским работником, прежде чем вводить прикорм в меню ребенка. Если раннее введение продуктов прикорма рекомендовано вашим доктором, то уменьшите количество потребления детской смеси согласно рекомендации.
Объяснение урока: Смеси | Nagwa
В этом эксплейнере мы научимся определять и описывать различные типы смеси и их физические свойства.
Химия изучает материю, любой материал, который имеет как массу, так и объем. Материю можно далее классифицировать как чистое вещество или смесь. Такие элементы, как алюминий (Al),
углерод (C) и железо
(Fe) являются чистыми веществами. Когда элементы
химически связывать друг с другом такие соединения, как вода
(НО2),
углекислый газ (CO2) и хлорид натрия
(NaCl). Соединения также
относятся к чистым веществам.
Когда два или более вещества, элемента или соединения физически объединены а не химически, образуется смесь. Чтобы классифицироваться как смесь, вещества должны сохранять их различные личности и должны быть в состоянии быть отделены друг от друга физическими средствами. Примеры смесей включают воздух, молоко, соленую воду, и цемент.
Определение: Смесь
Смесь – это соединение двух или более веществ физическими средствами в в которых вещества сохраняют свою отличительную идентичность.
На рисунке ниже показаны различные атомы, соединения и смеси на молекулярном уровень.
Пример 1. Определение определения смеси
Какое из следующих утверждений лучше всего описывает смесь?
- Химическая комбинация двух или более веществ
- Молекула, состоящая из различных типов атомов
- Нехимическая комбинация двух или более веществ
- Вещество, состоящее только из одного типа атома или молекулы
- Комбинация двух веществ в различных физических состояниях
Ответ
Смесь – это комбинация двух или более веществ. выбор ответа
D не может описать смесь, так как присутствует только один тип атома или молекулы. Кроме того, чтобы быть смесью, вещества должны быть физически смешаны, а не
химически объединены. Мы можем исключить варианты ответов A и B, поскольку они
описать химические соединения. В то время как физические состояния веществ
объединенные в смесь, могут быть другими, как в смеси, образованной, когда соль
растворяется в воде, физические состояния могут быть такими же, как в смеси
образуется при смешивании молока с кофе. Таким образом, мы можем исключить ответ
выбор E. Утверждение, которое лучше всего описывает смесь, это ответ
выбор С.
выбор ответа
D не может описать смесь, так как присутствует только один тип атома или молекулы. Кроме того, чтобы быть смесью, вещества должны быть физически смешаны, а не
химически объединены. Мы можем исключить варианты ответов A и B, поскольку они
описать химические соединения. В то время как физические состояния веществ
объединенные в смесь, могут быть другими, как в смеси, образованной, когда соль
растворяется в воде, физические состояния могут быть такими же, как в смеси
образуется при смешивании молока с кофе. Таким образом, мы можем исключить ответ
выбор E. Утверждение, которое лучше всего описывает смесь, это ответ
выбор С.
Когда два или более вещества объединяются, образуя смесь, имеющую однородную
По составу смесь можно отнести к гомогенной. Приставка «гомо-» означает то же самое и указывает на то, что
состав и свойства смеси везде одинаковые. Однородную смесь также называют раствором.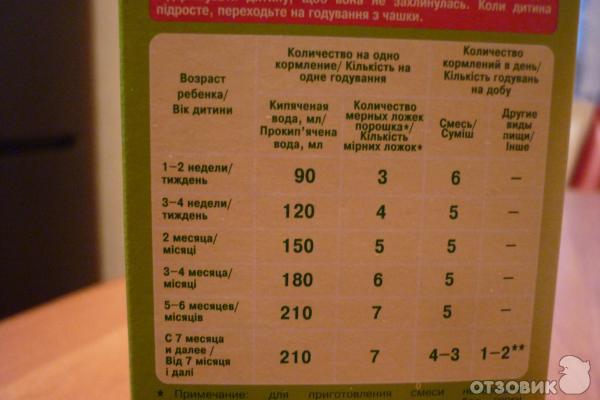
Определение: Однородная смесь
Однородная смесь – это смесь с однородным составом. Это также часто называют решением.
Соленая вода является примером гомогенного раствора. Смесь состоит из хлорид натрия (NaCl) и вода (HO2). После объединения получается смесь однородна по всему объему и соль не различима из воды.
Другим примером гомогенной смеси является воздух. Воздух состоит из азота, кислород, аргон, углекислый газ, водяной пар и другие газы. Состав воздуха однороден, и различные газы не могут быть отличающиеся друг от друга.
Раствор состоит из растворителя, основного компонента и растворенных веществ, второстепенные компоненты. Растворенное вещество также может быть описано как вещество который растворяется, в то время как растворитель описывается как вещество, которое делает растворение.
Определение: Растворитель
Растворитель – это основной компонент раствора, в который вводятся другие вещества. раствориться.
раствориться.
Определение: Растворенное вещество
Растворенное вещество – это второстепенный компонент раствора, описываемого вещества. как растворяющийся.
В примере с соленой водой соль является растворенным веществом, а вода — растворителем. В воздухе азот является растворителем, так как он составляет 78% от общего количества. состав смеси. Поэтому, рассматривая воздух как смесь, кислород, аргон, углекислый газ и водяной пар считаются быть растворенными веществами.
Мы часто думаем о растворах как о жидкостях, состоящих из твердого вещества, растворенного в воде, но растворенное вещество и растворитель могут быть твердыми, жидкими или газообразными. Примеры различных решения приведены в таблице ниже.
| Types of Solutions | ||||
|---|---|---|---|---|
| State of Solute | State of Solvent | State of Solution | Example | |
| Gas | Gas | Gas | Air | |
| Gas | Liquid | Жидкость | Безалкогольные напитки | |
| Жидкость | Жидкость | Жидкость | Этанол в воде | |
| Жидкость | 760076 | Жидкость | Соленая вода | |
| Газ | Сплошные | Сплошные | (H3) в палладие или платине | |
| Liquid | ||||
| Liquid | ||||
| Liquid | ||||
| Liquid | .||||
| Твердый | Твердый | Твердый | Сплавы, такие как латунь (Zn растворен в Cu) | |
Пример 2. Определение физического состояния растворенного вещества и растворителя в атмосферных условиях Воздух
Заполните пропуски: Атмосферный воздух – это раствор, в котором физическое состояние растворенного вещества и физическое состояние растворителя.
Ответ
Раствор – это гомогенная смесь, состоящая из одного или нескольких растворенных веществ.
растворяется в растворителе. Растворитель является основным компонентом раствора,
а растворенное вещество является второстепенным компонентом раствора. Решение в
Вопрос атмосферный воздух. Атмосферный воздух в основном состоит из азота,
кислород и аргон с приблизительным процентным составом
78%, 21%,
и 1% соответственно. Это означает, что азот является растворителем. тогда как кислород и аргон являются растворенными веществами. И растворитель, и растворенные вещества находятся в
газообразное состояние. Следовательно, мы должны заполнить оба пробела в вопросе
со словом газ .
тогда как кислород и аргон являются растворенными веществами. И растворитель, и растворенные вещества находятся в
газообразное состояние. Следовательно, мы должны заполнить оба пробела в вопросе
со словом газ .
Только определенное количество растворенного вещества может быть растворено в растворителе при данной температура. Растворы, содержащие максимально возможное количество растворенного вещества. растворенные в растворителе при определенной температуре, называются насыщенными решения.
Определение: насыщенный раствор
Насыщенный раствор – это раствор, содержащий максимальное количество растворенного вещества. растворяется в растворителе при данной температуре.
Если в растворителе растворено меньше максимального количества растворенного вещества при определенной температуры раствор считается ненасыщенным.
Определение: ненасыщенный раствор
Ненасыщенный раствор – это раствор, содержащий меньше максимального количества
растворенное вещество, растворенное в растворителе при данной температуре.
Возможно превышение максимального количества растворенного вещества, которое должно быть в растворителе способен содержать. При нагревании насыщенного раствора растворитель может растворить больше растворенного вещества. После растворения дополнительного растворенного вещества раствор медленно охлаждается до исходной температуры. Полученный охлажденный раствор содержит больше, чем максимальное количество растворенного вещества и называется перенасыщенным решение.
Определение: Перенасыщенный раствор
Перенасыщенный раствор – это раствор, который содержит больше максимального количества растворенного вещества, чем должно быть растворено в растворителе при данной температуре.
Пересыщенные растворы нестабильны. Легкие вибрации или частицы пыли могут вызвать кристаллизацию избыточного растворенного вещества и
выпадает в осадок из раствора. Например, многоразовая грелка для рук содержит перенасыщенный раствор ацетата натрия.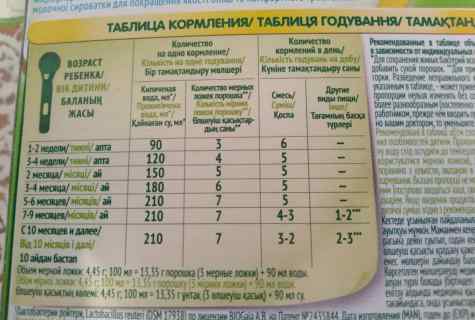 Когда диск внутри мешочка взбалтывается, избыток ацетата натрия выпадает из раствора в виде белых кристаллов и выделяется тепло.
Когда диск внутри мешочка взбалтывается, избыток ацетата натрия выпадает из раствора в виде белых кристаллов и выделяется тепло.
Пример 3: Описание типа раствора, полученного растворением ацетата натрия в воде
В эксперименте студент добавил ацетат натрия к фиксированному объему воды. В конце концов, студент достиг точки, в которой больше не было натрия. ацетат растворился. Затем студент нагревал раствор до тех пор, пока кристаллы не исчезли. ацетата натрия были видны. Затем раствору давали остыть немного. На диаграмме ниже показаны наблюдения студента.
- Какой из следующих терминов описывает раствор B?
- Коллоидный
- Насыщенный
- Супернатный
- Перенасыщенный
- Ненасыщенный
- Какой из следующих терминов описывает раствор D?
- Colloidal
- НЕВЕРТИРОВАННАЯ
- Насыщенные
- SuperNate
- .
 Сверхедренные
Сверхедренные
Ответ
Часть 1
Решение является гомодной микрой, что Solisty One One One One Or SoliStist Or SoliStiest Or SoliStist Or SoliStist SoliStios Mixctore One Or Solistory Solistry Mociestues. растворяется в растворителе. Растворитель является основным компонентом раствора. а растворенное вещество является второстепенным компонентом раствора. В этом примере ацетат натрия является растворенным веществом, а вода является растворителем.
При приготовлении растворов растворитель может растворять только определенное количество растворенного вещества при данной температуре. Когда максимальное количество растворенного вещества было растворяется в растворителе при желаемой температуре, раствор считается насыщенным. Когда количество растворенного вещества меньше максимального растворяется в растворителе, раствор считается ненасыщенным.
В начале эксперимента к раствору А ацетата натрия добавляют
фиксированный объем воды. Первоначально можно было увеличить количество ацетата натрия.
растворенный. Это означает, что раствор был ненасыщенным. В конце концов,
была достигнута точка, когда больше не растворялся ацетат натрия, раствор B. Максимальное количество ацетата натрия было растворено в воде. Раствор B можно охарактеризовать как насыщенный, вариант ответа B.
Первоначально можно было увеличить количество ацетата натрия.
растворенный. Это означает, что раствор был ненасыщенным. В конце концов,
была достигнута точка, когда больше не растворялся ацетат натрия, раствор B. Максимальное количество ацетата натрия было растворено в воде. Раствор B можно охарактеризовать как насыщенный, вариант ответа B.
Часть 2
Когда в растворителе растворено больше максимального количества растворенного вещества при данной температуре раствор считается пересыщенным. Повышение температуры растворителя часто позволяет растворить больше растворенного вещества. растворенный. Если полученный раствор охлаждать медленно, избыток растворенного вещества может оставаться в растворителе, образуя пересыщенный раствор.
В эксперименте раствор Б нагревали до тех пор, пока избыток ацетата натрия
кристаллы растворились, раствор C. Затем раствору дали остыть,
раствор D. Обратите внимание, что в растворе отсутствуют кристаллы ацетата натрия.
раствор D. Это означает, что избыток ацетата натрия все еще растворен в
растворитель. Раствор D можно охарактеризовать как перенасыщенный, вариант ответа E.
Обратите внимание, что в растворе отсутствуют кристаллы ацетата натрия.
раствор D. Это означает, что избыток ацетата натрия все еще растворен в
растворитель. Раствор D можно охарактеризовать как перенасыщенный, вариант ответа E.
Некоторые растворенные вещества при растворении в воде ионизируются или диссоциируют на ионы. Эти растворенные вещества называются электролитами, потому что полученный раствор проводит электричество.
Определение: Электролит
Электролит – это вещество со свободно движущимися ионами, которое может проводить электричество при расплавлении или растворении в воде.
Электролиты могут быть сильными или слабыми. Сильные электролиты – это растворенные вещества, полностью ионизируются или диссоциируют при растворении в воде. Примеры включают ионные хлорид натрия (NaCl) и полярный ковалентная соляная кислота (HCl): NaCl()Na()+Cl()HCl()H()+Cl()saqaqgaqaqHO()HO()22ll+-+-
Ионы (H+) не остаются свободными в растворе
и усваиваются молекулами воды, образуя ионы гидроксония
(НО3+). Химическое уравнение для
ионизация (HCl) выше часто используется для
сократите реакцию, хотя приведенное ниже химическое уравнение является более точным:
HCl()+HO()HO()+Cl()aqlaqaq23+–
Химическое уравнение для
ионизация (HCl) выше часто используется для
сократите реакцию, хотя приведенное ниже химическое уравнение является более точным:
HCl()+HO()HO()+Cl()aqlaqaq23+–
Слабые электролиты – это растворенные вещества, которые лишь частично диссоциируют при растворении в воды. Примером может служить уксусная кислота. (CHCOOh4). Обратите внимание, что в приведенном ниже уравнении стрелка равновесия (⇌) используется в место стрелки вперед (→) чтобы указать, что только некоторые из молекул уксусной кислоты ионизируются: CHCOOH()+HO()CHCOO()+HO()323–3+llaqaq
Растворенные вещества, не образующие ионов при растворении в воде, называются неэлектролиты.
Определение: Неэлектролит
Неэлектролит – это вещество, не имеющее свободно движущихся ионов, которые может проводить электричество при расплавлении или растворении в воде.
Сахар является примером неэлектролита. Сахар растворяется в воде, образуя
раствор, но молекулы сахара не ионизируются. Следовательно, в результате
раствор не проводит электричество.
Сахар растворяется в воде, образуя
раствор, но молекулы сахара не ионизируются. Следовательно, в результате
раствор не проводит электричество.
Тестер электропроводности представляет собой простое устройство, состоящее из лампочки, электроды и источник питания. Когда электроды помещаются в раствор содержащий электролит, электрический ток может течь через раствор к замкните цепь, и лампочка загорится. Лампочка будет ярче загорается, когда тестер проводимости помещен в раствор, содержащий слабый электролит а затем помещают в раствор, содержащий сильный электролит. Если электроды поместить в раствор, содержащий неэлектролит, электрический ток не сможет течь, и лампочка не будет производить свет. Показано использование тестера проводимости в трех различных растворах. на рисунке ниже.
Пример 4. Определение того, какое из трех веществ является сильным электролитом
Показаны три различных раствора. В каком растворе содержится сильное
электролит?
В каком растворе содержится сильное
электролит?
Ответ
Электролит – это вещество, проводящее электричество при растворении в воды. Это связано с образованием ионов, когда растворенное вещество диссоциирует или ионизируется с образованием раствора. Процесс растворения глюкозы (ЧО6126), (NHOh5) и (NaOH) в воду можно представить следующие уравнения: CHO()CHO()NHOH()NH()+OH()NaOH()Na()+OH()612661264+4–+–saqaqaqaqsaqaqHOHO22
Хотя глюкоза растворяется в воде, она не ионизируется с образованием ионов в решение. Поэтому мы можем отказаться от стакана A.
Гидроксид аммония (NHOh5) и натрия
гидроксид (NaOH) являются электролитами. Электролиты можно считать сильными или слабыми. Сильные электролиты полностью
диссоциируют при растворении, в то время как слабые электролиты лишь частично диссоциируют
при растворении. Различие между двумя типами электролитов может быть
видно в уравнениях реакции как стрелка равновесия
(⇌) будет использоваться, когда слабый
электролит растворяется, а стрелка вперед
(→)
используется при растворении сильного электролита.
Из уравнений реакции видно, что (NHOh5) является слабым электролитом, а (NaOH) является сильным электролитом. Раствором, содержащим сильный электролит, является химический стакан C.
Когда два или более веществ объединяются, образуя смесь, имеющую неоднородный По составу смесь можно отнести к гетерогенной. Приставка «гетеро-» означает «другой» и указывает на то, что состав и свойства смеси везде разные.
Определение: Гетерогенная смесь
Гетерогенная смесь – это смесь с неоднородным составом.
Сера, смешанная с железными опилками, является примером гетерогенной смеси. Серные и железные опилки остаются отдельными, и смесь не кажется одинаковой повсюду.
Нефть, смешанная с водой, является еще одним примером гетерогенной смеси.
Часто при гетерогенных смесях различные вещества в смеси
видно невооруженным глазом; однако это не относится ко всем разнородным
смеси. Коллоиды представляют собой гетерогенные смеси, состав которых кажется одинаковым. на всем протяжении при осмотре невооруженным глазом. В связи с этим они часто
принимают за однородные смеси. Однако при осмотре с увеличением
стекла или под микроскопом видно, что коллоиды не имеют однородной
состав. Примеры коллоидов включают туман, безе и молоко.
на всем протяжении при осмотре невооруженным глазом. В связи с этим они часто
принимают за однородные смеси. Однако при осмотре с увеличением
стекла или под микроскопом видно, что коллоиды не имеют однородной
состав. Примеры коллоидов включают туман, безе и молоко.
Определение: Коллоид
Коллоид представляет собой разновидность гетерогенной смеси, в которой диспергированы частицы по всей среде, в результате чего смесь выглядит однородной. состав при осмотре невооруженным глазом.
Суспензии представляют собой гетерогенную смесь, состоящую из очень больших взвешенные в среде частицы, которые со временем осядут на дно контейнер. Примеры суспензий включают муку, меловой порошок, и грязь смешалась с водой.
Определение: Суспензия
Суспензия – это тип гетерогенной смеси, в которой крупные частицы
подвешены в среде. Крупные частицы осядут на дно
контейнер со временем.
На приведенном ниже рисунке сравниваются растворы, коллоиды и суспензии.
Пример 5: Определение типа смеси, образующейся при добавлении сахара в воду
Что из следующего верно при добавлении сахара в воду?
- Они образуют гетерогенную смесь и называются коллоидами.
- Они образуют гомогенную смесь и называются коллоидами.
- Они образуют гетерогенную смесь и называются раствором.
- Образуют гетерогенную смесь и называются суспензией.
- Они образуют гомогенную смесь и называются раствором.
Ответ
Суспензия – гетерогенная смесь, состоящая из крупных частиц
подвешен в среде. Частицы не растворяются в среде и,
определенное время осядет на дно емкости. Коллоид представляет собой гетерогенную смесь, состоящую из мелких частиц, диспергированных
в среде. Частицы не растворяются в среде и не оседают
на дно контейнера. Суспензии и коллоиды выглядят мутными.
Раствор – это гомогенная смесь, состоящая из частиц, растворенных в Средняя. Частицы не оседают на дно контейнера и они не могут быть разделены фильтрацией. Растворы могут быть окрашены, но всегда ясны.
Основываясь на определениях суспензии, коллоида и раствора, мы можем исключить варианты ответов B и C. Когда сахар смешивается с водой, сахар растворяется в воде, образуя прозрачную смесь. Эта смесь решение. Правильный ответ – вариант ответа E.
На приведенной ниже диаграмме приведены термины, относящиеся к смесям.
Ключевые моменты
- Смесь состоит из двух или более веществ, которые физически смешаны.
- Смеси могут быть классифицированы как гомогенные или гетерогенные.
- Гомогенные смеси также называются растворами и состоят из растворенного вещества и растворитель.
- Количество растворенного вещества, присутствующего в растворе, может быть выражено терминами
ненасыщенные, насыщенные и перенасыщенные.

- Растворенные вещества, образующие ионы при растворении, называются электролитами.
- Коллоиды выглядят как растворы, но состоят из более крупных частиц, диспергированных в диспергирующая среда.
- Взвеси состоят из очень крупных частиц в среде, которые оседают на время.
NCERT Solutions for Class 9 Science Chapter 2
- Решения НЦЭРТ
- Класс 9
- Наука
- материя вокруг нас чиста
Наука NCERT 9 класс, глава 2, Чиста ли окружающая нас материя? начинается с краткого обсуждения чистых веществ. После этого делается акцент на концепции смеси, в которой обсуждаются три типа смесей:
После этого делается акцент на концепции смеси, в которой обсуждаются три типа смесей:
Раствор
Подвеска
Коллоидный раствор
При объяснении решений свойства решений подробно обсуждаются вместе с примерами некоторых распространенных решений. Дополнительная информация о сплавах также представлена в главе 9.0347 Чиста ли материя вокруг нас? . Концепция концентрации раствора вместе с его формулой и соответствующими экспериментами включена в главу Чиста ли материя вокруг нас? . Подобным образом суспензии и коллоидные растворы вместе с их свойствами и некоторыми общими примерами обсуждаются в последующих разделах главы. Следующие способы разделения компонентов смеси обсуждаются в главе 9.0347 Чиста ли материя вокруг нас?:
Каждый метод обсуждается с помеченной диаграммой вместе с его приложениями. Кроме того, в главе делается акцент на концепции физических и химических изменений с помощью примеров. Классификация чистых веществ на элементов и соединений вместе с их основными различиями включена в главу Чиста ли материя вокруг нас?
Кроме того, в главе делается акцент на концепции физических и химических изменений с помощью примеров. Классификация чистых веществ на элементов и соединений вместе с их основными различиями включена в главу Чиста ли материя вокруг нас?
Следующие темы рассматриваются в главе Чиста ли окружающая нас материя?
- Что такое смесь?
- Что такое решение?
- Разделение компонентов смеси
- Физические и химические изменения
- Какие существуют типы чистых веществ?
Страница № 15:
Вопрос 1:
Что подразумевается под чистым веществом?
Ответ:
Чистое вещество – это такое вещество, которое состоит из частиц одного типа, т. е. все частицы, входящие в состав вещества, имеют одинаковую химическую природу. Чистые вещества можно разделить на элементы или соединения.
Видео Решение для чистой материи вокруг нас (Страница: 15 , Q.
 No.: 1)
No.: 1)NCERT Решение для науки класса 9 — чистая ли материя вокруг нас 15 , Вопрос 1
Страница № 15:
Вопрос 2:
Перечислите точки различия между гомогенными и гетерогенными смесями.
Ответ:
Однородная смесь – это смесь, имеющая однородный состав по всей смеси. Например: соль в воде, сахар в воде, медный купорос в воде
Гетерогенная смесь представляет собой смесь, имеющую неоднородный состав по всей смеси. Например: хлористый натрий и железные пломбы, соль и сера, масло и вода
Видео Решение для чистой материи вокруг нас (Страница: 15 , Q.No.: 2)
NCERT Решение для науки класса 9 — это материя вокруг нас чистый 15 , Вопрос 2
Страница № 18:
Вопрос 1:
Различайте гомогенные и гетерогенные смеси с примерами.
Ответ:
Однородная смесь – это смесь, имеющая однородный состав по всей смеси. Например, смеси соли в воде, сахара в воде, сульфата меди в воде, йода в спирте, сплава и воздуха имеют одинаковый состав во всех смесях.
С другой стороны, гетерогенная смесь представляет собой смесь, имеющую неоднородный состав по всей смеси. Например, состав смесей хлористого натрия и железных наполнителей, соли и серы, масла и воды, мелового порошка в воде, пшеничной муки в воде, молока и воды неодинаков во всех смесях.
Видео Решение для чистой материи вокруг нас (Страница: 18 , Q.No.: 1)
NCERT Решение для науки класса 9 — чистая ли материя вокруг нас 18 , Вопрос 1
Страница № 18:
Вопрос 2:
Чем отличаются друг от друга золь, раствор и суспензия?
Ответ:
Sol представляет собой гетерогенную смесь. В этой смеси частицы растворенного вещества настолько малы, что их невозможно увидеть невооруженным глазом. Кроме того, они кажутся равномерно распределенными по всей смеси. В этой смеси наблюдается эффект Тиндаля. Например: магнезиальное молочко, грязь
Раствор представляет собой гомогенную смесь. В этой смеси частицы растворенного вещества растворяются и равномерно распределяются по всей смеси. Эффект Тиндаля в этой смеси не наблюдается. Например: соль в воде, сахар в воде, йод в спирте, сплав
Эффект Тиндаля в этой смеси не наблюдается. Например: соль в воде, сахар в воде, йод в спирте, сплав
Суспензии представляют собой гетерогенные смеси. В этой смеси частицы растворенного вещества видны невооруженным глазом и остаются взвешенными по всему объему среды. В этой смеси наблюдается эффект Тиндаля. Например: меловой порошок и вода, пшеничная мука и вода
Видео Решение для чистой материи вокруг нас (Страница: 18 , Q.No.: 2)
NCERT Решение для науки класса 9 — чистая ли материя вокруг нас 18 , Вопрос 2
Страница № 18:
Вопрос 3:
Для получения насыщенного раствора 36 г хлорида натрия растворяют в 100 г воды при температуре 293 К. Найдите его концентрацию при этой температуре.
Ответ:
Масса растворенного вещества (хлорида натрия) = 36 г (Дано)
Масса растворителя (воды) = 100 г (Дано)
Тогда масса раствора = масса растворенного вещества + масса растворителя
= (36 + 100) г
= 136 г
Следовательно, концентрация (масса в процентах) раствора
Видео Решение Чиста ли материя вокруг нас? следующие химические или физические изменения:
• Рубка деревьев
• Плавление масла в кастрюле
• Ржавление альмиры
• Кипячение воды с образованием пара
• Прохождение электрического тока через воду и разложение воды на водород и кислород
• Растворение поваренной соли в воде
• Приготовление фруктового салата из сырых фруктов
• Сжигание бумаги и дерева
Ответ:
• Рубка деревьев → Физическое изменение
• Растапливание масла на сковороде → Физическое изменение
• Ржавление альмиры → Химическое изменение
• Кипение воды с образованием пара → Физическое изменение
• Прохождение электрического тока через воду и разложение воды на газообразный водород и кислород → Химическое изменение
• Растворение поваренной соли в вода → Физическое изменение
• Приготовление фруктового салата из сырых фруктов → Физическое изменение
• Сжигание бумаги и дерева → Химическое изменение
Видео Решение чистоты окружающей нас материи (Страница: 24 , Q.
 No.: 1)
No.: 1)NCERT Решение для класса 9 науки — чистая ли материя вокруг нас 24 , Вопрос 1
Номер страницы 24:
Вопрос 2:
Попробуйте разделить окружающие вас вещи на чистые вещества или смеси.
Ответ:
Чистое вещество: Вода, соль, сахар
Смесь : Соленая вода, почва, дерево, воздух, прохладительные напитки, резина, губка, туман, молоко, масло, одежда, продукты питания
Видео решение ибо материя вокруг нас чиста (Страница: 24 , № Q: 2)
NCERT Решение для науки 9 класса — чистая ли материя вокруг нас 24 , Вопрос 2
Страница № 24:
Вопрос 3:
Какие типы смесей разделяют методом кристаллизации?
Ответ:
Методом кристаллизации чистые твердые вещества отделяются от примесей. Например, соль, полученную из моря, отделяют от примесей; кристаллы квасцов ( Phitkari ) отделяют от нечистых образцов.
Видео Решение для чистой материи вокруг нас (Страница: 24 , Q.
 No.: 3)
No.: 3)NCERT Решение для науки класса 9 — чистая ли материя вокруг нас 24 , Вопрос 3
Страница № 28:
Вопрос 1:
Какие методы разделения вы будете применять для разделения следующих веществ?
(а) Хлорид натрия из его раствора в воде.
(b) Хлорид аммония из смеси, содержащей хлорид натрия и хлорид аммония.
(c) Мелкие частицы металла в моторном масле автомобиля.
(d) Различные пигменты из экстракта цветочных лепестков.
e) Масло из творога.
f) Нефть из воды.
(г) Заварка из чая.
(ч) Штифты железные из песка.
(i) Зерна пшеницы из шелухи.
(j) Мелкие частицы грязи, взвешенные в воде.
Ответ:
(a) Хлорид натрия из его раствора в воде → Испарение
(b) Хлорид аммония из смеси, содержащей хлорид натрия и хлорид аммония → Возгонка
(c) Мелкие частицы металла в моторном масле автомобиль → Центрифугирование или фильтрация или декантация
(d) Различные пигменты из экстракта цветочных лепестков → Хроматография
(e) Масло из творога → Центрифугирование
(f) Масло из воды → Использование делительной воронки
(g) Чайные листья из чая → Фильтрация
(h) Железные штифты из песка → Магнитная сепарация
(i) Зерна пшеницы из шелухи → Веяние
(j) Мелкие частицы грязи, взвешенные в воде → Центрифугирование
Видео Решение чистоты окружающей нас материи (Страница: 28 , Q.
 №: 1)
№: 1)NCERT Решение для 9 класса науки — чистая ли материя вокруг нас 28 , Вопрос 1
Номер страницы 28:
Вопрос 2:
Напишите шаги, которые вы бы использовали для приготовления чая. Используйте слова: раствор, растворитель, растворенное вещество, растворить, растворить, нерастворить, фильтрат и остаток.
Ответ:
Сначала в качестве растворителя берется вода в блюдце. Этой воде (растворителю) дают закипеть. При нагревании к растворителю добавляют молоко и чайные листья в виде растворенных веществ . Они образуют раствор. Затем раствор сливают через ситечко. Нерастворимая часть раствора остается на сите в виде остатка . К фильтрату добавляют сахар, который растворяется в фильтрате. Полученный раствор и есть искомый чай.
Видео Решение для чистой материи вокруг нас (Страница: 28 , Q.No.: 2)
NCERT Решение для науки класса 9 — чистая ли материя вокруг нас 28 , Вопрос 2
Страница № 28:
Вопрос 3:
Pragya проверила растворимость трех различных веществ при разных температурах и собрала данные, как указано ниже (результаты приведены в следующей таблице, как граммы вещества, растворенные в 100 граммах воды с образованием насыщенного раствора) .
| Растворенное вещество | Температура в K | ||||
| 283 | 293 | 313 | 333 | 353 | |
| Нитрат калия | 21 | 32 | 62 | 106 | 167 |
| Хлорид натрия | 36 | 36 | 36 | 37 | 37 |
| Хлорид калия | 35 | 35 | 40 | 46 | 54 |
| Хлорид аммония | 24 | 37 | 41 | 55 | 66 |
а) Какая масса нитрата калия потребуется для получения насыщенного раствора нитрата калия в 50 граммах воды при температуре 313 К?
(b) Прагья готовит насыщенный раствор хлорида калия в воде при температуре 353 К и оставляет раствор охлаждаться при комнатной температуре. Что она увидит, когда раствор остынет? Объяснять.
Что она увидит, когда раствор остынет? Объяснять.
(c) Найдите растворимость каждой соли при 293 К. Какая соль имеет наибольшую растворимость при этой температуре?
(d) Как влияет изменение температуры на растворимость соли?
Ответ:
(а) При 313 К 62 грамма нитрата калия растворяются в 100 граммах воды. Таким образом, для получения насыщенного раствора нитрата калия в 50 граммах воды нам потребуется
62 x 50 = 31 грамм нитрата калия
100
(б) Некоторое количество растворимого хлорида калия выделится в виде кристаллов при комнатной температуре. температуре, потому что растворимость хлорида калия будет уменьшаться с понижением температуры.
(c)
(i) Растворимость нитрата калия при 293 K составляет 32 грамма.
(ii) Растворимость хлорида натрия при 293 K составляет 36 граммов.
(iii) Растворимость хлорида калия при 293 К составляет 35 граммов.
(iv) Растворимость хлорида аммония при 293 К составляет 37 граммов.
Растворимость хлорида аммония самая высокая при этой температуре.
(d) Растворимость соли увеличивается с повышением температуры.
Видео Решение для чистой материи вокруг нас (Страница: 28 , Q.No.: 3)
NCERT Решение для 9 класса науки — чистая ли материя вокруг нас 28 , Вопрос 3
Страница № 29:
Вопрос 4:
Объясните следующие примеры:
(a) Насыщенный раствор
(b) Чистый вещество
(c) Коллоид
(d) Суспензия
Ответ:
(a) Насыщенный раствор
Насыщенный раствор – это раствор, в котором растворено максимальное количество растворенного вещества при данной температуре. Раствор не может растворяться сверх этого количества растворенного вещества при этой температуре. Любое дополнительное добавленное растворенное вещество будет оседать на дне контейнера в виде осадка.
Предположим, что 500 г растворителя могут растворить максимум 150 г конкретного растворенного вещества при 40°C. Тогда раствор, полученный растворением 150 г этого растворенного вещества в 500 г этого растворителя при 300 К, называется насыщенным раствором при 300 К.
Тогда раствор, полученный растворением 150 г этого растворенного вещества в 500 г этого растворителя при 300 К, называется насыщенным раствором при 300 К.
(b) Чистое вещество
Чистое вещество – это вещество, частиц одного типа, т. е. все частицы, входящие в состав вещества, обладают одинаковыми химическими свойствами.
Например, соль, сахар, вода являются чистыми веществами.
(c) Коллоид
Коллоид представляет собой гетерогенную смесь. Размер растворенных веществ в этой смеси настолько мал, что их нельзя увидеть по отдельности невооруженным глазом, и кажется, что они равномерно распределены по всей смеси. Частицы растворенного вещества не оседают, если смесь не трогают. Это означает, что коллоиды достаточно стабильны. Коллоиды не могут быть разделены в процессе фильтрации. Их можно разделить центрифугированием. Коллоиды проявляют эффект Тиндаля. Например, молоко, масло, пена, туман, дым, облака.
(d) Суспензия
Суспензия представляет собой гетерогенную смесь. Растворенные частицы в этой смеси остаются взвешенными во всем объеме среды. Частицы можно увидеть невооруженным глазом. Подвеска демонстрирует эффект Тиндаля. Частицы растворенного вещества оседают, когда смесь остается нетронутой. Это означает, что подвески неустойчивы. Суспензии можно разделить методом фильтрации. Например, смеси из мелового порошка и воды, пшеничной муки и воды.
Растворенные частицы в этой смеси остаются взвешенными во всем объеме среды. Частицы можно увидеть невооруженным глазом. Подвеска демонстрирует эффект Тиндаля. Частицы растворенного вещества оседают, когда смесь остается нетронутой. Это означает, что подвески неустойчивы. Суспензии можно разделить методом фильтрации. Например, смеси из мелового порошка и воды, пшеничной муки и воды.
Видео Решение для чистой материи вокруг нас (Страница: 29 , Q.No.: 4)
NCERT Решение для науки класса 9 — чистая ли материя вокруг нас 29 , Вопрос 4
Страница № 29:
Вопрос 5:
Классифицируйте каждое из следующего как гомогенную или гетерогенную смесь.
Газированная вода, древесина, воздух, почва, уксус, фильтрованный чай
Ответ:
Гомогенные смеси : Газированная вода, воздух, уксус
Гетерогенные смеси : Древесина, почва, фильтрованный чай
Видео Решение чистоты материи вокруг нас (Страница: 29 , Q.
 No.: 5)
No.: 5)NCERT Решение для 9 класса науки — чистота материи вокруг нас 29 , вопрос 5
Страница № 29:
Вопрос 6:
Как бы вы подтвердили, что данная вам бесцветная жидкость является чистой водой?
Ответ:
Каждая жидкость имеет характерную температуру кипения. Чистая вода имеет температуру кипения 100°C (373 K) при 1 атмосферном давлении. Если данная бесцветная жидкость кипит даже немного выше или ниже 100°С, то данная жидкость не является чистой водой. Он должен кипеть при резких 100°C. Таким образом, наблюдая за температурой кипения, мы можем подтвердить, является ли данная бесцветная жидкость чистой водой или нет.
Видео Решение для чистой материи вокруг нас (Страница: 29 , Q.No.: 6)
NCERT Решение для науки класса 9 — чистая ли материя вокруг нас 29 , Вопрос 6
Страница № 29:
Вопрос 7:
Какие из следующих материалов относятся к категории «чистого вещества»?
(a) Лед
(b) Молоко
(c) Железо
(d) Соляная кислота
(e) Оксид кальция
(f) Ртуть
(g) Кирпич
0002 (h) Древесина(i) Воздух
Ответ:
К категории «чистого вещества» относятся следующие материалы:
(a) Лед
(c) Железо
(d) Соляная кислота
(e) Оксид кальция
(f) Ртуть
Видео Решение для чистой материи вокруг нас (Страница: 29 , Q.
 No.: 7)
No.: 7)NCERT Решение для науки класса 9 — чистая ли материя вокруг нас 29 , Вопрос 7
Страница № 29:
Вопрос 8:
Определите растворы среди следующих смесей:
(a) Почва
(b) Морская вода
(c) Воздух
(d) Уголь
(e) Газированная вода
Ответ:
Следующие смеси растворы:
(b) Морская вода
(c) Воздух
(e) Газированная вода
Видео Решение для чистоты окружающей нас материи (Страница: 29, Q.No.: 8)
NCERT Solution для 9 класса наука — чистая ли материя вокруг нас 29 , вопрос 8
Страница № 29:
Вопрос 9:
Что из следующего покажет «эффект Тиндаля»?
(a) Раствор соли
(b) Молоко
(c) Раствор медного купороса
(d) Раствор крахмала
Ответ:
Раствор молока и крахмала покажет «эффект Тиндаля».
Видео Решение для чистой материи вокруг нас (Страница: 29 , Q.No.: 9)
NCERT Решение для науки класса 9 — чистая ли материя вокруг нас 29 , Вопрос 9
Страница № 29:
Вопрос 10:
Распределите по элементам, соединениям и смесям:
(a) Натрий
(b) Почва
(c) Раствор сахара
3
2 (0) Серебро (e) Карбонат кальция(f) Олово
(g) Кремний
(h) Уголь
(i) Воздух
(j) Мыло
(k) Метан
9002 Двуокись углерода (m) Кровь
Ответ:
Элементы
(а) Натрий |
(г) Серебро |
(ж) Олово |
(г) Кремний |
Соединения
(e) Карбонат кальция |
(л) Метан |
(л) Углекислый газ |
Смеси
(б) Почва |
(c) Сахарный раствор |
(з) Уголь |
(и) Воздух |
(к) Мыло |
(м) Кровь |
Видео Решение для чистой материи вокруг нас (Страница: 29, Q.


 Ag()/Hg()sl
Ag()/Hg()sl