Содержание
Эволюция акушерства: от древних практик к инновационным технологиям
Акушерство — это область медицины, которая прошла долгий путь от примитивных практик до высокотехнологичной науки. Как же оно развивалось и что представляет собой сегодня? Давайте окунемся в увлекательный мир современного акушерства и узнаем, какие секреты безопасных родов оно хранит.
Помните ли вы, как наши прабабушки рожали? Часто это происходило дома, с помощью повитухи, без какой-либо медицинской помощи. А теперь? Теперь роды — это целая операция, где каждый шаг продуман и обеспечен современными технологиями. Но как мы пришли к этому?
От интуиции к науке: путь акушерства
Акушерство прошло путь от интуитивных практик к строгой науке. В древности роды считались естественным процессом, который не требует вмешательства. Но с развитием медицины стало ясно, что правильная помощь может спасти жизни матери и ребенка. Сегодня акушерство — это сложная система знаний и технологий, направленная на обеспечение безопасности родов.
Какие же методы используются в акушерстве в настоящее время? Их множество, и они постоянно совершенствуются. Начнем с предродовой диагностики. Современные УЗИ-аппараты позволяют увидеть малыша еще до его рождения, оценить его развитие и выявить возможные проблемы. А генетические тесты помогают предсказать риск наследственных заболеваний.
Во время родов применяются различные методы обезболивания, от эпидуральной анестезии до ингаляционной аналгезии. Эти методы позволяют снизить стресс для матери и ребенка, сделать процесс родов более комфортным. Но не думайте, что все сводится только к обезболиванию! Современное акушерство — это целый комплекс мер, направленных на обеспечение безопасности.
Технологии на страже жизни
Вы когда-нибудь задумывались, как врачи следят за состоянием плода во время родов? Раньше это было сложно, но сегодня на помощь приходят современные технологии. Кардиотокография (КТГ) позволяет непрерывно мониторить сердцебиение плода и сокращения матки. Это помогает вовремя заметить признаки дистресса плода и принять необходимые меры.
А что если возникают осложнения? И здесь современное акушерство во всеоружии. Кесарево сечение, которое раньше было рискованной операцией, сегодня стало рутинной процедурой благодаря развитию хирургических техник и анестезиологии. Вакуум-экстракция и акушерские щипцы помогают в случаях, когда нужно ускорить второй этап родов.
Но технологии — это не все. Важную роль играет и подход к ведению родов. Современное акушерство стремится к индивидуальному подходу, учитывающему особенности каждой женщины. Партнерские роды, свободное положение во время родов, ранний контакт матери и ребенка — все это стало возможным благодаря пониманию психологических аспектов родов.
Инновации на страже материнства
А знаете ли вы, что современное акушерство не останавливается на достигнутом? Постоянно появляются новые методики и технологии. Например, фетальная хирургия позволяет проводить операции на плоде еще до его рождения. Звучит как научная фантастика, не правда ли? Но это уже реальность.
Искусственная матка — еще одна инновация, которая может изменить будущее акушерства. Пока это экспериментальная технология, но она уже показала обнадеживающие результаты в выхаживании глубоко недоношенных детей. Представьте себе мир, где каждый ребенок, независимо от срока гестации, имеет шанс на жизнь!
Генная терапия открывает новые горизонты в лечении наследственных заболеваний. Уже сейчас возможно выявить многие генетические аномалии до рождения ребенка. А в будущем, возможно, мы сможем корректировать эти аномалии еще на стадии эмбриона.
Вызовы современного акушерства
Однако не все так гладко в мире современного акушерства. Оно сталкивается с рядом вызовов. Один из них — растущее число кесаревых сечений. С одной стороны, эта операция спасает жизни. С другой — ее чрезмерное использование может приводить к осложнениям. Как найти баланс? Это вопрос, над которым бьются современные акушеры.
Другой вызов — это вопрос доступности качественной акушерской помощи. В развитых странах женщины имеют доступ к самым современным технологиям. Но как быть с развивающимися странами, где материнская смертность все еще остается высокой? Это глобальная проблема, требующая решения.

И наконец, этические вопросы. Пренатальная диагностика позволяет выявить многие заболевания плода. Но как быть с правом на жизнь? Где грань между медицинской необходимостью и евгеникой? Эти вопросы требуют не только медицинского, но и философского осмысления.
Будущее акушерства: что нас ждет?
Каким будет акушерство будущего? Можно предположить, что оно станет еще более персонализированным. Уже сейчас развивается направление «акушерства, основанного на доказательствах». Оно предполагает индивидуальный подход к каждой беременности, основанный на научных данных и личных особенностях женщины.
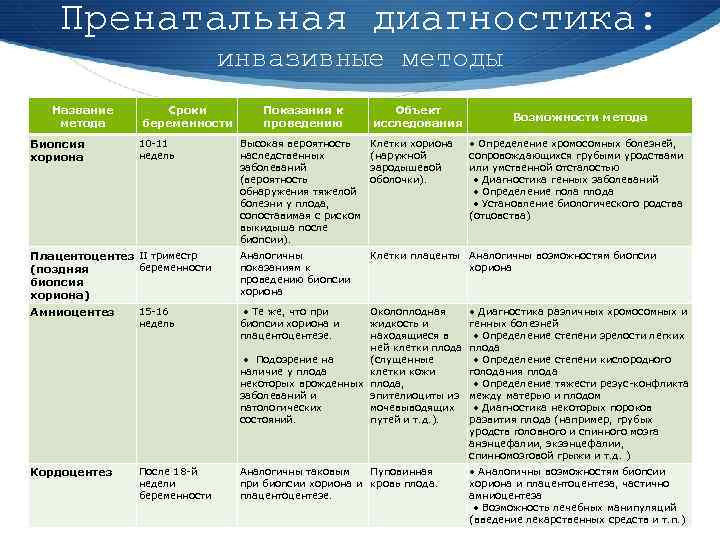
Вероятно, мы увидим еще большее развитие неинвазивных методов диагностики. Уже сейчас неинвазивное пренатальное тестирование позволяет выявить многие генетические аномалии по крови матери. В будущем эти методы станут еще более точными и информативными.
Искусственный интеллект тоже может сыграть свою роль в будущем акушерства. Уже сейчас разрабатываются алгоритмы, способные прогнозировать осложнения беременности на основе больших данных. В будущем эти технологии могут стать неотъемлемой частью акушерской практики.
Таким образом, современное акушерство — это сложная, многогранная область медицины, которая постоянно развивается. От древних практик до инновационных технологий — путь был долгим, но результат впечатляет. Сегодня рождение ребенка стало намного безопаснее, чем когда-либо в истории человечества. И кто знает, какие еще чудеса принесет нам будущее в этой области?
Ультразвуковая диагностика: ключ к пренатальному здоровью плода
Представьте себе, что вы можете заглянуть в будущее и увидеть своего ребенка еще до его рождения. Звучит как научная фантастика? А вот и нет! Это реальность, которую нам подарила ультразвуковая диагностика. Эта технология стала настоящей революцией в акушерстве, позволив врачам и будущим родителям буквально заглянуть в утробу матери.
Но как это работает? Ультразвуковое исследование (УЗИ) использует высокочастотные звуковые волны для создания изображений внутренних органов. В случае беременности, эти волны проникают через живот матери и отражаются от тканей плода, создавая детальную картину его развития. Это как подводная съемка, только вместо воды — околоплодные воды, а вместо рыбки — ваш будущий малыш.

От пиксельных картинок к 4D-реальности
Помните первые УЗИ-снимки? Черно-белые, нечеткие, больше похожие на абстрактную живопись, чем на изображение ребенка. Сейчас же технологии шагнули далеко вперед. Современные аппараты УЗИ способны создавать четкие трехмерные изображения, а то и вовсе показывать плод в режиме реального времени в формате 4D. Вы можете увидеть, как ваш малыш улыбается, зевает или даже сосет большой палец!
Но УЗИ — это не просто возможность полюбоваться на своего будущего ребенка. Это мощный диагностический инструмент, который играет ключевую роль в современном акушерстве. Какие методы используются в акушерстве в настоящее время? УЗИ — один из самых важных.
УЗИ как детектив: что можно узнать?
УЗИ позволяет врачам собрать массу важной информации о развитии плода. Вот лишь некоторые вещи, которые можно узнать с помощью этого исследования:
- Срок беременности и предполагаемая дата родов
- Пол ребенка (хотя не всегда со 100% точностью)
- Количество плодов (привет, близнецы!)
- Расположение плаценты
- Количество околоплодных вод
- Развитие органов плода
- Наличие возможных аномалий развития
Это как если бы у вас был рентгеновский взгляд, который позволяет видеть сквозь стены утробы. Только вместо супергеройских способностей — высокотехнологичное оборудование и опытный врач-диагност.
УЗИ в разные триместры: что и когда смотрят?
УЗИ проводится на разных сроках беременности, и каждое исследование имеет свои цели. Давайте разберемся, что и когда смотрят:
- Первый триместр (до 13 недель):
- Подтверждение беременности
- Определение срока беременности
- Проверка сердцебиения плода
- Скрининг на хромосомные аномалии
- Второй триместр (13-28 недель):
- Оценка анатомии плода
- Определение пола (если родители хотят знать)
- Измерение роста плода
- Оценка расположения плаценты
- Третий триместр (после 28 недель):
- Оценка количества околоплодных вод
- Проверка положения плода перед родами
Это как серия снимков в фотоальбоме развития вашего малыша, только каждый «снимок» несет в себе важную медицинскую информацию.

Допплерография: слушаем пульс жизни
Отдельно стоит упомянуть допплерографию — особый вид УЗИ, который позволяет оценить кровоток в сосудах плода и плаценты. Это как если бы вы могли услышать, как бьется сердце вашего малыша, и увидеть, как кровь течет по его tiny венам и артериям.
Допплерография особенно важна при осложненной беременности. Она помогает выявить проблемы с плацентарным кровотоком, которые могут привести к задержке роста плода или другим осложнениям. Это как система раннего предупреждения, которая позволяет врачам вовремя принять необходимые меры.
Безопасность УЗИ: мифы и реальность
Несмотря на широкое использование УЗИ, некоторые будущие мамы все еще беспокоятся о его безопасности. Давайте разберемся, насколько обоснованы эти страхи.
УЗИ использует звуковые волны, а не ионизирующее излучение, как рентген. Это означает, что оно не вызывает повреждения клеток и ДНК. Многочисленные исследования не выявили никаких негативных последствий УЗИ для плода или матери.
Однако, как и с любой медицинской процедурой, УЗИ следует проводить только по показаниям. Частые «развлекательные» УЗИ не рекомендуются, так как любое воздействие на плод должно быть обоснованным.
Будущее УЗИ: что нас ждет?
Технологии УЗИ продолжают развиваться. Что нас ждет в будущем? Вот несколько exciting направлений:
- Искусственный интеллект в интерпретации УЗИ-изображений
- Еще более детальные 3D и 4D изображения
- Портативные УЗИ-сканеры, которые можно подключить к смартфону
- Комбинация УЗИ с другими методами визуализации для еще более точной диагностики
Представьте себе будущее, где УЗИ станет таким же обычным делом, как измерение температуры. Где каждая беременная женщина сможет «увидеть» своего малыша в любой момент, просто приложив небольшой датчик к животу.
УЗИ как часть комплексного подхода
Важно помнить, что УЗИ — это лишь один из инструментов в арсенале современного акушерства. Оно используется в комплексе с другими методами диагностики и наблюдения за беременностью.

Какие еще методы используются в акушерстве в настоящее время? Это и неинвазивное пренатальное тестирование (НИПТ), позволяющее выявить генетические аномалии по крови матери, и кардиотокография (КТГ) для мониторинга сердцебиения плода во время беременности и родов, и множество других методов.
УЗИ — это как фонарик, освещающий путь в темноте. Оно помогает врачам и будущим родителям ориентироваться в сложном процессе беременности, выявлять потенциальные проблемы и принимать информированные решения.
В заключение хочется сказать, что ультразвуковая диагностика стала настоящим прорывом в акушерстве. Она позволила нам заглянуть в таинственный мир внутриутробного развития, сделала беременность более безопасной и контролируемой. Но при этом она не лишила этот процесс волшебства и чуда. Ведь что может быть более волшебным, чем увидеть своего будущего ребенка еще до его рождения?
Естественные роды vs. кесарево сечение: критерии выбора метода родоразрешения
Роды — это кульминация девятимесячного путешествия, финишная прямая марафона беременности. Но вот вопрос: каким способом пересечь эту финишную черту? Естественным путем или с помощью кесарева сечения? Этот выбор — один из самых важных в современном акушерстве, и он зависит от множества факторов.
Представьте себе, что беременность — это как полет на самолете. Естественные роды — это как обычная посадка: все идет по плану, самолет плавно приземляется на взлетно-посадочную полосу. А кесарево сечение? Это как экстренная посадка на воду: иногда необходимая мера, которая может спасти жизни, но требует особой подготовки и навыков от экипажа (в нашем случае — медицинского персонала).
Естественные роды: путь, проложенный природой
Естественные роды — это то, что задумала природа. Это процесс, отточенный миллионами лет эволюции. Но что делает их такими особенными? Давайте разберемся.
Во-первых, естественные роды запускают каскад гормональных изменений, которые подготавливают организм матери и ребенка к новой жизни. Окситоцин, эндорфины, адреналин — это как химический коктейль, который помогает справиться с родовыми болями и установить связь между матерью и ребенком.

Во-вторых, проходя через родовые пути, ребенок получает «прививку» материнской микрофлорой, что важно для формирования его иммунной системы. Это как первый урок выживания для малыша.
В-третьих, сам процесс родов стимулирует дыхательную систему новорожденного. Сжатие грудной клетки во время прохождения по родовым путям помогает вытеснить жидкость из легких ребенка, подготавливая их к первому вдоху.
Кесарево сечение: когда природе нужна помощь
Кесарево сечение — это хирургическая операция, которая может быть необходима по ряду причин. Но какие методы используются в акушерстве в настоящее время для проведения кесарева сечения?
- Классическое кесарево сечение с вертикальным разрезом
- Кесарево сечение по Дерфлеру с горизонтальным разрезом
- Экстраперитонеальное кесарево сечение (без вскрытия брюшной полости)
Каждый метод имеет свои показания и особенности. Выбор зависит от конкретной ситуации и опыта хирурга.
Кесарево сечение может быть плановым или экстренным. Плановое — это как заранее забронированный билет на самолет. Вы знаете дату и время вылета (в нашем случае — родов). Экстренное — это как вынужденная посадка: решение принимается быстро, когда возникает угроза для матери или ребенка.
Критерии выбора: когда что предпочтительнее?
Так как же выбрать между естественными родами и кесаревым сечением? Вот несколько ключевых факторов:
- Положение плода:
Если ребенок находится в ягодичном предлежании или поперечном положении, естественные роды могут быть рискованными. В таких случаях часто рекомендуют кесарево сечение.
- Размер плода:
Крупный плод (макросомия) может быть показанием к кесареву сечению, особенно если есть несоответствие размеров плода и таза матери.
- Многоплодная беременность:
Близнецы или тройня? Это не обязательно означает кесарево, но повышает его вероятность.
- Предыдущие кесаревы сечения:
Хотя возможны и естественные роды после кесарева (VBAC), многие врачи предпочитают повторное кесарево для минимизации рисков.
- Состояние здоровья матери:
Некоторые заболевания (например, тяжелая форма преэклампсии) могут быть показанием к кесареву сечению.
- Состояние плода:
Признаки дистресса плода во время беременности или родов могут потребовать экстренного кесарева сечения.
Выбор метода родоразрешения — это как шахматная партия, где нужно учесть множество факторов и просчитать возможные ходы на несколько шагов вперед.
Риски и преимущества: две стороны медали
Как и любое медицинское вмешательство, и естественные роды, и кесарево сечение имеют свои риски и преимущества. Давайте рассмотрим их подробнее.
Естественные роды:
- Преимущества:
- Более быстрое восстановление после родов
- Меньший риск респираторных проблем у новорожденного
- Стимуляция выработки грудного молока
- Риски:
- Возможность разрывов промежности
- Риск гипоксии плода при затяжных родах
- Вероятность экстренного кесарева сечения
Кесарево сечение:
- Преимущества:
- Возможность планирования даты родов
- Меньший риск травматизма для плода при определенных состояниях
- Сохранение целостности тазового дна
- Риски:
- Более длительный период восстановления
- Риск инфекционных осложнений
- Возможные проблемы с будущими беременностями
Выбор между естественными родами и кесаревым сечением — это как выбор между двумя дорогами. Обе могут привести к цели, но путешествие будет разным.
Современные тенденции: куда движется акушерство?
В последние годы наблюдается интересная тенденция: с одной стороны, растет количество кесаревых сечений (в некоторых странах их доля достигает 50% и более), с другой — усиливается движение за естественные роды.
Какие методы используются в акушерстве в настоящее время для поддержки естественных родов? Вот некоторые из них:
- Вертикальные роды и свободное положение роженицы
- Гидротерапия (роды в воде)
- Немедикаментозные методы обезболивания (дыхательные техники, массаж)
- Партнерские роды
В то же время, технологии кесарева сечения тоже не стоят на месте. Развиваются методики «мягкого» кесарева сечения, направленные на максимальное приближение опыта к естественным родам. Это включает раннее прикладывание к груди, контакт «кожа к коже» сразу после рождения.

Индивидуальный подход: ключ к успешным родам
Современное акушерство стремится к индивидуализации подхода. Каждая беременность уникальна, и то, что подходит одной женщине, может не подойти другой.
Важную роль играет информированное согласие. Будущая мама должна понимать все за и против каждого метода родоразрешения. Это как если бы вы выбирали маршрут путешествия: вы должны знать все особенности дороги, прежде чем отправиться в путь.
Некоторые клиники практикуют составление «плана родов» — документа, в котором женщина может выразить свои пожелания относительно процесса родов. Это может включать предпочтения по обезболиванию, присутствию партнера, использованию определенных процедур.
Будущее родовспоможения: что нас ждет?
Акушерство продолжает развиваться, и мы можем ожидать новых интересных тенденций. Вот некоторые направления, которые могут определять будущее родовспоможения:
- Персонализированная медицина: использование генетического профиля для прогнозирования рисков и выбора оптимальной тактики ведения беременности и родов.
- Роботизированная хирургия: возможно, в будущем кесарево сечение будет выполняться роботами-хирургами под контролем человека.
- Виртуальная реальность для обезболивания: использование VR-технологий для отвлечения от боли во время родов.
- Искусственная матка: технология, которая может изменить наше понимание о преждевременных родах.
Выбор между естественными родами и кесаревым сечением — это не просто медицинское решение. Это выбор пути, которым новая жизнь придет в этот мир. И хотя наука и технологии предоставляют нам все больше возможностей, ключевым остается индивидуальный подход, учитывающий уникальность каждой женщины и каждой беременности.
Анестезия в родах: современные подходы к обезболиванию
Роды — это как марафон, только вместо 42 километров у вас несколько часов интенсивной работы. И как любой марафонец нуждается в поддержке на дистанции, так и роженица нуждается в обезболивании. Но какие методы используются в акушерстве в настоящее время для облегчения этого непростого пути?

Современное акушерство предлагает целый арсенал средств для борьбы с болью во время родов. От древних практик дыхания до высокотехнологичных медицинских процедур — выбор настолько широк, что порой голова идет кругом. Давайте разберемся, что к чему в этом многообразии методов обезболивания.
Немедикаментозные методы: природа знает лучше?
Начнем с того, что ближе к природе. Немедикаментозные методы обезболивания — это как натуральная косметика в мире красоты. Они обещают эффект без побочных действий. Но насколько они эффективны?
- Дыхательные техники: Это как йога для рожениц. Правильное дыхание помогает расслабиться и отвлечься от боли. Метод Ламаза, например, учит особым паттернам дыхания для каждой стадии родов.
- Массаж: Нежные прикосновения партнера или доулы могут творить чудеса. Это как волшебная палочка, которая превращает боль в приятные ощущения.
- Водные процедуры: Теплый душ или ванна — это как SPA-процедура во время родов. Вода расслабляет мышцы и снимает напряжение.
- Акупунктура и акупрессура: Эти древние китайские практики — как карта сокровищ на теле человека. Воздействуя на определенные точки, можно уменьшить болевые ощущения.
Эти методы хороши тем, что их можно комбинировать и использовать на любом этапе родов. Они не имеют противопоказаний и побочных эффектов. Но, как и натуральная косметика, они могут быть недостаточно эффективны при сильной боли.
Фармакологические методы: наука приходит на помощь
Когда природных методов недостаточно, на помощь приходит современная фармакология. Это как перейти от велосипеда к автомобилю — эффективно, но требует более внимательного подхода.
Какие методы используются в акушерстве в настоящее время для медикаментозного обезболивания? Вот основные игроки на этом поле:
- Закись азота (веселящий газ):
Это как легкий коктейль на вечеринке — снимает напряжение, но оставляет в сознании. Смесь закиси азота с кислородом вдыхают через маску во время схваток. Эффект быстрый, но кратковременный.
- Опиоидные анальгетики:
Это уже серьезная артиллерия. Препараты вроде морфина или фентанила вводят внутримышечно или внутривенно. Они эффективны, но могут вызывать сонливость и тошноту у матери, а также влиять на дыхание новорожденного.

- Эпидуральная анестезия:
Вот она, королева обезболивания в родах! Анестетик вводится в эпидуральное пространство позвоночника, блокируя болевые сигналы. Это как выключить звук у телевизора — картинка есть, а звука (в нашем случае — боли) нет.
Каждый из этих методов имеет свои плюсы и минусы. Выбор зависит от индивидуальной ситуации, предпочтений женщины и рекомендаций врача.
Эпидуральная анестезия: панацея или палка о двух концах?
Эпидуральная анестезия заслуживает отдельного разговора. Это как суперсовременный смартфон в мире телефонов — многофункциональный и эффективный, но требующий умелого обращения.
Преимущества эпидуральной анестезии очевидны: она обеспечивает отличное обезболивание, позволяет женщине оставаться в сознании и участвовать в процессе родов. Но есть и обратная сторона медали:
- Может замедлить процесс родов
- Увеличивает вероятность использования инструментальных методов родовспоможения (щипцы, вакуум-экстрактор)
- Может вызвать падение артериального давления у матери
- В редких случаях приводит к головной боли после родов
Современные методики, такие как walking epidural (ходячая эпидуралка), позволяют снизить некоторые из этих рисков. Эта техника позволяет женщине двигаться во время родов, что способствует их прогрессу.
Комбинированные подходы: лучшее из двух миров
Современное акушерство все чаще обращается к комбинированным подходам в обезболивании родов. Это как фьюжн-кухня в кулинарии — берем лучшее из разных традиций и создаем что-то новое и эффективное.
Например, сочетание дыхательных техник и эпидуральной анестезии может дать отличные результаты. Женщина использует дыхательные упражнения на ранних стадиях родов, а когда боль становится слишком интенсивной, переходит к эпидуральной анестезии.
Другой пример — комбинация гидротерапии и фармакологических методов. Теплая вода помогает расслабиться и снять напряжение, а при необходимости можно использовать закись азота или опиоидные анальгетики.
Индивидуальный подход: ключ к успеху
В современном акушерстве нет универсального решения для всех. Каждая женщина уникальна, и ее опыт родов тоже будет уникальным. Поэтому индивидуальный подход — это как custom-made костюм в мире обезболивания родов.

Важную роль играет предродовая подготовка. Это как тренировки перед марафоном. Женщина должна знать о доступных методах обезболивания, их преимуществах и рисках. Это позволяет ей сделать информированный выбор и быть готовой к различным сценариям.
Некоторые клиники практикуют составление «плана обезболивания» — документа, в котором женщина может выразить свои предпочтения по методам обезболивания. Это как написать сценарий для своих родов, хотя, конечно, жизнь может внести свои коррективы.
Новые горизонты: что нас ждет в будущем?
Наука не стоит на месте, и в области обезболивания родов тоже появляются новые интересные разработки. Вот некоторые направления, за которыми стоит следить:
- Ремифентанил PCA (patient-controlled analgesia): Это как персональный диджей боли. Женщина сама контролирует введение препарата с помощью специального устройства.
- Нитевидная эпидуральная анестезия: Эта техника позволяет вводить анестетик через очень тонкий катетер, что снижает риск осложнений.
- Виртуальная реальность: Представьте, что во время схваток вы гуляете по тропическому пляжу или любуетесь северным сиянием. VR-технологии могут стать мощным инструментом отвлечения от боли.
- Транскраниальная магнитная стимуляция: Это как массаж для мозга. Метод использует магнитные поля для стимуляции определенных участков мозга, что может помочь в управлении болью.
Эти инновационные подходы пока находятся на стадии исследований и экспериментов, но они открывают захватывающие перспективы для будущего акушерства.
Этические аспекты: право на выбор
Вопрос обезболивания в родах имеет не только медицинский, но и этический аспект. Это как дебаты о свободе воли в философии. С одной стороны, каждая женщина имеет право на облегчение боли. С другой — есть мнение, что боль в родах естественна и даже необходима для формирования связи между матерью и ребенком.
Современное акушерство стремится найти баланс между этими позициями. Ключевой принцип — информированное согласие. Женщина должна иметь доступ к полной информации о методах обезболивания и право выбора.

При этом важно помнить, что планы могут меняться. Женщина, планировавшая естественные роды без обезболивания, может в процессе родов попросить эпидуральную анестезию. И это нормально. Гибкость и отсутствие осуждения — важные принципы современного подхода к обезболиванию в родах.
В заключение хочется сказать, что современное акушерство предлагает широкий спектр методов обезболивания родов — от древних практик до высокотехнологичных медицинских процедур. Выбор метода — это как выбор пути в лабиринте. Нет единственно правильного решения, есть то, что подходит именно вам в данный момент. Главное — быть информированной, гибкой и доверять себе и своему телу.
Партнерские роды: роль поддержки близких в процессе деторождения
Ух ты, как быстро летит время! Кажется, совсем недавно акушерство было совсем другим, а сегодня оно преображается на глазах. Что же изменилось? Какие методы используются в акушерстве в настоящее время? Давайте окунемся в этот захватывающий мир современного родовспоможения и узнаем, как оно развивается, чтобы сделать появление новой жизни максимально безопасным и комфортным.
Современное акушерство — это настоящий симбиоз науки и искусства. Оно вобрало в себя вековые традиции и новейшие технологии, чтобы создать идеальные условия для рождения малыша. Но знаете, что самое интересное? Несмотря на все достижения, главным действующим лицом по-прежнему остается сама природа. Акушеры лишь помогают ей, создавая оптимальные условия для естественного процесса.
Технологический прорыв в родильных залах
Представьте себе родильный зал будущего. Нет, это не фантастический фильм — это реальность современного акушерства! Высокотехнологичное оборудование здесь соседствует с уютной, почти домашней обстановкой. Кардиотокографы непрерывно следят за состоянием малыша, а специальные датчики контролируют самочувствие мамы. Но это лишь верхушка айсберга.
Одним из революционных методов стало применение 3D и 4D УЗИ. Эти технологии позволяют увидеть малыша еще до его рождения с невероятной четкостью. Врачи могут оценить развитие плода, выявить возможные аномалии и вовремя принять необходимые меры. А будущие родители? Они получают уникальную возможность «познакомиться» со своим крохой задолго до первой встречи. Разве это не чудо?

Естественные роды: возвращение к истокам
Парадоксально, но факт: чем дальше развивается медицина, тем больше внимания уделяется естественному течению родов. Современное акушерство стремится минимизировать вмешательство в природный процесс. Вертикальные роды, роды в воде, домашние роды под наблюдением специалистов — все эти методы набирают популярность. И знаете что? Исследования показывают, что такой подход снижает риск осложнений и ускоряет восстановление после родов.
Но как же быть с болью? Неужели придется терпеть? Ни в коем случае! Современное акушерство предлагает целый арсенал методов обезболивания. От классической эпидуральной анестезии до инновационных техник, таких как гипноз или акупунктура. Каждая женщина может выбрать то, что подходит именно ей. Главное — комфорт и безопасность.
Индивидуальный подход: ключ к успешным родам
Знаете, в чем секрет современного акушерства? В понимании того, что каждые роды уникальны. Нет универсальных решений, подходящих всем. Поэтому сегодня так важен индивидуальный подход. Врачи тщательно изучают историю каждой пациентки, учитывают ее пожелания и особенности. Это позволяет составить оптимальный план ведения беременности и родов.
А как насчет партнерских родов? Это уже не просто модный тренд, а научно обоснованная практика. Исследования показывают, что присутствие близкого человека снижает уровень стресса у роженицы, уменьшает потребность в обезболивании и даже сокращает продолжительность родов. Удивительно, правда?
Психологическая подготовка: недооцененный аспект
Знаете, что часто упускают из виду, говоря о современном акушерстве? Психологическую подготовку! А ведь это не менее важно, чем физическая готовность. Сегодня будущим мамам предлагают целый комплекс услуг: от индивидуальных консультаций до групповых занятий по подготовке к родам. Цель? Снять страх, научить правильно дышать и расслабляться, подготовить к встрече с малышом.
И это работает! Женщины, прошедшие такую подготовку, чувствуют себя увереннее, легче переносят роды и быстрее восстанавливаются после них. А что может быть важнее для начала новой жизни?
Технологии на службе безопасности
Безопасность — вот что стоит во главе угла современного акушерства. И здесь на помощь приходят высокие технологии. Компьютерные системы мониторинга позволяют отслеживать состояние мамы и малыша в режиме реального времени. Малейшее отклонение от нормы — и система подает сигнал. Врачи могут мгновенно отреагировать на изменения, предотвращая возможные осложнения.
А как вам идея «умных» родильных залов? Это не фантастика, а реальность некоторых современных клиник. Автоматизированные системы контролируют температуру, влажность, освещение — все, чтобы создать идеальные условия для рождения малыша. Представляете, какой уровень комфорта и безопасности это обеспечивает?
Послеродовое восстановление: новый взгляд
Современное акушерство не заканчивается с рождением малыша. Огромное внимание уделяется послеродовому периоду. Раннее прикладывание к груди, совместное пребывание мамы и малыша, поддержка грудного вскармливания — все это стало нормой в современных роддомах. А знаете почему? Исследования показывают, что такой подход способствует более быстрому восстановлению мамы и лучшей адаптации новорожденного.
Но и это еще не все! Современное акушерство предлагает целый комплекс реабилитационных мероприятий после родов. От специальной гимнастики до физиотерапевтических процедур. Цель? Помочь женщине как можно быстрее вернуться к привычной жизни и наслаждаться материнством в полной мере.
Подводя итоги, можно сказать, что современное акушерство — это удивительный мир, где высокие технологии сочетаются с индивидуальным подходом, а научные достижения — с уважением к природе. Оно стремится сделать роды максимально безопасными и комфортными, не забывая при этом об уникальности каждой женщины и каждого малыша. И знаете что? Похоже, у него это отлично получается!
Послеродовое наблюдение: важность раннего выявления осложнений
Когда речь заходит о современном акушерстве, многие сразу представляют себе высокотехнологичные родильные залы и сложные медицинские процедуры. Но знаете что? Настоящая магия начинается после того, как малыш появился на свет. Послеродовое наблюдение — это тот самый ключ, который открывает дверь к полноценному восстановлению мамы и здоровому развитию новорожденного. Так почему же оно так важно? И какие методы используются в акушерстве в настоящее время для обеспечения безопасности в этот период?
Представьте себе, что роды — это марафон. Вы пробежали дистанцию, пересекли финишную черту, но гонка еще не окончена. Послеродовой период — это время восстановления, адаптации и новых вызовов. И именно здесь современное акушерство проявляет всю свою мощь и заботу.
Ранняя диагностика — залог спокойствия
Первые дни после родов — это настоящий калейдоскоп эмоций и физических изменений. Но как отличить нормальное течение послеродового периода от тревожных симптомов? Вот где на сцену выходит современная диагностика. Сегодня акушеры вооружены целым арсеналом методов, позволяющих выявить малейшие отклонения на ранних стадиях.
Возьмем, к примеру, ультразвуковое исследование. Раньше его проводили только при подозрении на осложнения. А теперь? Это рутинная процедура, которая помогает оценить состояние матки, исключить задержку частей плаценты и выявить другие потенциальные проблемы. И знаете что? Это лишь верхушка айсберга!
Лабораторные исследования: невидимые стражи здоровья
А как насчет того, что невозможно увидеть невооруженным глазом? Здесь на помощь приходят современные лабораторные методы. Анализ крови, например, может рассказать целую историю о состоянии организма молодой мамы. Уровень гемоглобина, лейкоцитов, С-реактивного белка — все эти показатели словно кусочки пазла складываются в общую картину здоровья.
Но не будем забывать и о гормональном фоне. Послеродовой период — это настоящие американские горки для эндокринной системы. Современные методы позволяют отслеживать уровень гормонов и вовремя корректировать возможные нарушения. Это особенно важно для профилактики послеродовой депрессии — настоящего бича современного общества.
Физическое обследование: искусство прикосновения
Несмотря на все технологические достижения, ничто не может заменить опытных рук акушера. Физическое обследование остается краеугольным камнем послеродового наблюдения. Оценка состояния матки, швов (если были), молочных желез — все это требует не только знаний, но и настоящего мастерства.

И знаете что интересно? Современное акушерство все чаще обращается к древним практикам. Например, массаж живота после родов, который веками использовался в традиционной медицине, сегодня переживает второе рождение. Исследования показывают, что он не только способствует сокращению матки, но и улучшает общее самочувствие женщины.
Психологическая поддержка: невидимый фронт
А теперь давайте поговорим о том, что нельзя измерить приборами или увидеть на УЗИ. Психологическое состояние молодой мамы — это та сфера, которой современное акушерство уделяет все больше внимания. И не зря! Послеродовая депрессия — это не выдумка и не блажь, а серьезное состояние, которое может иметь далеко идущие последствия.
Какие методы используются в акушерстве в настоящее время для решения этой проблемы? От индивидуальных консультаций с психологом до групп поддержки для молодых мам. Некоторые клиники даже предлагают онлайн-сессии, чтобы женщина могла получить помощь, не выходя из дома. Удобно, не правда ли?
Мониторинг новорожденного: две стороны одной медали
Послеродовое наблюдение — это не только о маме. Здоровье новорожденного — вот что держит в напряжении всю команду медиков. Современное акушерство предлагает целый комплекс мер для мониторинга состояния малыша.
Неонатальный скрининг — это настоящий прорыв в ранней диагностике. Простой анализ крови из пяточки может выявить целый ряд генетических заболеваний еще до появления первых симптомов. А как насчет слухового скрининга? Эта процедура, ставшая рутинной во многих роддомах, позволяет выявить нарушения слуха на самых ранних стадиях.
Грудное вскармливание: наука и искусство
Казалось бы, что может быть естественнее, чем кормление грудью? Но и здесь современное акушерство не стоит на месте. Консультанты по лактации — это новая профессия, появившаяся на стыке медицины и педагогики. Они помогают молодым мамам освоить технику кормления, решить проблемы с лактацией и обеспечить малышу правильное питание.
А знаете ли вы о существовании специальных приложений для смартфонов, которые помогают отслеживать режим кормления, вес малыша и другие важные параметры? Вот оно, слияние традиций и технологий в действии!

Домашние визиты: возвращение к истокам
Интересно, что при всей своей технологичности современное акушерство все чаще обращается к практике домашних визитов. И это не шаг назад, а настоящий прорыв в послеродовом наблюдении. Судите сами: молодая мама может получить квалифицированную помощь, не покидая дома. Это снижает риск инфекций, уменьшает стресс и позволяет специалисту оценить условия, в которых находятся мама и малыш.
Некоторые клиники идут еще дальше, предлагая услуги «мобильных бригад». В их состав входят акушер-гинеколог, педиатр и психолог. Такой комплексный подход позволяет решать самый широкий спектр проблем на месте.
Телемедицина: будущее уже здесь
А как вам идея консультации с врачом через видеосвязь? Телемедицина стремительно входит в практику послеродового наблюдения. И это не просто дань моде. Для женщин, живущих в отдаленных районах, или тех, кому сложно выбраться из дома с новорожденным, это настоящее спасение.
Но телемедицина — это не только видеоконсультации. Это еще и возможность удаленного мониторинга. Специальные устройства могут передавать врачу данные о температуре, артериальном давлении и других важных показателях в режиме реального времени. Фантастика? Нет, реальность современного акушерства!
Образование и поддержка: знание — сила
Современное акушерство понимает: информированная мама — это спокойная мама. Поэтому огромное внимание уделяется образовательным программам. Школы для молодых родителей, онлайн-курсы, информационные брошюры — все это помогает женщинам лучше понимать процессы, происходящие в их организме, и вовремя распознавать тревожные симптомы.
А как вам идея круглосуточной горячей линии для молодых мам? Такие сервисы уже работают во многих клиниках, позволяя женщинам получить квалифицированный совет в любое время суток.
Подводя итог, можно сказать, что современное акушерство в послеродовом периоде — это сложная система, сочетающая в себе высокие технологии, индивидуальный подход и глубокое понимание физиологических и психологических процессов. Оно не просто лечит — оно поддерживает, обучает и сопровождает. И знаете что? Похоже, это именно то, что нужно молодым мамам в этот непростой, но такой важный период их жизни.
Будущее акушерства: перспективные направления и технологии
Мир акушерства не стоит на месте. Он несется вперед со скоростью света, постоянно удивляя нас новыми открытиями и технологиями. Но куда же движется эта отрасль медицины? Какие методы используются в акушерстве в настоящее время, и что нас ждет завтра? Давайте заглянем за кулисы современной науки и попробуем представить, как будут выглядеть роды будущего.
Искусственный интеллект: новый член акушерской бригады
Представьте себе родильный зал, где рядом с акушером-гинекологом «работает» искусственный интеллект (ИИ). Фантастика? Отнюдь! Уже сегодня ИИ активно внедряется в акушерскую практику. Например, системы машинного обучения анализируют тысячи кардиотокограмм, помогая врачам точнее оценивать состояние плода. А как насчет ИИ, который предсказывает вероятность преждевременных родов на основе анализа множества факторов? Это уже реальность в некоторых передовых клиниках.
Но это только начало. В будущем ИИ может стать незаменимым помощником в принятии сложных решений во время родов. Представьте систему, которая в режиме реального времени анализирует все показатели матери и плода, сопоставляет их с огромной базой данных и выдает рекомендации по ведению родов. Звучит впечатляюще, не так ли?
Генетика и персонализированная медицина: роды по индивидуальному сценарию
А что если мы сможем «написать сценарий» родов еще до зачатия? Развитие генетики и персонализированной медицины открывает перед акушерством совершенно новые горизонты. Уже сейчас проводятся исследования, позволяющие на основе генетического анализа прогнозировать вероятность осложнений беременности и родов.
Но давайте пойдем дальше. Представьте, что на основе генетического профиля женщины можно будет разработать индивидуальный план ведения беременности и родов. Подобрать оптимальное питание, физические нагрузки, даже тип обезболивания во время родов — все это может стать реальностью в ближайшем будущем. Это не просто удобство — это новый уровень безопасности для матери и ребенка.
Роботы-акушеры: фантастика или реальность?
Когда речь заходит о роботах в медицине, многие представляют себе сцены из научно-фантастических фильмов. Но знаете что? Роботы уже вовсю «трудятся» в операционных, помогая хирургам проводить сложнейшие вмешательства. Так почему бы им не прийти в акушерство?
Конечно, речь не идет о том, что робот полностью заменит акушера. Но представьте себе робота-ассистента, который может выполнять рутинные манипуляции с невероятной точностью. Или робота, способного проводить УЗИ-исследования, не уставая и не теряя концентрации. Это не просто повышение эффективности — это новый уровень безопасности и точности в акушерстве.
Виртуальная и дополненная реальность: новый взгляд на роды
А теперь давайте немного помечтаем. Представьте себе роженицу, которая во время схваток «гуляет» по живописному пляжу или «плавает» среди коралловых рифов. Фантазия? Нет, это уже реальность в некоторых прогрессивных клиниках. Технологии виртуальной реальности (VR) начинают использоваться для отвлечения и расслабления во время родов.
Но это лишь верхушка айсберга. Дополненная реальность (AR) может стать незаменимым инструментом для акушеров. Представьте очки AR, которые позволяют врачу «видеть» положение плода внутри матки, отслеживать его движения в реальном времени. Это не просто круто — это может радикально повысить безопасность и эффективность родовспоможения.
Тканевая инженерия: новая эра в лечении осложнений
Одной из самых перспективных областей современной медицины является тканевая инженерия. И акушерство не остается в стороне от этого тренда. Уже сегодня ведутся исследования по использованию стволовых клеток для лечения различных осложнений беременности.
Но давайте заглянем чуть дальше. Представьте, что мы сможем «выращивать» плаценту в лаборатории для женщин с плацентарной недостаточностью. Или использовать 3D-печать для создания индивидуальных имплантов для коррекции анатомических аномалий. Звучит как научная фантастика? Возможно. Но именно так выглядит будущее акушерства.

Неинвазивная диагностика: знать все, не причиняя вреда
Одним из главных трендов современного акушерства является стремление к минимизации инвазивных процедур. И будущее в этом плане выглядит весьма оптимистично. Уже сейчас неинвазивное пренатальное тестирование (НИПТ) позволяет с высокой точностью выявлять генетические аномалии плода по крови матери.
Но это только начало. Ученые работают над методами, которые позволят получать полную информацию о здоровье плода без всякого риска для беременности. Представьте себе анализ, который по капле крови матери может рассказать все о развитии органов плода, его метаболизме, даже о потенциальных талантах будущего ребенка. Фантастика? Возможно. Но именно к этому стремится современное акушерство.
Микробиом: невидимый союзник здоровой беременности
В последние годы ученые все больше внимания уделяют микробиому человека — сообществу микроорганизмов, населяющих наш организм. И оказывается, что микробиом играет огромную роль в течении беременности и родов.
Уже сейчас ведутся исследования по использованию пробиотиков для профилактики преждевременных родов. Но будущее может быть еще интереснее. Представьте, что мы сможем «настраивать» микробиом женщины еще до беременности, чтобы обеспечить ее идеальное течение. Или использовать анализ микробиома для прогнозирования и профилактики осложнений. Это не просто новый метод — это целая философия акушерства будущего.
Телемедицина и мобильные технологии: акушер всегда на связи
Мы живем в эпоху, когда смартфон стал неотъемлемой частью нашей жизни. И акушерство не остается в стороне от этого тренда. Уже сейчас существуют приложения, позволяющие беременным женщинам отслеживать свое состояние и получать консультации врача онлайн.
Но будущее может быть еще более впечатляющим. Представьте себе «умные» пояса, которые круглосуточно мониторят состояние плода и передают данные врачу. Или системы домашнего мониторинга, которые позволят значительную часть беременности вести под наблюдением врача, не выходя из дома. Это не просто удобство — это новый уровень доступности качественной акушерской помощи.
Итак, мы заглянули в будущее акушерства, и оно выглядит захватывающе. Искусственный интеллект, роботы, виртуальная реальность — все эти технологии уже стучатся в двери родильных домов. Но знаете что самое интересное? При всей этой технологической революции главным в акушерстве остается человек — акушер, который использует все эти невероятные инструменты для того, чтобы сделать появление новой жизни максимально безопасным и комфортным. И это, пожалуй, самое важное достижение современного акушерства.
