Содержание
Применение метода непрерывной амниоинфузии с использованием подкожной порт-системы при преждевременном разрыве плодных оболочек и сроке беременности менее 28 недель. Первый опыт в России
DOI
https://dx.doi.org/10.18565/aig.2017.12.141-147
1 Кафедра перинатологии, акушерства и гинекологии лечебного факультета, ФГБOУ ВО МЗРФ Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого, Красноярск, Россия; 2 КБУЗ Красноярский краевой клинический центр охраны материнства и детства, Красноярск, Россия; 3 Кафедра генетики, цитологии и биоинженерии, ФГБОУ ВО Воронежский государственный университет, Воронеж, Россия; 4 Университетский клиника акушерства и фетальной медицины, Университетский медицинский центр Халле, Университет Мартина Лютера Халле-Витенберг, Халле, Германия; 5 Кафедра акушерства и гинекологии, ФГАОУ ВО Белгородский государственный национальный исследовательский университет, Белгород, Россия
Преждевременный разрыв плодных оболочек (ПРПО) является одной из основных причин высокой неонатальной смертности и заболеваемости.
Цель исследования. Цель этого исследования состояла в том, чтобы продлить период пролонгирования беременности без увеличения инфекционного риска с использованием метода непрерывной амниоинфузии, осуществляемого через подкожную порт-систему.
Материал и методы. У пациентки с ПРПО при сроке 25 недель гестации проводили непрерывную амниоинфузию (100 мл/ч, 2400 мл/сутки, SDP (4±2 см) через подкожную порт-систему с использованием гипотонического раствора, по свойствам подобного амниотической жидкости.
Заключение. Первый опыт применения метода непрерывной амниоинфузии позволил нам увеличить интервал пролонгирования беременности при ПРПО до 10 дней. Этот новый метод, безусловно, может использоваться у беременных с ПРПО и олиго/ангидрамнионом при сроке Ключевые слова
олиго-ангидрамнион
амниоинфузия
преждевременный разрыв плодных оболочек (ПРПО)
преждевременные роды
Полный текст статьи
доступен в «Библиотеке Врача»
1. Audra P., Le Garrec M. Rupture prématurée des membranes à terme et avant terme. EMC, Obstétrique. 2010; 5(4): 1-19.
Audra P., Le Garrec M. Rupture prématurée des membranes à terme et avant terme. EMC, Obstétrique. 2010; 5(4): 1-19.
2. Goldenberg R.L., Culhane J.F., Iams J.D., Romero R. Epidemiology and causes of preterm birth. Lancet. 2008; 371(9606): 75-84.
3. Дятлова Л.И. Факторы риска преждевременного излития околоплодных вод при беременности 22-34 недели. Международный журнал экспериментального образования. 2015; 4-2: 312-22.
4. Tchirikov M., Bapayeva G., Zhumadilov Z.Sh., Dridi Y., Harnisch R., Herrmann A. Treatment of PPROM with anhydramnion in humans: first experience with different amniotic fluid substitutes for continuous amnioinfusion through a subcutaneously implanted port system. J. Perinat. Med. 2013; 41(6): 657-63.
5. Jung E.Y., Park K.H., Lee S.Y., Ryu A., Oh K.J. Non-invasive prediction of intra-amniotic infection and/or inflammation in patients with cervical insufficiency or an asymptomatic short cervix (≤15 mm). Arch. Gynecol. Obstet. 2015; 292(3): 579-87.
6. Афанасиева М.Х., Болотских В.М., Полякова В.О. Преждевременное излитие околоплодных вод (современные взгляды на этиологию и патогенез, перспективы прогнозирования). Журнал акушерства и женских болезней. 2014; 63(3): 4-11.
Афанасиева М.Х., Болотских В.М., Полякова В.О. Преждевременное излитие околоплодных вод (современные взгляды на этиологию и патогенез, перспективы прогнозирования). Журнал акушерства и женских болезней. 2014; 63(3): 4-11.
7. Болотских В.М., Милютина Ю.П. Преждевременное излитие околоплодных вод: иммунологические и биохимические аспекты проблемы, вопросы диагностики и тактики ведения. Журнал акушерства и женских болезней. 2011; 60(4): 104-16.
8. Jung E.Y., Choi B.Y., Rhee J., Park J., Cho S.H., Park K.H. Relation between amniotic fluid infection or cytokine levels and hearing screen failure in infants at 32 wk gestation or less. Pediatr. Res. 2017; 81(2): 349-55.
9. Armstrong-Wells J., Donnelly M., Post M.D., Manco-Johnson M.J., Winn V.D., Sébire G. Inflammatory predictors of neurologic disability after preterm premature rupture of membranes. Am. J. Obstet. Gynecol. 2015; 212(2): 212. e1-9.
10. Yin N., Wang H., Zhang H., Ge H., Tan B., Yuan Y. et al. IL-27 induces a pro-inflammatory response in human fetal membranes mediating preterm birth. Int. Immunopharmacol. 2017; 50: 361-9.
Int. Immunopharmacol. 2017; 50: 361-9.
11. Dutta E.H., Behnia F., Boldogh I., Saade G.R., Taylor B.D., Kacerovský M., Menon R. Oxidative stress damage-associated molecular signaling pathways differentiate spontaneous preterm birth and preterm premature rupture of the membranes. Mol. Hum. Reprod. 2016; 22(2): 143-57.
12. Цхай В.Б., Набережнев Ю.И., Дудина А.Ю., Головченко О.В. Возможности и перспективы применения трансабдоминальной амниоинфузии для пролонгирования беременности при преждевременном разрыве плодных оболочек и маловодии. Акушерство и гинекология. 2016; 11: 5-10. https://dx.doi.org/10.18565/aig.2016.11.5-10
13. Souza A.S., Patriota A.F., Guerra G.V., Melo B.C. Evaluation of perinatal outcomes in pregnant women with preterm premature rupture of membranes. Rev. Assoc. Med. Bras. 2016; 62(3): 269-75.
14. Drassinower D., Friedman A.M., Običan S.G., Levin H., Gyamfi-Bannerman C. Prolonged latency of preterm premature rupture of membranes and risk of neonatal sepsis. Am. J. Obstet. Gynecol. 2016; 214(6): 743. e1-6.
Am. J. Obstet. Gynecol. 2016; 214(6): 743. e1-6.
15. Hofmeyr G.J., Eke A.C., Lawrie TA. Amnioinfusion for trimester preterm premature rupture of membranes. Cochrane Database Syst. Rev. 2014; (3): CD000942.
16. Roberts D., Vause S., Martin W., Green P., Walkinshaw S., Bricker L. et al. Amnioinfusion in very early preterm prelabor rupture of membranes (AMIPROM): pregnancy, neonatal and maternal outcomes in a randomized controlled pilot study. Ultrasound Obstet. Gynecol. 2014; 43(5): 490-9.
17. Van Teeffelen S., Pajkrt E., Willekes C., Van Kuijk S.M., Mol B.W. Transabdominal amnioinfusion for improving fetal outcomes after oligohydramnios secondary to preterm prelabour rupture of membranes before 26 weeks. Cochrane Database Syst. Rev. 2013; (8): CD009952.
18. Tchirikov M., Zhumadilov Z., Winarno A.S., Haase R., Buchmann J. Treatment of preterm premature rupture of membranes with oligo-/anhydramnion colonized by multiresistant bacteria with continuous amnioinfusion and antibiotic administrations through a subcutaneously implanted intrauterine port system: A case report.
19. Tchirikov M., Steetskamp J., Hohmann M., Koelbl H. Long-term amnioinfusion through a subcutaneously implanted amniotic fluid replacement port system for treatment of PPROM in humans. Eur. J. Obstet. Gynecol. Reprod. Biol. 2010; 152(1): 30-3.
20. Козлов П.В., Николаев Н.Н., Дегтярев Д.Н., Луценко Н.Н., Мальцева С.А., Дубинина Е.Н. Влияния длительности безводного промежутка на перинатальные исходы при недоношенной беременности, осложненной преждевременным разрывом плодных оболочек. Здравоохранение и медицинская техника. 2006; 3: 10-1.
Поступила 16.08.2017
Принята в печать 22.09.2017
Виталий Борисович Цхай, д.м.н., профессор, зав. кафедрой перинатологии, акушерства и гинекологии лечебного факультета ФГБОУ ВО КрасГМУ
им. проф. В.Ф. Войно-Ясенецкого. Адрес: 660022, Россия, Красноярск, ул. П. Железняка, д. 1. Телефон: 8 (923) 287-21-34. E-mail: [email protected]
 м.н., с.н.с. кафедры генетики, цитологии и биоинженерии ФГБОУ ВО Воронежский государственный университет.
м.н., с.н.с. кафедры генетики, цитологии и биоинженерии ФГБОУ ВО Воронежский государственный университет. Адрес: 394018, Россия, Воронеж, ул. Университетская площадь, д. 1. Телефон: 8 (910) 323-12-47. E-mail: [email protected]
Михаил Николаевич Чириков, д.м.н., профессор, директор университетской клиники акушерства и перинатальной медицины, Центра фетальной хирургии,
Университетская клиника (Халле) Университета Мартина Лютера Халле-Витенберг, Халле, Германия
Татьяна Тимофеевна Лобанова, заведующая отделением ультразвуковой и функциональной диагностики КБУЗ Красноярский краевой клинический центр охраны материнства и детства. Адрес: 600074, Россия, Красноярск, ул. Академика Киренского, 2А. Телефон: 8 (913) 197-48-68. E-mail: [email protected]
Анна Юрьевна Дудина, ассистент кафедры перинатологии, акушерства и гинекологии лечебного факультета ФГБОУ ВО Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого. Врач акушер-гинеколог отделения патологии беременных №1.

Олег Васильевич Головченко, к.м.н., доцент кафедры акушерства и гинекологии медицинского факультета ФГАОУ ВО Белгородский государственный национальный исследовательский университет. Адрес: 308015, Россия, Белгород, ул. Победы, д. 85. Телефон: 8 (910) 325-88-07. E-mail: [email protected]
Для цитирования: Цхай В.Б., Набережнев Ю.И., Чириков М.Н., Лобанова Т.Т., Дудина А.Ю., Головченко О.В. Применение метода непрерывной амниоинфузии с использованием подкожной порт-системы при преждевременном разрыве плодных оболочек и сроке беременности менее 28 недель. Первый опыт в России. Акушерство и гинекология. 2017; 12: 141-7.
Применение метода непрерывной амниоинфузии с использованием подкожной порт-системы при преждевременном разрыве плодных оболочек и сроке беременности менее 28 недель.
 Первый опыт в России
Первый опыт в России1 Кафедра перинатологии, акушерства и гинекологии лечебного факультета, ФГБOУ ВО МЗРФ Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого, Красноярск, Россия;
2 КБУЗ Красноярский краевой клинический центр охраны материнства и детства, Красноярск, Россия;
3 Кафедра генетики, цитологии и биоинженерии, ФГБОУ ВО Воронежский государственный университет, Воронеж, Россия;
4 Университетский клиника акушерства и фетальной медицины, Университетский медицинский центр Халле, Университет Мартина Лютера Халле-Витенберг, Халле, Германия;
5 Кафедра акушерства и гинекологии, ФГАОУ ВО Белгородский государственный национальный исследовательский университет, Белгород, Россия
Преждевременный разрыв плодных оболочек (ПРПО) является одной из основных причин высокой неонатальной смертности и заболеваемости. С потерей амниотической жидкости и развитием олиго/ангидрамниона связаны сверхранние преждевременные роды, гипоплазия легких плода и «синдром воспалительного ответа плода».
Цель исследования. Цель этого исследования состояла в том, чтобы продлить период пролонгирования беременности без увеличения инфекционного риска с использованием метода непрерывной амниоинфузии, осуществляемого через подкожную порт-систему.
Материал и методы. У пациентки с ПРПО при сроке 25 недель гестации проводили непрерывную амниоинфузию (100 мл/ч, 2400 мл/сутки, SDP (4±2 см) через подкожную порт-систему с использованием гипотонического раствора, по свойствам подобного амниотической жидкости.
Заключение. Первый опыт применения метода непрерывной амниоинфузии позволил нам увеличить интервал пролонгирования беременности при ПРПО до 10 дней. Этот новый метод, безусловно, может использоваться у беременных с ПРПО и олиго/ангидрамнионом при сроке
Преждевременный разрыв плодных оболочек (ПРПО) осложняет 4% всех беременностей, составляет 45% преждевременных родов и является одной из основных причин перинатальных потерь [1–3].
ПРПО при недоношенном сроке беременности, приводящий к массивной потере амниотической жидкости, способствует не только перинатальным потерям, но и развитию многочисленных перинатальных осложнений: легочной гипоплазии, некротизирующего энтероколита, неонатальному сепсису, неврологическим проблемам, внутрижелудочковым кровоизлияниям, деформации суставов, респираторному дистресс-синдрому плода [4].
В современной литературе отсутствует однозначное мнение об этиологии и патогенезе ПРПО. В последнее время появились исследования, посвященные роли усиленной экспрессии матричной металлопротеиназы, провоспалительных цитокинов – интерлейкина-1 (ИЛ-1), интерлейкина-6 (ИЛ-6), фактора некроза опухоли-α (TNF-α) и многих других [5–9]. Особый интерес представляет верификация ключевых сигнальных молекул, обеспечивающих целостность плодных оболочек и разработка на этой основе программ, позволяющих оптимизировать прогноз при ПРПО [5].
Воспаление в системе мать-плод, как известно, участвует в патогенезе преждевременных родов. Интерлейкин-27 (ИЛ-27) может являться посредником воспалительного ответа при некоторых осложнениях беременности. N. Yin и соавт. (2017) впервые сообщали, что при аберрантной экспрессии ИЛ-27 может выступать посредником в чрезмерной воспалительной реакции в плодных оболочках, что способствует началу преждевременных родов [10].
В исследовании J. Armstrong-Wells (2015) воспаление со стороны плода и плаценты было связано с повышенным уровнем материнских интерлейкинов (ИЛ-6 и ИЛ-8) при родах и плодовых интерлейкинов (ИЛ-1β, ИЛ-6, ИЛ-8 и TNF-α). При этом неблагоприятный неврологический исход у новорожденных был связан с воспалением со стороны плода и плаценты и коротким промежутком времени от момента ПРПО до родов, независимо от гестационного возраста при рождении или результатов ультразвукового исследования головного мозга [9].
При этом неблагоприятный неврологический исход у новорожденных был связан с воспалением со стороны плода и плаценты и коротким промежутком времени от момента ПРПО до родов, независимо от гестационного возраста при рождении или результатов ультразвукового исследования головного мозга [9].
Также установлено, что ассоциированные с окислительным стрессом повреждения мембраны эмбриона и остановки клеточного цикла могут определять неблагоприятные исходы беременности, такие как спонтанные преждевременные роды и ПРПО. Стресс-ассоциированные окислительные повреждения молекулярных сигнальных путей могут позволить врачам дифференцировать между спонтанными преждевременными родами и преждевременными родами вследствие ПРПО [11].
В настоящее время у беременных с олиго- и ангидрамнионом после ПРПО приоритетной является выжидательная тактика с проведением антибактериальной терапии, токолиза и антенатальным введением кортикостероидов для профилактики респираторного дистресс-синдрома плода [12–14].
Высокая частота развития серьезных акушерских и перинатальных осложнений, которые являются следствием ПРПО, диктуют необходимость поиска совершенно новых высокотехнологичных методов лечения. В последние годы за рубежом активно проводят исследования по применению амниоинфузии с целью пролонгирования беременности у женщин с ПРПО и маловодием, прежде всего в интересах плода [4, 15–18].
Проведенные в зарубежных клиниках немногочисленные исследования предполагают с целью повышения выживаемости крайне недоношенных новорожденных использовать в случаях ПРПО периодически повторяемые амниоинфузии для поддержания нормального объема околоплодных вод [15–17]. Проведенный анализ показал, что первый опыт применения трансабдоминальных амниоинфузий, особенно при гестационном сроке менее 26 недель, позволяет надеяться на позитивный перинатальный исход. Однако периодически повторяющиеся амниоинфузии опасны возможной травматизацией плода и инфицированием [18, 19].
М. Tchirikov впервые предложил методику постоянной амниоинфузии через подкожно имплантируемую порт-систему. Использование этой технологии позволило автору не только избежать осложнений, характерных для периодической амниоинфузии, но и пролонгировать беременность у 7 женщин после ПРПО в среднем на 49 дней на фоне семидневной антибиотикотерапии. Преимущество данной методики связано, в первую очередь, с осуществлением постоянного вымывания из полости матки бактерий и факторов воспаления [4, 19].
Использование этой технологии позволило автору не только избежать осложнений, характерных для периодической амниоинфузии, но и пролонгировать беременность у 7 женщин после ПРПО в среднем на 49 дней на фоне семидневной антибиотикотерапии. Преимущество данной методики связано, в первую очередь, с осуществлением постоянного вымывания из полости матки бактерий и факторов воспаления [4, 19].
В настоящее время продолжаются исследования, изучающие эффективность амниоинфузии после ПРПО при олиго-/ангидрамнионе, но нет достаточного числа исследований, сравнивающих акушерские и перинатальные результаты после выжидательного консервативного лечения и такого инвазивного вмешательства, каковым является амниоинфузия.
Цель исследования: оценка эффективности постоянной амниоинфузии в сочетании с антибактериальной терапией у беременных с ПРПО и олиго/ангидрамнионом при сроке беременности от 22…
Цхай В.Б., Набережнев Ю.И., Чириков М.Н., Лобанова Т.Т., Дудина А.Ю., Головченко О.В.
Легочная гипоплазия коррелирует с длительностью ангидрамниона у пациенток с почечным ангидрамнионом на ранних сроках беременности (EPRA)
- Статья
- Опубликовано:
- Эрик Б. Джелин 1 na1 ,
- Джоди Э. Хупер ORCID: orcid.org/0000-0002-8209-3559 2 na1 ,
- Элеонора Дурегон 3 ,
- Алекс К. Уильямсон ORCID: orcid.org/0000-0003-2724-1704 4 ,
- Сара Олсон 5 ,
- Кристин Фогтлайн 5,6 и Анги Джеджи
- … ORCID: orcid.org/0000-0002-1792-4029 7,8
Журнал перинатологии том 41 , страницы 1924–1929 (2021)Цитировать эту статью
221 доступ
Сведения о показателях
Субъекты
- Почки
- Детская болезнь почек
- Заболевания дыхательных путей
Abstract
Исходная информация
Почечный ангидраманиоз на ранних сроках беременности (EPRA) возникает, когда у плода развивается анурия до 22 недель гестационного возраста (GA), и считается летальным во всех случаях.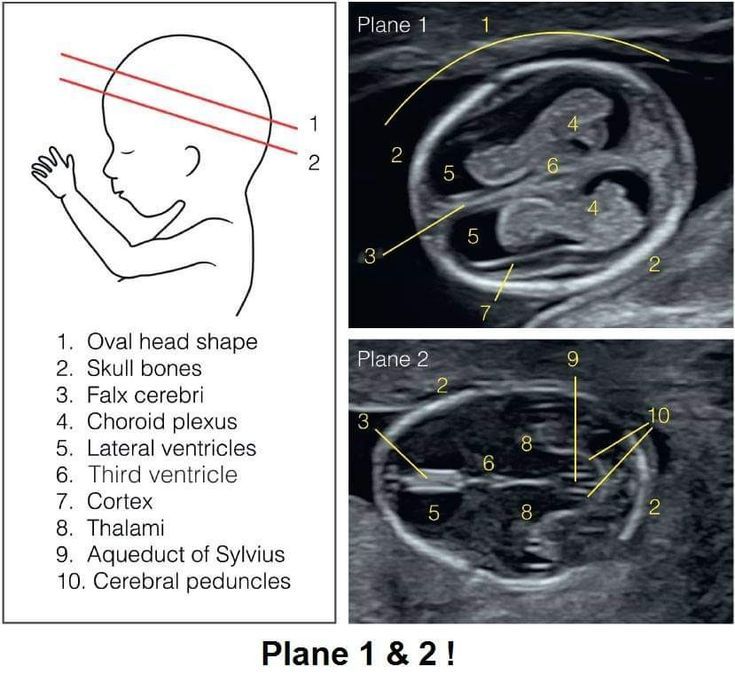 Серийные амниоинфузии успешно уменьшают летальную легочную гипоплазию, связанную с EPRA, и приводят к выживанию новорожденных, перитонеальному диализу и пересадке почки.
Серийные амниоинфузии успешно уменьшают летальную легочную гипоплазию, связанную с EPRA, и приводят к выживанию новорожденных, перитонеальному диализу и пересадке почки.
Цель
Мы стремились оценить легочную патологию нелеченых плодов и новорожденных, перенесших EPRA.
Дизайн исследования
Это ретроспективная серия случаев всех плодов и новорожденных с диагнозом изолированного EPRA, которые подверглись вскрытию в одном центре третичной медицинской помощи в период с 1987 по 2018 год. Данные вскрытия коррелировали с данными УЗИ и гестационным возрастом при родах. Регистрировали массу плода, массу легких и стадию развития легких.
Результаты
Девятнадцать случаев соответствовали критериям для анализа и варьировались от 16 до 38 недель ГВ при прерывании беременности или рождении. Наблюдаемое и ожидаемое (O/E) отношение массы легких к массе тела было в значительной степени связано с ГА (9). 0089 r = -0,51, p = 0,03), так что по мере увеличения GA отношение O/E уменьшалось. При ограничении пациентов старше 22 недель это соотношение усиливалось ( r = -0,75, p = 0,01). Важно отметить, что общая масса тела O/E не имела отношения к GA.
0089 r = -0,51, p = 0,03), так что по мере увеличения GA отношение O/E уменьшалось. При ограничении пациентов старше 22 недель это соотношение усиливалось ( r = -0,75, p = 0,01). Важно отметить, что общая масса тела O/E не имела отношения к GA.
Заключение
Это исследование показывает, что степень легочной гипоплазии в EPRA увеличивается с увеличением продолжительности ангидрамниона. Это говорит о том, что амниоинфузии, вероятно, принесут наибольшую пользу, как только их можно будет начать.
Это предварительный просмотр содержимого подписки, доступ через ваше учреждение
Варианты доступа
Подписаться на журнал
Получить полный доступ к журналу на 1 год
118,99 €
всего 9,92 € за выпуск
Подписаться
Расчет налогов будет завершен во время оформления заказа.
Купить статью
Получите ограниченный по времени или полный доступ к статье на ReadCube.
32,00 $
Купить
Все цены указаны без учета стоимости.
Рис. 1: Нормальная масса легких и масса легких по шкале EPRA в зависимости от гестационного возраста (наложение). Рис. 2: O/E Легкие: соотношение веса плода в зависимости от гестационного возраста. Рис. 3. График наблюдаемого/ожидаемого отношения массы легких к массе тела в разбивке по группам ГА (≤22 против >22 недель) свидетельствует об отрицательной линейной зависимости между обеими группами ГА. Рис. 4: График наблюдаемой и ожидаемой массы плода по GA.Ссылки
Джелин А.С., Сагасер К.Г., Форстер К.Р., Ибекве Т., Нортон М.Е., Джелин Э.Б. Этиология и лечение почечной ангидрамниона на ранних сроках беременности: есть ли место для серийных амниоинфузий? Пренат Диагн.
 2020; 40: 528–37.
2020; 40: 528–37.Артикул Google ученый
О’Хара Э.М., Джелин А.С., Миллер Дж.Л., Руано Р., Аткинсон М.А., Башат А.А. и соавт. Амниоинфузии для лечения ангидрамниона с ранним началом, вызванного почечными аномалиями: предпосылки и обоснование исследования почечной ангидрамниона у плода. Диагностика плода Тер. 2019;45:365–72.
Артикул Google ученый
Киттерман Дж.А. Влияние механических сил на рост легких плода. Клин Перинатол. 1996;23:727–40.
Артикул КАС Google ученый
Joe P, Wallen LD, Chapin CJ, Lee CH, Allen L, Han VK, et al. Влияние механических факторов на рост и созревание легких у эмбрионов овец. Am J Physiol. 1997; 272:L95–105.
КАС пабмед Google ученый
- «>
Najrana T, Ramos LM, Abu Eid R, Sanchez-Esteban J. Малогидрамнион снижает размер клеток легких и препятствует эпителиально-эндотелиальному развитию. Педиатр Пульмонол. 2017;52:746–56.
Артикул Google ученый
Нельсон К.М., Глегхорн Дж.П., Панг М.Ф., Яслов Дж.М., Гудвин К., Варнер В.Д. и др. Микрожидкостные грудные полости показывают, что трансмуральное давление контролирует скорость развития легких. Разработка. 2017; 144:4328–35.
КАС пабмед ПабМед Центральный Google ученый
Чен К.М., Ван Л.Ф., Чжоу Х.К., Лан Ю.Д. Маловодие снижает экспрессию тромбоцитарного фактора роста в легких плода крысы. Неонатология. 2007;92: 187–93.
Артикул КАС Google ученый
Хара А., Чапин С.Дж., Эртсей Р., Киттерман Дж.А. Изменения растяжения легких плода изменяют экспрессию фактора роста эндотелия сосудов и его изоформ в развивающемся легком крысы.
 Педиатр рез. 2005; 58:30–7.
Педиатр рез. 2005; 58:30–7.Артикул КАС Google ученый
Warburton D. Обзор развития легких у новорожденного человека. Неонатология. 2017;111:398–401.
Артикул Google ученый
Шитни Дж.С. Развитие легкого. Сотовые Ткани Res. 2017; 367: 427–44.
Артикул Google ученый
Weaver DJ Jr, Somers MJG, Martz K, Mitsnefes MM. Клинические исходы и выживаемость у педиатрических пациентов, начинающих хронический диализ: отчет регистра NAPRTCS. Педиатр Нефрол. 2017;32:2319–30.
Артикул Google ученый
Кэри В.А., Тэлли Л.И., Серинг С.А., Яскула Дж.М., Матиас Р.С. Результаты диализа, начатого в неонатальный период для лечения терминальной стадии почечной недостаточности: специальный анализ североамериканских педиатрических почечных испытаний и совместных исследований.
 Педиатрия. 2007; 119: e468–73.
Педиатрия. 2007; 119: e468–73.Артикул Google ученый
Мицнефес М.М., Ласкин Б.Л., Даххоу М., Чжан С., Фостер Б.Дж. Риск смертности среди детей, первоначально получавших диализ по поводу терминальной стадии болезни почек, 1990–2010. ДЖАМА. 2013; 309:1921–9.
Артикул КАС Google ученый
Кэмерон Д., Луптон Б.А., Фаркухарсон Д., Хируки Т. Амниоинфузии при агенезии почек. Акушерство Гинекол. 1994; 83: 872-6.
КАС пабмед Google ученый
Bienstock JL, Birsner ML, Coleman F, Hueppchen NA. Успешное внутриутробное вмешательство по поводу двусторонней агенезии почек. Акушерство Гинекол. 2014; 124:413–5.
Артикул Google ученый
Шелдон К.Р., Ким Э.
 Д., Чандра П., Консепсьон В., Галло А., Су С. и др. Два младенца с двусторонней агенезией почек, которые были переведены с хронического перитонеального диализа на трансплантацию почки. педиатр транспл. 2019;23:e13532.
Д., Чандра П., Консепсьон В., Галло А., Су С. и др. Два младенца с двусторонней агенезией почек, которые были переведены с хронического перитонеального диализа на трансплантацию почки. педиатр транспл. 2019;23:e13532.Google ученый
Мокси-Мимс М, Раджу ТНК. Ангидрамнион при пороках развития почек: Резюме семинара Национального института здравоохранения. Акушерство Гинекол. 2018;131:1069–79.
Артикул Google ученый
Sugarman J, Anderson J, Baschat AA, Herrera Beutler J, Bienstock JL, Bunchman TE, et al. Этические соображения относительно амниоинфузий для лечения двусторонней почечной агенезии плода. Акушерство Гинекол. 2018;131:130–4.
Артикул Google ученый
Комсток Дж., Фуртадо Л., Брайсон С. Диагностическая патология: гистология плода.
 1-е изд. Солт-Лейк-Сити: электронная книга Amirsys, Inc; 2013.
1-е изд. Солт-Лейк-Сити: электронная книга Amirsys, Inc; 2013.Арчи Дж.Г., Коллинз Дж.С., Лебель Р.Р. Количественные стандарты вскрытия плода и новорожденного. Ам Джей Клин Патол. 2006; 126: 256–65.
Артикул Google ученый
Куни Т.П., Терлбек В.М. Метод радиального альвеолярного подсчета Эмери и Митала: переоценка 2-внутриутробного и раннего постнатального роста легких. грудная клетка. 1982; 37: 580–3.
Артикул КАС Google ученый
Моссингер А.С., Хардинг Р., Адамсон Т.М., Сингх М., Киу Г.Т. Роль объема легочной жидкости в росте и созревании легкого плода овцы. Джей Клин Инвест. 1990;86:1270–7.
Артикул КАС Google ученый
Чен К.М., Чжоу Х.К., Ван Л.Ф., Ланг Ю.Д. Экспериментальное олигогидрамнион снижает содержание коллагена в гипоплазированных легких плода крысы.
 Экспер Биол Мед. 2008; 233:1334–40.
Экспер Биол Мед. 2008; 233:1334–40.Артикул КАС Google ученый
Jelin E, Lee H. Окклюзия трахеи при врожденной диафрагмальной грыже плода: опыт США. Клин Перинатол. 2009;36:349–61,ix.
Артикул Google ученый
Риддл С., Хабли М., Таббах С., Лим Ф.Ю., Мингес М., Кингма П. и др. Современные исходы лечения пациентов с изолированной двусторонней агенезией почек с вмешательством плода и без него. Диагностика плода Тер. 2020; 47: 675–81.
Артикул Google ученый
Ву К.С., Чен К.М., Чжоу Х.К. Легочная гипоплазия, вызванная маловодием: результаты исследований на животных и популяционное исследование. Педиатр Неонатол. 2017;58:3–7.
Артикул Google ученый
Ссылки на скачивание
Благодарности
EBJ получил финансирование от NIH NICHD RO1HD100540-01. ACJ получил финансирование от NIH NIDDK K23DK119949-02.
ACJ получил финансирование от NIH NIDDK K23DK119949-02.
Информация об авторе
Примечания авторов
Эти авторы внесли равный вклад: Эрик Б. Джелин, Джоди Э. Хупер.
Авторы и организации
Отделение детской хирургии, кафедра хирургии, Университет Джона Хопкинса, Балтимор, Мэриленд, США , США
Джоди Э. Хупер
Отделение трансляционной геронтологии, Национальный институт старения (NIA/NIH), Балтимор, Мэриленд, США
Элеонора Дурегон
Кафедра патологии и лабораторной медицины, Медицинская школа Цукера в Хофстра/Нортуэлл, Хемпстед, штат Нью-Йорк, США
Алекс К. Уильямсон
Биостатистика, эпидемиология Школа медицины Джонса Хопкинса, Балтимор, Мэриленд, США
Сара Олсон и Кристин Фёгтлайн
Педиатрический факультет, Университет Джонса Хопкинса, Балтимор, Мэриленд, США
Кристин Фёгтлайн
Отделение гинекологии и акушерства матери и плода, Университет Джона Хопкинса, Балтимор, Мэриленд, США
Angie C.
 Jelin
Jelin
Авторы
- Eric B. Jelin
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Джоди Э. Хупер
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Eleonora Duregon
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Alex K. Williamson
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Сара Олсон
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Kristin Voegtline
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Angie C.
 Jelin
JelinПросмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Вклады
Все перечисленные авторы внесли свой вклад в разработку и реализацию исследования, в анализ результатов и в написание рукописи.
Автор, ответственный за переписку
Энджи С. Джелин.
Заявление об этике
Конкурирующие интересы
Авторы не заявляют об отсутствии конкурирующих интересов.
Дополнительная информация
Примечание издателя Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Права и разрешения
Перепечатка и разрешения
Об этой статье
RAFT – исследование почечной ангидрамниоза плода
Ранняя беременность почечная ангидрамнион (EPRA) Ранняя беременность почечная ангидрамнион (EPRA) – это состояние, при котором беременная женщина не имеет амниотической жидкости вокруг плода (ребенка) из-за проблем с почечная система. EPRA возникает, когда почки, мочеточники, мочевой пузырь или уретра ребенка не развиваются должным образом, что препятствует способности ребенка производить или выделять мочу. После 16 недель беременности моча ребенка вносит более 90% амниотической жидкости вокруг ребенка. Амниотическая жидкость необходима для нормального развития легких у ребенка. Нелеченый EPRA считается повсеместно фатальным.
EPRA возникает, когда почки, мочеточники, мочевой пузырь или уретра ребенка не развиваются должным образом, что препятствует способности ребенка производить или выделять мочу. После 16 недель беременности моча ребенка вносит более 90% амниотической жидкости вокруг ребенка. Амниотическая жидкость необходима для нормального развития легких у ребенка. Нелеченый EPRA считается повсеместно фатальным.
В исследовании Renal Anhydramnios Fetal Therapy (RAFT) исследуется экспериментальное лечение матерей и их детей, пострадавших от EPRA. Исследование направлено на то, чтобы определить, могут ли повторяющиеся инъекции жидкости (амниоинфузии) в матку обратить вспять эффекты EPRA, чтобы пораженные дети имели достаточную функцию легких, чтобы выжить вне матки.
Исследование Renal Anhydramnios Fetal Therapy (RAFT) проводится под руководством д-ра Джены Миллер, доктора медицинских наук, доцента кафедры гинекологии и акушерства в Центре терапии плода Джона Хопкинса, и доктора Мередит А. Аткинсон, доктора медицинских наук, MHS. , доцент кафедры педиатрии отделения детской нефрологии. Он финансируется Национальным институтом детского здоровья и развития человека Юнис Кеннеди Шрайвер (NICHD) и поддерживается Североамериканской сетью терапии плода.
Аткинсон, доктора медицинских наук, MHS. , доцент кафедры педиатрии отделения детской нефрологии. Он финансируется Национальным институтом детского здоровья и развития человека Юнис Кеннеди Шрайвер (NICHD) и поддерживается Североамериканской сетью терапии плода.
- ClinicalTrials.gov Идентификатор: NCT03500328
- Информация о проекте в отчете NIH
Для получения дополнительной информации, пожалуйста, свяжитесь с одним из участвующих клинических центров, указанных на карте ниже.
RAFT финансируется Национальным институтом детского здоровья и развития человека Юнис Кеннеди Шрайвер (NICHD) и поддерживается Североамериканской сетью терапии плода (NAFTNet) и NAPRTCS.
Джелин А.С., Сагасер К.Г., Форстер К.Р., Ибекве Т., Нортон М.Е., Джелин Э.Б. Этиология и лечение почечной ангидрамниона на ранних сроках беременности: есть ли место для серийных амниоинфузий? Пренат Диагн. 2020 апр;40(5):528-537. doi: 10.1002/pd.5658. Epub 2020 19 фев. PMID: 32003482.
Джелин Э.Б., Аткинсон М., Кейзер А., Блюменфельд Ю.Дж., Башат А.А. Ответ на «Современные результаты лечения пациентов с изолированной двусторонней агенезией почек с вмешательством плода и без него» исследователей RAFT. Диагностика плода Тер. 2020;47(10):785-786. дои: 10.1159/000509749. Epub 2020, 7 августа. PMID: 32772023; PMCID: PMC7556342.
Шугарман Дж., Андерсон Дж., Башат А.А., Эррера Бейтлер Дж., Биенсток Дж.Л., Банчман Т.Э., Десаи Н.М., Гейтс Э., Голдберг А., Гримм П.С., Генри Л.М., Джелин Э.Б., Джонсон Э., Хертенштейн К.Б., Мастроянни А.С., Меркурио М.Р. , Neu A, Nogee LM, Polzin WJ, Ralston SJ, Ramus RM, Singleton MK, Somers MJG, Wang KC, Boss R. Этические соображения относительно амниоинфузий для лечения двусторонней почечной агенезии плода. Акушерство Гинекол. 2018 Январь; 131(1):130-134. дои: 10.1097/АОГ.0000000000002416. PMID: 29215523.
Джелин Э.Б., Аткинсон М., Кейзер А., Блюменфельд Ю.Дж., Башат А.А. Ответ на «Современные результаты лечения пациентов с изолированной двусторонней агенезией почек с вмешательством плода и без него» исследователей RAFT.
