Содержание
УЗИ, не могу успокоиться
19.03.2012 15:20
Б 9 акушерских недель, была сегодня на узи, КТР по сроку, сердечко бьётся, а плодное яйцо на 6,5 недель, очень маленькое. Сказали надо срочно к врачу и назначать лечение,подкармливать плодное яйцо. Вышла из кабинета и разревелась. Неужели всё так плохо?!! В заключении написали : нельзя исключить микроамнио…(дальше неразборчиво)
Пожалуйста,отзовитесь, кому ставили маленькое плодное яйцо не по сроку. Что меня ждёт дальше?
Есть очень нехороший опыт в прошлую Б, поэтому сейчас любое отклонение вызывает панику.
автор
19.03.2012 15:35
может была поздняя овуляция? Не переживайте раньше времени.
Дяка **
19.03.2012 17:13
Спасибо,я взяла себя в руки. Почитала, что это не так то вроде и страшно. Вопрос в том,зачем врач нагнетала обстановку? неприятно как-то
автор
19.03.2012 21:08
Врач (и не только ваша) руководствуется принципом «лучше перебдеть чем недобдеть».
Дяка **
19.03.2012 15:46
У меня такое же было!!! Ставили гипоплазию амниона.
Уже родила здорового мальчишку!!!!
boa C.S.
19.03.2012 17:07
Спасибо за поддержку! Положительный пример как нельзя кстати)
автор
20.03.2012 17:06
Девочки а как расшифровывается КТР? У меня это первая беременность, я еще не все термины знаю))
skyler *
20.03.2012 17:19
http://budumamoi.ru/ktr.html
Anonymous
20.03.2012 19:00
Спасибо))
skyler *
20.03.2012 20:40
31 мм на 6,5 недель??! это Вам что-то не то написали, или не так поняли. Или это еще какой-то вариант измерения ПЯ (обычно высчитывают средний размер)
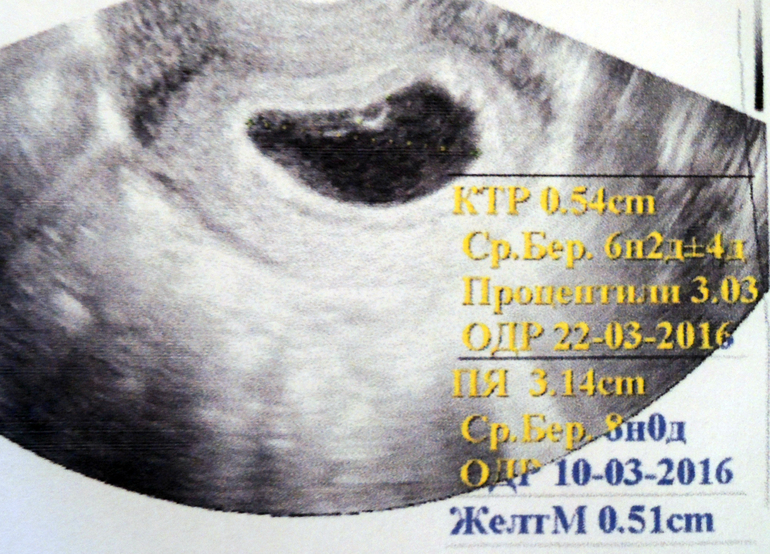
 Вот по размеру ПЯ мне нарисовали 7-8 недель, и напряглись, потому что перед этим у меня подряд 2 ЗБ. Назначили много чего, и я это все пью, потому что сами понимаете, боюсь повторения. Сегодня была снова на узи, ровно 10 ак недель, КТР = 21 мм, ПЯ 29 мм, и врач УЗИ, и ведущий меня врач остались довольны ростом, теперь все на 9-10 недель. Будем, конечно, и дальше наблюдаться в динамике почаще, но 31 мм вообще, кажется, не должно вызывать никаких вопросов. Удачи!
Вот по размеру ПЯ мне нарисовали 7-8 недель, и напряглись, потому что перед этим у меня подряд 2 ЗБ. Назначили много чего, и я это все пью, потому что сами понимаете, боюсь повторения. Сегодня была снова на узи, ровно 10 ак недель, КТР = 21 мм, ПЯ 29 мм, и врач УЗИ, и ведущий меня врач остались довольны ростом, теперь все на 9-10 недель. Будем, конечно, и дальше наблюдаться в динамике почаще, но 31 мм вообще, кажется, не должно вызывать никаких вопросов. Удачи!Anonymous
20.03.2012 20:59
Спасибо, что ответили. Врач УЗИ и на осмотре сказала 31 мм и написала в заключении. По таблицам в инете у меня и размер КТР и размер ПЯ соответствует 8 неделям Б. У меня 9 недель по месячным, поэтом развите на 8 недель меня не пугает, я точно знаю, что зачатие случилось через 2 недели после М. Меня очень напрягло,что ПЯ на 6,5 недель, вот это явное отставание, но опять же я склонна думать, что УЗИстка ошиблась, 31 мм не может быть на 6,5 недель (судя по интернетовским таблицам)
 А Вам большое спасибо за ответ, я тоже очень трясусь за свою Б. Здорового малыша и лёгкой Б.
А Вам большое спасибо за ответ, я тоже очень трясусь за свою Б. Здорового малыша и лёгкой Б.автор
05.03.2020 12:46
Здравствуйте!) По узи у меня сейчас тоже самое эмбрион 16 мм (8 недель и 3 дня), а плодное яйцо 18мм (6недель и 5 дней) Скажете пожалуйста как прошла ваша беременность?)
marina_k_a_265287222 +
19.03.2012 17:11
Может есть здесь кто-нибудь как и я 9недельный?
Почему узистка 31мм плодного яйца определила на 6,5 недель? по таблицам в инете это не меньше 8 недель.
Поделитесь своими показателями,пожалуйста. Я немного успокоилась, но сердце всё равно не на месте.
автор
19.03.2012 20:51
Успокаивайтесь совсем. Тревогой вы ничего не измените. У меня в 8 недель узи показывало 7. Это нормально.
Особенно учитывая цикл и что дети всегда растут и развиваются скачкообразно. Сегодня там у вас 7 недель, через неделю будет 9. И на более поздних сроках тоже будут расхождения по срокам. То срок в срок, то на неделю отстает, то на больший срок.
Отдыхайте и не переживайте. Скорее всего узистка ошиблась. Для своего спокойствия можете переделать.
Lingvo V.I.P.
19.03.2012 21:21
Откопала свой листик УЗ диагностики: 8,5 недель, КТР 16 мм, плодное 45*20
Дяка **
19.03.2012 22:04
Я помню в начале этой беременности ревели из-за ХГЧ, у меня тоже оно отсатвало на 1,5 недели. Я была просто в шоке. А потом выяснилось, что была поздняя овуляция. Удачи вам!
Anonymous
19.03.2012 22:19
У меня полезавтра УЗИ, будет ровно 9 недель(по месячным), напишу потом что скажут. Не переживайте!
skyler *
20. 03.2012 15:54
03.2012 15:54
И у меня завтра УЗИ, тоже посмотрим на цифры
Фрешка *
20.03.2012 15:55
Очень жду вашего ответа,напишите мне завтра,пожалуйста
автор
21.03.2012 12:48
21.9 мм, срок поставили 9 ак. недель, сказали что все нормально)))
skyler *
21.03.2012 19:53
21,9 это плодное яйцо? а КИР при этом какой?
Спасибо, что написали)
автор
19.03.2012 21:05
ага! мне тоже так сказали! только через неделю уже все было в норме + разглядели что там их два! А я неделю рыдала, вообще не понимаю как мои дети все это вынесли 🙂 Теперь 2 лосика уже 8ми лет! Никогда не паникуйте…Всегда есть шанс ошибки или шанс все исправить (вылечить или как-то помочь) Легкой беременности и здорового малыша!
Anonymous
20.03.2012 15:20
У меня сейчас 9-я неделя, КТР был 28 мм если не ошибаюсь . По узи поставили 6 недель, от ПДПМ — 8-9 недель.
По узи поставили 6 недель, от ПДПМ — 8-9 недель.
20.03.2012 15:53
Девочки,спасибо всем большое!В 13 недель записана на плановое УЗИ , подожду, посмотрим, что там скажут, а пока просто к врачу схожу. Раз малявочка по сроку, плодное яйцо , надеюсь, подрастёт.
автор
Открыть в форуме
MMF/MPA является основным медиатором отсроченного гуморального ответа со сниженным снижением уровня антител у реципиентов почечного трансплантата после вакцинации мРНК SARS-CoV-2 показатели сероконверсии по сравнению с нормальной популяцией после вакцинации мРНК SARS-CoV-2 (1–3). Таким образом, исследования, в том числе наше исследование Dia-Vacc, идентифицировали антиметаболит MMF/MPA (помимо белатацепта) как критический тип иммунодепрессанта, связанный с отсутствием сероконверсии через 2 месяца после вакцинации против SARS-CoV-2 у KTR (1–3). В течение 6 месяцев последующих исследований сероконверсированные KTR [по сравнению с медицинским персоналом (МП)] подвергались риску сильного снижения антител IgG и RBD-IgG, но ни антител IgA, ни клеточного иммунитета (4).
 Таким образом, титры антител KTR достигали пика на более низком уровне, а выраженное снижение антител сочеталось с усилением ответа IgG или RBD-IgG по крайней мере у 15% пациентов. Несмотря на то, что MMF/MPA вводят большинству всех реципиентов органов во всем мире, его влияние на снижение уровня антител у сероконвертированных реципиентов трансплантата после вакцинации мРНК SARS-CoV-2 остается неясным. Согласно ранее существовавшим данным о влиянии ММФ/МПА на связанную с вакцинацией сероконверсию и образование антител, мы предположили, что лечение ММФ/МПА может также приводить к выраженному снижению уровня антител в течение дополнительных 4 месяцев наблюдения после сероконверсии в 8-недельный момент времени после начала вакцинации мРНК у 132 KTR когорты DIA-Vacc.
Таким образом, титры антител KTR достигали пика на более низком уровне, а выраженное снижение антител сочеталось с усилением ответа IgG или RBD-IgG по крайней мере у 15% пациентов. Несмотря на то, что MMF/MPA вводят большинству всех реципиентов органов во всем мире, его влияние на снижение уровня антител у сероконвертированных реципиентов трансплантата после вакцинации мРНК SARS-CoV-2 остается неясным. Согласно ранее существовавшим данным о влиянии ММФ/МПА на связанную с вакцинацией сероконверсию и образование антител, мы предположили, что лечение ММФ/МПА может также приводить к выраженному снижению уровня антител в течение дополнительных 4 месяцев наблюдения после сероконверсии в 8-недельный момент времени после начала вакцинации мРНК у 132 KTR когорты DIA-Vacc.Методы
Дизайн исследования
В 2- (T2) и 6-месячной (T3) оценке (дополнительный рисунок 1) проспективного обсервационного исследования DIA-Vacc (1) (NCT04799808) мы проанализировали специфические клеточные ( анализ высвобождения интерферона-γ) и гуморальный иммунный ответ после двукратного введения мРНК SARS-CoV-2 без третьей вакцинации у 112 из 132 KTR (см. Дополнительную таблицу 1) с сероконверсией (положительный результат на антитела de novo IgA или IgG с помощью ELISA (связанные с ферментом иммуноферментный анализ), КТР 112 ). Кроме того, 26 из 132 KTR с сероконверсией представляют собой отдельную группу только IgA de novo положительных, но IgG отрицательных KTR IgA на Т2 (рис. 1, также называемых «слабо сероконверсионными»). В 20 из 26 случаев этой группы KTR IgA по непредвиденному индивидуальному решению диализных центров (процедура, разрешенная законом в Германии) была проведена дополнительная третья вакцинация через 4,2 ± 1 месяца. В Т0 (начало вакцинации), Т2 и Т3 у всех участников исследования оценивали антитела IgG или IgA, специфичные для SARS-CoV-2, к белку Spike S1 и антитела к рецептор-связывающему домену (RBD-IgG) в Т2 или Т3. (1). Уровни и изменения титра классифицировались по-разному в зависимости от того, на что обращали внимание. Для оценки и сравнения подгрупп, определяемых ответом сопоставимой экспрессии (т.
Дополнительную таблицу 1) с сероконверсией (положительный результат на антитела de novo IgA или IgG с помощью ELISA (связанные с ферментом иммуноферментный анализ), КТР 112 ). Кроме того, 26 из 132 KTR с сероконверсией представляют собой отдельную группу только IgA de novo положительных, но IgG отрицательных KTR IgA на Т2 (рис. 1, также называемых «слабо сероконверсионными»). В 20 из 26 случаев этой группы KTR IgA по непредвиденному индивидуальному решению диализных центров (процедура, разрешенная законом в Германии) была проведена дополнительная третья вакцинация через 4,2 ± 1 месяца. В Т0 (начало вакцинации), Т2 и Т3 у всех участников исследования оценивали антитела IgG или IgA, специфичные для SARS-CoV-2, к белку Spike S1 и антитела к рецептор-связывающему домену (RBD-IgG) в Т2 или Т3. (1). Уровни и изменения титра классифицировались по-разному в зависимости от того, на что обращали внимание. Для оценки и сравнения подгрупп, определяемых ответом сопоставимой экспрессии (т. е. снижением титра до сопоставимых абсолютных значений), были определены уровни и соответствующие пределы (см. 2.4 Интервальная классификация по уровням). Для общей оценки и сравнения в отношении относительных изменений, определяемых как повышение, равенство или снижение титров, были сформированы диапазоны. Для последнего использовался диапазон 20% для T3 по сравнению с T2 изменения титров/значений антител и анализа высвобождения интерферона-γ (IGRA) (увеличены, равны или уменьшены) и был рассчитан процент пациентов в пределах каждого диапазона ( Таблица 1). Кроме того, временной ход антител был проанализирован по шкале интервалов. Обнаруживаемые диапазоны значений антител против спайков S1-IgG и RBD-IgG были разделены на пять интервалов, обозначенных от 0 до 4 (называемых «уровнями» в анализе данных), и изменение уровней, варьирующееся от -4 до +4, рассчитывали для каждого пациента. Снижение уровня от Т2 до Т3 не менее чем на две единицы определялось как сильное снижение (1).
е. снижением титра до сопоставимых абсолютных значений), были определены уровни и соответствующие пределы (см. 2.4 Интервальная классификация по уровням). Для общей оценки и сравнения в отношении относительных изменений, определяемых как повышение, равенство или снижение титров, были сформированы диапазоны. Для последнего использовался диапазон 20% для T3 по сравнению с T2 изменения титров/значений антител и анализа высвобождения интерферона-γ (IGRA) (увеличены, равны или уменьшены) и был рассчитан процент пациентов в пределах каждого диапазона ( Таблица 1). Кроме того, временной ход антител был проанализирован по шкале интервалов. Обнаруживаемые диапазоны значений антител против спайков S1-IgG и RBD-IgG были разделены на пять интервалов, обозначенных от 0 до 4 (называемых «уровнями» в анализе данных), и изменение уровней, варьирующееся от -4 до +4, рассчитывали для каждого пациента. Снижение уровня от Т2 до Т3 не менее чем на две единицы определялось как сильное снижение (1).
Рисунок 1 .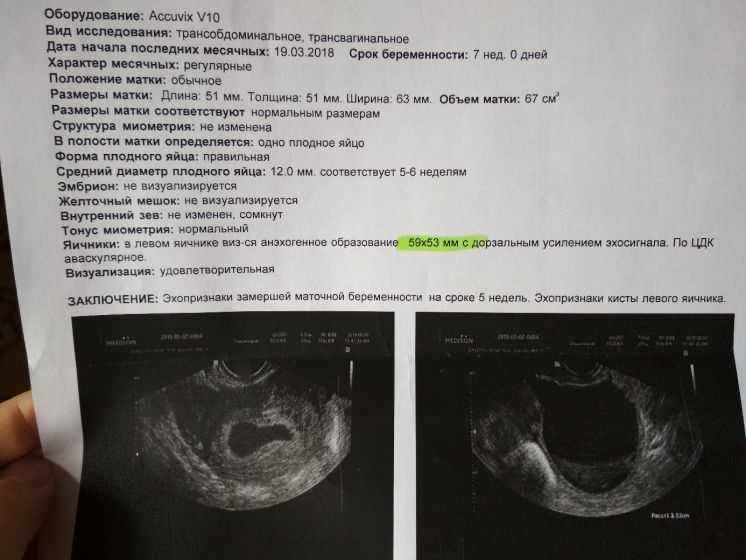
Таблица 1 . Показатели иммунного ответа через 6 месяцев после вакцинации (T3) по сравнению с T2 в когорте сероконвертированных реципиентов почечного трансплантата (KTR) 112 .
Исходный план исследования
В первоначальном неинтервенционном проспективном обсервационном исследовании DIA-Vacc (1) участвовали первые 26 из 36 региональных нефрологических центров. Дальнейшие центры не могут быть рассмотрены из-за финансовых ограничений. В общей сложности 3101 участник был зачислен для изучения динамики специфического клеточного ответа и/или гуморальной сероконверсии к заболеванию и/или вакцинации против SARS-CoV-2 у MP, DP и 368 KTR (см. Рисунок 1). Чтобы сообщить о чистых показателях гуморальной сероконверсии, как указано здесь, была создана «чистая когорта вакцинации», ретроспективно исключающая всех симптоматических и бессимптомных пациентов с COVID-19. инфицированных или умерших участников до, во время и после вакцинации (до Т2). Дальнейшее описание см. в другом месте (1). Другая когорта, называемая «когорта клинической вакцинации», состоит из когорты «чистой вакцинации», но включает всех участников, которые перенесли симптоматическое или бессимптомное заболевание (или смерть) COVID-19 строго во время или после вакцинации для оценки клинических результатов вакцинации. Начало исследования (Т0) было непосредственно перед первой вакцинацией. Дальнейший мониторинг моментов времени описан в другом месте (1). По наличию вакцины первоначально только первые четыре диализных центра были назначены на кампанию вакцинации и получили мРНК BNT162b2, в то время как все остальные последующие диализные центры получили вакцину мРНК-1273 для обеих вакцинаций. Ни один диализный центр, ни пациент, ни член парламента, ни исследовательский центр (Дрезден) не имели выбора или влияния в отношении типа вакцины. Все диализные центры были проинформированы по одновременная электронная почта из центрального института вакцинации о начале кампании вакцинации.
инфицированных или умерших участников до, во время и после вакцинации (до Т2). Дальнейшее описание см. в другом месте (1). Другая когорта, называемая «когорта клинической вакцинации», состоит из когорты «чистой вакцинации», но включает всех участников, которые перенесли симптоматическое или бессимптомное заболевание (или смерть) COVID-19 строго во время или после вакцинации для оценки клинических результатов вакцинации. Начало исследования (Т0) было непосредственно перед первой вакцинацией. Дальнейший мониторинг моментов времени описан в другом месте (1). По наличию вакцины первоначально только первые четыре диализных центра были назначены на кампанию вакцинации и получили мРНК BNT162b2, в то время как все остальные последующие диализные центры получили вакцину мРНК-1273 для обеих вакцинаций. Ни один диализный центр, ни пациент, ни член парламента, ни исследовательский центр (Дрезден) не имели выбора или влияния в отношении типа вакцины. Все диализные центры были проинформированы по одновременная электронная почта из центрального института вакцинации о начале кампании вакцинации. У всех участников исследования (соответствие требованиям для лиц старше 18 лет и подписанного информированного согласия) в Т0, Т2 и Т3 были проведены вышеупомянутые измерения антител с использованием ИФА Euroimmun на анализаторах Euroimmun (5–9). Чтобы изучить клеточный иммунный ответ на SARS-CoV-2 в подгруппах, анализ высвобождения интерферона-γ, специфичного для SARS-CoV-2 (Euroimmun-SARS-CoV-2-IGRA для исследований, использует только ET 2606-3003 и EQ 6841-9).6011,2) (10). Подгруппа для IGRA была сформирована следующим образом: для анализа Т-клеток нужны яркие клетки. Для достижения высокой жизнеспособности в образцах IGRA обработка должна начинаться через <24 ч (установлено <6 ч) после сбора. Чтобы обеспечить такое высокое качество выборки, четырем центрам, расположенным поблизости от координационного центра исследования, было предложено принять участие в анализе этой подгруппы. При отборе учитывалось, что центры лечили достаточное количество пациентов с трансплантацией и что были представлены обе вакцины.
У всех участников исследования (соответствие требованиям для лиц старше 18 лет и подписанного информированного согласия) в Т0, Т2 и Т3 были проведены вышеупомянутые измерения антител с использованием ИФА Euroimmun на анализаторах Euroimmun (5–9). Чтобы изучить клеточный иммунный ответ на SARS-CoV-2 в подгруппах, анализ высвобождения интерферона-γ, специфичного для SARS-CoV-2 (Euroimmun-SARS-CoV-2-IGRA для исследований, использует только ET 2606-3003 и EQ 6841-9).6011,2) (10). Подгруппа для IGRA была сформирована следующим образом: для анализа Т-клеток нужны яркие клетки. Для достижения высокой жизнеспособности в образцах IGRA обработка должна начинаться через <24 ч (установлено <6 ч) после сбора. Чтобы обеспечить такое высокое качество выборки, четырем центрам, расположенным поблизости от координационного центра исследования, было предложено принять участие в анализе этой подгруппы. При отборе учитывалось, что центры лечили достаточное количество пациентов с трансплантацией и что были представлены обе вакцины. Точная процедура и анализ дополнительно описаны в другом месте (1).
Точная процедура и анализ дополнительно описаны в другом месте (1).
Статистический анализ
В описательном анализе основных конечных точек исследования категориальные переменные суммировались как абсолютные частоты или проценты, а непрерывные переменные суммировались с использованием среднего значения и SD или медианы и межквартильного диапазона (IQR). Временные тренды ответов IgG и RBD-IgG, а также различия между группами анализировали либо с помощью критерия знакового ранга Уилкоксона, либо критерия хи-квадрат, в зависимости от ситуации. Анализ факторов риска у пациентов с выраженным снижением уровня антител проводили с помощью множественной логистической регрессии. Для проверки гипотез был выбран уровень значимости 5% (двусторонний). Поправка Бонферрони применялась в течение постфактум тестирование групповых эффектов. Анализ данных был реализован в R Environment for Statistical Computing (11), версия 4.0.4.
Интервальная классификация по уровням
В предложенной интервальной классификации уровень 0 присваивается значениям IgG и RBD ниже соответствующего порога положительности [35,2 Единиц связывающего антитела/мл (BAU/мл) и 35% соответственно], а остальные значения разделены на четыре интервала примерно равной длины (дополнительная таблица 2). Эти интервалы можно использовать для количественной оценки изменения IgG или RBD-IgG между T2 и T3, где, например, положительное изменение соответствует увеличению IgG или RBD-IgG соответственно, причем изменение на 4 соответствует максимальному увеличению. . Основываясь на этом определении, мы назвали любое снижение более чем на один уровень (по крайней мере, два) «резкой реакцией на сильное снижение». Распределение уровней IgG и RBD-IgG на T2 и T3 и их изменение между T2 и T3 обобщены на дополнительных рисунках S2A-F и отдельно зависят от использования MMF/MPA.
Эти интервалы можно использовать для количественной оценки изменения IgG или RBD-IgG между T2 и T3, где, например, положительное изменение соответствует увеличению IgG или RBD-IgG соответственно, причем изменение на 4 соответствует максимальному увеличению. . Основываясь на этом определении, мы назвали любое снижение более чем на один уровень (по крайней мере, два) «резкой реакцией на сильное снижение». Распределение уровней IgG и RBD-IgG на T2 и T3 и их изменение между T2 и T3 обобщены на дополнительных рисунках S2A-F и отдельно зависят от использования MMF/MPA.
Многомерный анализ
Помимо пола, возраста и типа вакцины, связь между различными типами иммуносупрессивных препаратов, такими как ингибиторы кальциневрина, кортикостероиды, ингибиторы mTOR и MMF/MPA, и сильным снижением IgG-ответа изучалась с использованием штрафной шкалы. модель логистической регрессии, оцененная с использованием метода эластичной сети (12). На дополнительном рисунке 3 показана пошаговая процедура выбора модели, в которой предикторы (4 типа иммунодепрессантов) добавляются к регрессионной модели по одному, чтобы максимизировать соответствие, оцениваемое по отклонению, с учетом текущего количества предикторов. Наклон каждого пути на дополнительном рисунке 3 меняется по мере того, как в модель входит новый иммунодепрессант. Согласно этому графику, MMF/MPA обладает наибольшей объяснительной способностью как единственный предиктор.
Наклон каждого пути на дополнительном рисунке 3 меняется по мере того, как в модель входит новый иммунодепрессант. Согласно этому графику, MMF/MPA обладает наибольшей объяснительной способностью как единственный предиктор.
Определение группы KTR
IgA Группа KTR IgA ( n = 26) определяется как сероконверсионная группа с положительной реакцией IgA de novo без положительного ответа IgG на Т2 после двукратной вакцинации мРНК (< 35,2 BAU) /мл в соответствии с определением производителя, см. также рисунок 1). В этой группе 24 из 26 (92%) KTR получали ММФ/МПА, поскольку большинство из них (20/26) пришлось исключить из-за непредвиденной третьей вакцинации диализными центрами, несмотря на формальную сероконверсию. Девятнадцать из 24 пациентов, получавших ММФ/МПА, лечили KTR 9.Группа 0011 IgA получила дополнительную бустерную дозу мРНК-вакцины между T2 и T3. Напротив, 5 из 24 KTR IgA пациентов с MMF/MPA не были вакцинированы в третий раз.
Результаты
Реципиенты почечного трансплантата 112 группа: разделение всех 112 КТР на две группы с ММФ/МПА ( n = 61) и без ММФ/МПА ( n = 51) демонстрирует, что за исключением типы иммунодепрессантов обеих групп хорошо соответствуют характеристикам пациентов (дополнительная таблица 1). Многомерный анализ КТР 112 показало, что MMF/MPA, но не другие иммунодепрессанты, такие как ингибиторы кальциневрина, ингибиторы mTOR или глюкокортикоиды, значительно влияли на титры связанных с вакцинацией антител IgG против спайкового белка S1 и снижались между 2 и 6 месяцами (таблица 2). В то время как через 2 месяца уровни IgG у KTR  Общая тенденция к снижению наблюдалась в обеих группах, но KTR 112 с MMF/MPA в три раза реже демонстрировали сильное снижение IgG, чем KTR 112 без MMF/MPA ( p = 0,003). Сравнимая разница для KTR 112 с MMF/MPA и без них также наблюдалась для RBD-IgG: более низкие значения для MMF на Т2 ( p = 0,003) и отсутствие значимой разницы на Т3 ( p = 0,135).
Общая тенденция к снижению наблюдалась в обеих группах, но KTR 112 с MMF/MPA в три раза реже демонстрировали сильное снижение IgG, чем KTR 112 без MMF/MPA ( p = 0,003). Сравнимая разница для KTR 112 с MMF/MPA и без них также наблюдалась для RBD-IgG: более низкие значения для MMF на Т2 ( p = 0,003) и отсутствие значимой разницы на Т3 ( p = 0,135).
Таблица 2 . Многофакторный анализ снижения антител IgG между T2 и T3 у реципиентов трансплантата почки после сероконверсии [когорта реципиентов трансплантата почки (KTR) 112 ].
Таблица 3 . Анализ высвобождения антител и интерферона-γ (IGRA) титры 2 (T2) и через 6 месяцев (T3) после вакцинации у реципиентов трансплантата почки с сероконверсией (KTR) 112 когорта с микофенолата мофетилом или микофеноловой кислотой (MMF/MPA) и без них.
Рисунок 2A . Динамика антител IgG к SARS-CoV-2 у сероконвертированных реципиентов почечного трансплантата (KTR) без (зеленый) или с (оранжевый) лечением микофенолата мофетилом или микофеноловой кислотой (MMF/MPA). Каждая тонкая линия соответствует значениям антител IgG против спайкового белка S1 (QuantiVac, Euroimmun) участника исследования от T0 (начало вакцинации) через T2 (8 недель после начала вакцинации) до T3 (6 месяцев после начала вакцинации). KTR, обработанные без MMF/MPA, представлены зеленым цветом, а KTR, подвергшиеся обработке MMF/MPA, показаны оранжевым цветом. Учитывались только пациенты с успешной сероконверсией de novo на Т2 (положительный результат на антитела IgA или IgG к белку S1 SARS-CoV-2) после двукратной вакцинации мРНК и без антител к нуклеокапсиду SARS-CoV-2 (NCP). Область, заштрихованная серым цветом, обозначает пограничный диапазон IgG ниже уровня положительности. Вертикальная ось изображена на бревне 10 шкала с соответствующей единицей БАЕ/мл.
Каждая тонкая линия соответствует значениям антител IgG против спайкового белка S1 (QuantiVac, Euroimmun) участника исследования от T0 (начало вакцинации) через T2 (8 недель после начала вакцинации) до T3 (6 месяцев после начала вакцинации). KTR, обработанные без MMF/MPA, представлены зеленым цветом, а KTR, подвергшиеся обработке MMF/MPA, показаны оранжевым цветом. Учитывались только пациенты с успешной сероконверсией de novo на Т2 (положительный результат на антитела IgA или IgG к белку S1 SARS-CoV-2) после двукратной вакцинации мРНК и без антител к нуклеокапсиду SARS-CoV-2 (NCP). Область, заштрихованная серым цветом, обозначает пограничный диапазон IgG ниже уровня положительности. Вертикальная ось изображена на бревне 10 шкала с соответствующей единицей БАЕ/мл.
Рисунок 2B . Динамика антител RBD-IgG к SARS-CoV-2 у сероконвертированных реципиентов почечного трансплантата (KTR) без (зеленый) или с (оранжевый) лечением микофенолата мофетилом или микофеноловой кислотой (MMF/MPA). Каждая тонкая линия соответствует значениям антител RBD-IgG против спайкового белка S1 (Евроиммун) участника исследования от Т2 (8 недель после начала вакцинации) до Т3 (6 месяцев после начала вакцинации). KTR, обработанные без MMF/MPA, представлены зеленым цветом, а KTR, подвергшиеся обработке MMF/MPA, показаны оранжевым цветом. Учитывались только пациенты с успешной сероконверсией de novo на Т2 (положительный результат на антитела IgA или IgG к белку S1 SARS-CoV-2) после двукратной вакцинации мРНК и без антител к нуклеокапсиду SARS-CoV-2 (NCP). Область, заштрихованная серым цветом, обозначает пограничный диапазон RBD-IgG ниже уровня положительности. Вертикальная ось изображена на бревне 10 шкала с соответствующей единицей % ингибирования.
Каждая тонкая линия соответствует значениям антител RBD-IgG против спайкового белка S1 (Евроиммун) участника исследования от Т2 (8 недель после начала вакцинации) до Т3 (6 месяцев после начала вакцинации). KTR, обработанные без MMF/MPA, представлены зеленым цветом, а KTR, подвергшиеся обработке MMF/MPA, показаны оранжевым цветом. Учитывались только пациенты с успешной сероконверсией de novo на Т2 (положительный результат на антитела IgA или IgG к белку S1 SARS-CoV-2) после двукратной вакцинации мРНК и без антител к нуклеокапсиду SARS-CoV-2 (NCP). Область, заштрихованная серым цветом, обозначает пограничный диапазон RBD-IgG ниже уровня положительности. Вертикальная ось изображена на бревне 10 шкала с соответствующей единицей % ингибирования.
Используя 20% в качестве предела, только 48% или 48% пациентов с MMF/MPA, но 69% или 62% KTR без MMF показали снижение титров антител против шипа S1 IgG или RBD-IgG на Т3, соответственно (таблица 1, рис. 2А/В). В общей сложности 25% или 20% KTR 112 с MMF/MPA, но только 4% или 2% KTR без MMF/MPA показали увеличение антител IgG или RBD-IgG до T3. Этот отсроченный ответ антител/увеличение у пациентов с MMF/MPA также отражается 9% сероконверсированных KTR 112 , которые характеризуются положительной реакцией de novo RBD-IgG на Т3.
Этот отсроченный ответ антител/увеличение у пациентов с MMF/MPA также отражается 9% сероконверсированных KTR 112 , которые характеризуются положительной реакцией de novo RBD-IgG на Т3.
Напротив, уровни антител к белку IgA против шипа S1 и показатели клеточного иммунитета не зависели от использования MMF/MPA (таблица 1).
Только у одного KTR развилась бессимптомная болезнь COVID-19 с сероконверсией антинуклеокапсидных антител (NCP).
Реципиенты почечного трансплантата
IgA Группа Большинство (20/26) «только сероконвертирующих антител IgA против спайка S1» KTR 9Группа 0011 IgA (IgA, но без сероконверсии IgG) должна была быть исключена из приведенной выше оценки из-за непредвиденной третьей вакцинации диализными центрами, несмотря на формальную сероконверсию. В этой подгруппе 24 из 26 (92%) KTR получали MMF/MPA, что еще раз подтверждает общие результаты нашего исследования, связанные с MMF/MPA-зависимыми IgG-антителами. Девятнадцать из 24 пациентов, получавших MMF/MPA KTR IgA , получили дополнительную бустерную дозу мРНК-вакцины через 4,2 ± 1 месяц, что продемонстрировало заметное увеличение IgG (дополнительная таблица 3, дополнительная фигура 4) и RBD-IgG (дополнительная таблица 3) почти в все пациенты между T2 и T3 соответственно. Напротив, 5 из 24 КТР IgA пациентов с ММФ/МПА не были вакцинированы в третий раз и оставались на значительно более низком уровне титров антител Т3. Тем не менее, двое из пяти из этих пациентов с «сероконверсией только IgA» с MMF / MPA показали отсроченную de novo положительную реакцию антител IgG на Т3 без какой-либо бустерной вакцинации (дополнительная фигура 4).
Девятнадцать из 24 пациентов, получавших MMF/MPA KTR IgA , получили дополнительную бустерную дозу мРНК-вакцины через 4,2 ± 1 месяц, что продемонстрировало заметное увеличение IgG (дополнительная таблица 3, дополнительная фигура 4) и RBD-IgG (дополнительная таблица 3) почти в все пациенты между T2 и T3 соответственно. Напротив, 5 из 24 КТР IgA пациентов с ММФ/МПА не были вакцинированы в третий раз и оставались на значительно более низком уровне титров антител Т3. Тем не менее, двое из пяти из этих пациентов с «сероконверсией только IgA» с MMF / MPA показали отсроченную de novo положительную реакцию антител IgG на Т3 без какой-либо бустерной вакцинации (дополнительная фигура 4).
Обсуждение
Преимущественно используемый иммуносупрессивный антиметаболит MMF/MPA снижает как скорость сероконверсии, так и титры IgG и RBD-IgG у реципиентов органов через 2 месяца после вакцинации мРНК SARS-CoV-2 (1–3) . Данные нашего исследования неожиданно демонстрируют, что снижение количества антител у пациентов с сероконверсией, получавших ММФ/МПА, снижается, что приводит к эквивалентным показателям серопозитивности и титрам через 6 месяцев наблюдения по сравнению с KTR без ММФ/МПА. Наши данные свидетельствуют о том, что ММФ/МПА ответственен за отсроченный гуморальный иммунный ответ IgG с другой временной динамикой, в частности, выработкой и снижением уровня IgG-антител по сравнению с реципиентами трансплантата с иммуносупрессивной терапией без ММФ/МПА, у которых 35% лечились mTOR-I. . Почти все КТР с повышением или de novo Реакция антител IgG или RBD-IgG между 2 и 6 месяцами была обнаружена в группе MMF/MPA, где она наблюдалась примерно у четверти пациентов. Интересно, что эти эффекты ММФ/МФК не наблюдались в отношении связанного с вакцинацией IgA- или Т-клеточного ответа. Представляют ли эти результаты опосредованную MMF/MPA проблему задержки переключения IgM/IgG, но не IgA, остается неясным. Аналогичный отсроченный иммунный ответ при KTR был показан другими пациентами после заболевания COVID-19 (13). Здесь ранний ответ IgA и IgM против SARS-CoV-2 возник у KTR, тогда как ответ IgG оказался отсроченным по сравнению с иммунокомпетентными людьми. В то время как MMF/MPA, как и другие антиметаболиты, такие как азатиоприн или mTOR-I, оказывает широкий спектр ингибирующего действия на B-, T-, дендритные клетки, макрофаги и эндотелиальные клетки (14), снижает уровни IgG (15 ) и отчетливые эффекты на дифференциальные классы иммуноглобулинов (16), серьезные различия между MMF/MPA и mTOR-I были продемонстрированы при воздействии на KTR иммуноцианина, пневмококкового полисахарида (PPS) или столбнячного анатоксина (TT) (17).
Наши данные свидетельствуют о том, что ММФ/МПА ответственен за отсроченный гуморальный иммунный ответ IgG с другой временной динамикой, в частности, выработкой и снижением уровня IgG-антител по сравнению с реципиентами трансплантата с иммуносупрессивной терапией без ММФ/МПА, у которых 35% лечились mTOR-I. . Почти все КТР с повышением или de novo Реакция антител IgG или RBD-IgG между 2 и 6 месяцами была обнаружена в группе MMF/MPA, где она наблюдалась примерно у четверти пациентов. Интересно, что эти эффекты ММФ/МФК не наблюдались в отношении связанного с вакцинацией IgA- или Т-клеточного ответа. Представляют ли эти результаты опосредованную MMF/MPA проблему задержки переключения IgM/IgG, но не IgA, остается неясным. Аналогичный отсроченный иммунный ответ при KTR был показан другими пациентами после заболевания COVID-19 (13). Здесь ранний ответ IgA и IgM против SARS-CoV-2 возник у KTR, тогда как ответ IgG оказался отсроченным по сравнению с иммунокомпетентными людьми. В то время как MMF/MPA, как и другие антиметаболиты, такие как азатиоприн или mTOR-I, оказывает широкий спектр ингибирующего действия на B-, T-, дендритные клетки, макрофаги и эндотелиальные клетки (14), снижает уровни IgG (15 ) и отчетливые эффекты на дифференциальные классы иммуноглобулинов (16), серьезные различия между MMF/MPA и mTOR-I были продемонстрированы при воздействии на KTR иммуноцианина, пневмококкового полисахарида (PPS) или столбнячного анатоксина (TT) (17). Таким образом, только ММФ/МПА вызывал серьезное снижение количества В-клеток и полное нарушение первичных и вторичных гуморальных ответов, в то время как лечение эверолимусом mTOR-I приводило к первичным иммунным ответам и усилению Т-клеточно-зависимых и -независимых вторичных гуморальных ответов на указанные выше реакции. вакцина. Тем не менее, мотивированное вакцинацией прекращение или снижение дозы ММФ/МФК и экспозиция или замена mTOR-I должны быть сбалансированы с риском отторжения. В то время как некоторые центры трансплантологии уже рассматривают возможность временного прекращения лечения MMF/MPA для достижения сероконверсии у не сероконвертирующих KTR, наши данные демонстрируют опосредованный MMF/MPA сдвиг во временной динамике антител, связанный со сниженным риском ухудшения, что позволяет предположить, что этот подход не является необходимым для сероконвертирующих KTR. В этом контексте интересно, что сероконверсия KTR 9В группе 0011 IgA с сероконверсией IgA, но без IgG преобладала обработка MMF/MPA.
Таким образом, только ММФ/МПА вызывал серьезное снижение количества В-клеток и полное нарушение первичных и вторичных гуморальных ответов, в то время как лечение эверолимусом mTOR-I приводило к первичным иммунным ответам и усилению Т-клеточно-зависимых и -независимых вторичных гуморальных ответов на указанные выше реакции. вакцина. Тем не менее, мотивированное вакцинацией прекращение или снижение дозы ММФ/МФК и экспозиция или замена mTOR-I должны быть сбалансированы с риском отторжения. В то время как некоторые центры трансплантологии уже рассматривают возможность временного прекращения лечения MMF/MPA для достижения сероконверсии у не сероконвертирующих KTR, наши данные демонстрируют опосредованный MMF/MPA сдвиг во временной динамике антител, связанный со сниженным риском ухудшения, что позволяет предположить, что этот подход не является необходимым для сероконвертирующих KTR. В этом контексте интересно, что сероконверсия KTR 9В группе 0011 IgA с сероконверсией IgA, но без IgG преобладала обработка MMF/MPA. В этой группе пациентов ревакцинация мРНК (третья) по-прежнему приводила к заметному увеличению титра IgG и RBD-IgG почти у всех пациентов, что указывает на ценность измерений антител IgA. Тем не менее, несмотря на отсутствие видимых клинических последствий этого отсроченного иммунного ответа в нашей исследуемой популяции, эта ситуация может измениться в зависимости от региональных условий пандемии, когда может потребоваться своевременная и надежная защита.
В этой группе пациентов ревакцинация мРНК (третья) по-прежнему приводила к заметному увеличению титра IgG и RBD-IgG почти у всех пациентов, что указывает на ценность измерений антител IgA. Тем не менее, несмотря на отсутствие видимых клинических последствий этого отсроченного иммунного ответа в нашей исследуемой популяции, эта ситуация может измениться в зависимости от региональных условий пандемии, когда может потребоваться своевременная и надежная защита.
Принимая во внимание частоту и последствия недостаточной защиты в уязвимой популяции реципиентов трансплантатов, иммунный мониторинг должен быть неотъемлемой частью ухода за пациентами и использоваться для определения сроков дополнительных ревакцинаций. Таким образом, MMF/MPA, по-видимому, является наиболее важным лекарственным средством, изменяющим не только вероятность сероконверсии, но также пиковый уровень и временной ход образования и снижения специфических антител IgG и RBD-IgG после успешной вакцинации против SARS-CoV-2.
Заявление о доступности данных
После публикации основной цели данные могут быть предоставлены заинтересованным ученым по запросу (например, для мета-анализа, медицинских регистров или других научных вопросов) анонимным способом в течение пяти лет, если члены группа DIA-Vacc соглашается.
Заявление об этике
В соответствии с профессиональным кодексом поведения для врачей (15 долларов США) клиническое исследование было представлено экспертным советам по этике в Техническом университете Дрездена (TU Dresden), ответственным за координирующего исследователя (BO-EK-45012021), а также в Лейпцигском университете (046/21-lk) и Саксонской медицинской ассоциации (Sächsische Landesärztekammer — EK-BR-10/21-1), ответственных за дальнейшее участие в исследованиях.
Вклад авторов
Вкладчики JSt и CH внесли свой вклад в разработку дизайна исследования, сбор данных, интерпретацию данных и составление рукописи. TS, JSc, GG, AP, AS, FG, FK, HK, PA, JSr, KF и TT участвовали в сборе данных и организации исследования. AK и RM участвовали в статистическом анализе или управлении данными исследования. TS, JSc, GG и AP участвовали в наборе пациентов и сборе данных. Все авторы внесли свой вклад в статью и одобрили представленную версию.
AK и RM участвовали в статистическом анализе или управлении данными исследования. TS, JSc, GG и AP участвовали в наборе пациентов и сборе данных. Все авторы внесли свой вклад в статью и одобрили представленную версию.
Финансирование
Это исследование финансировалось Else Kröner Fresenius Stiftung, Bad Homburg v. d. H., номер гранта Fördervertrag EKFS 2021_EKSE.27 и «Sächsisches Staatsministerium für Wissenschaft, Kultur und Tourismus» через Sächsische AufbauBank, номер гранта (SAB-Antragsnr). (100592538).
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Примечание издателя
Все претензии, изложенные в этой статье, принадлежат исключительно авторам и не обязательно представляют претензии их дочерних организаций или издателя, редакторов и рецензентов. Любой продукт, который может быть оценен в этой статье, или претензии, которые могут быть сделаны его производителем, не гарантируются и не поддерживаются издателем.
Благодарности
* DIA-Vacc-Исследователи
Членов в алфавитном порядке в соответствующих центрах:
1 Medizinische Klinik und Poliklinik III, Universitätsklinikum, Карл Густав Карус, Technische Universität Dresden, Dresden, Germany
Andreann, Nicole Bunker, Susanne Drolfus, Petyaranna, Anrena, Anrena, Anrena, Anrena, Anrena, Drinana, Drinana, Drinana, Angeren, Dresana, Angeren, Drishen, Dresana. Haaser, Sabrina Heide, Gabriele Hirt, Franziska Klemt, Markus Latk, Jens Passauer, Miriam Poser, Margrit Reinhardt, Ronny Rettig, Vladimir Todorov, Kerstin Zäumer
3 KfH-Nierenzentrum am Klinikum Chemnitz, Krankenhaus Küchwal, Германия
Angela Grzegorek, Markus Hallmann, Saskia Härtwig, Christiane Hintzen-Kruse, Frauke Neidt und Söhne, Susann Reissland, Bianca Seidel, Anett Speer, Peggy Weiß, Christine Wiech
4 Dialysezentrum Chemnitz, Chemnitz, Germany
Маркус Глэзер, Ульрике Рихардт, Аня Рихтер, Катрин Шайбнер, Андреас Зон
5 KfH-Nierenzentrum am Klinikum St. Georg, Лейпциг, Германия
Georg, Лейпциг, Германия
Йоахим Беж, Печень Карефманн, Кристиан Шуффио, Клаудхауф Сивенова
6 PHV Dialysezentrum Dresden-Johannstadt, Dresden, Germany
Steffen Bischoff, Petra Müller, Tatjana Seitz
8 Institut für Transfusionsmedizin Plauen, DRK-Blutspendedienst Nord-Ost gemeinnützige GmbH , Plauen, Germany
Надин Хильдебрандт, Андреас Карл.
Дальнейшие сторонники
Д. Михаэль Альбрехт, Medizinischer Vorstand (Sprecher), Universitätsklinikum Carl Gustav Carus Dresden
Томас Грюневальд, Хемниц, Ворзитцендер Сэчсиш Ипфкомиссия
Патриция Кляйн, Эрцтлише Гесчафтсфюхрерин, Сент -Сент -Сент -Эрсенд.
EUROIMMUN Medizinische Labordiagnostika AG, Любек, Германия, предоставила для этого исследования анализы ELISA на антитела и анализы высвобождения гамма-интерферона.
Дополнительный материал
Дополнительный материал к этой статье можно найти в Интернете по адресу: https://www. frontiersin.org/articles/10.3389/fmed.2022.928542/full#supplementary-material
frontiersin.org/articles/10.3389/fmed.2022.928542/full#supplementary-material
Ссылки
1. Stumpf J, Siepmann T, Lindner T, Karger C, Schwobel J, Anders L, et al. Гуморальный и клеточный иммунитет к вакцинации против SARS-CoV-2 у пациентов с почечным трансплантатом по сравнению с диализными пациентами: проспективное многоцентровое обсервационное исследование с использованием мРНК-1273 или мРНК-вакцины BNT162b2. Lancet Reg Health Eur . (2021) 9:100178. doi: 10.1016/j.lanepe.2021.100178
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
2. Группер А., Рабинович Л., Шварц Д., Шварц И.Ф., Бен-Йегояда М., Шашар М. и др. Снижение гуморального ответа на вакцину мРНК SARS-CoV-2 BNT162b2 у реципиентов почечного трансплантата без предварительного контакта с вирусом. Am J Трансплантация. (2021) 21:2719–26. doi: 10.1111/ajt.16615
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
3. Боярский Б.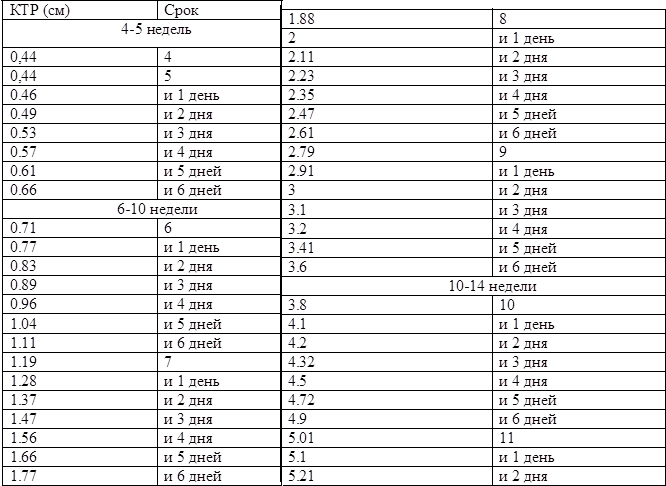 Дж., Вербель В.А., Эйвери Р.К., Тобиан А.Р., Масси А.Б., Сегев Д.Л., и соавт. Реакция антител на 2-дозную серию мРНК вакцины против SARS-CoV-2 у реципиентов трансплантатов паренхиматозных органов. ЯМА. (2021) 325:2204–6. doi: 10.1001/jama.2021.7489
Дж., Вербель В.А., Эйвери Р.К., Тобиан А.Р., Масси А.Б., Сегев Д.Л., и соавт. Реакция антител на 2-дозную серию мРНК вакцины против SARS-CoV-2 у реципиентов трансплантатов паренхиматозных органов. ЯМА. (2021) 325:2204–6. doi: 10.1001/jama.2021.7489
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
4. Stumpf J, Schwobel J, Lindner T, Anders L, Siepmann T, Karger C, et al. Риск сильного снижения уровня антител у диализных пациентов и пациентов после трансплантации после вакцинации мРНК SARS-CoV-2: данные за шесть месяцев обсервационного исследования диа-вакка. Ланцет Reg Health Eur. (2022) 17:100371. doi: 10.1016/j.lanepe.2022.100371
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
5. Падоан А., Шаковелли Л., Бассо Д., Негрини Д., Зуин С., Косма С. и другие. Ответ IgA-Ab на шиповидный гликопротеин SARS-CoV-2 у пациентов с COVID-19: продольное исследование. Клин Чим Акта. (2020) 507: 164–6. doi: 10. 1016/j.cca.2020.04.026
1016/j.cca.2020.04.026
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
6. Rubio-Acero R, Castelletti N, Fingerle V, Olbrich L, Bakuli A, Wölfel R, et al. В поисках корреляции защиты от SARS-CoV-2: прямое сравнение двух количественных анализов S1 в группе предварительно охарактеризованных олиго-/бессимптомных пациентов. Заразить Dis Ther . (2021) 10:1505–18. doi: 10.1007/s40121-021-00475-x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
7. Müller L, Andrée M, Moskorz W, Drexler I, Walotka L, Grothmann R, et al. Возрастной иммунный ответ на вакцину Biontech/Pfizer BNT162b2 против COVID-19. Клин Заражение Дис . 73:2065–72. doi: 10.1101/2021.03.03.21251066
CrossRef Полный текст | Google Scholar
8. Meyer B, Torriani G, Yerly S, Mazza L, Calame A, Arm-Vernez I, et al. Валидация коммерчески доступного серологического иммуноанализа SARS-CoV-2. Clin Microbiol Infect. (2020) 26:1386–94. doi: 10.1016/j.cmi.2020.06.024
doi: 10.1016/j.cmi.2020.06.024
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
9. EUROIMMUN Medizinische Labordiagnostika AG aPc. SARS-CoV-2 NeutraLISA . (2021). Доступно в Интернете по адресу: https://www.coronavirus-diagnostics.com/documents/Indications/Infections/Coronavirus/EI_2606_D_UK_F.pdf (по состоянию на 31 марта 2021 г.).
Google Scholar
10. Aiello A, Najafi Fard S, Petruccioli E, Petrone L, Vanini V, Farroni C, et al. Спайк является наиболее узнаваемым антигеном на платформе цельной крови как при остром, так и при выздоравливающем COVID-19.пациенты. Int J Infect Dis. (2021) 106: 338–47. doi: 10.1016/j.ijid.2021.04.034
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
11. R Core Team. R: Язык и среда для статистических вычислений . 4.0.1 изд. Вена: R Foundation for Statistical Computing (2020).
Google Scholar
12. Фридман Дж., Хасти Т., Тибширани Р. Пути регуляризации для обобщенных линейных моделей через координатный спуск. J Программное обеспечение стат. (2010) 33:1–22. doi: 10.18637/jss.v033.i01
Пути регуляризации для обобщенных линейных моделей через координатный спуск. J Программное обеспечение стат. (2010) 33:1–22. doi: 10.18637/jss.v033.i01
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
13. Cravedi P, Ahearn P, Wang L, Yalamarti T, Hartzell S, Azzi Y, et al. Отсроченная кинетика IgG, но не IgA, антиспайковых антител у реципиентов трансплантата после инфекции SARS-CoV-2. J Am Soc Нефрол. (2021) 32:3221–30. doi: 10.1681/ASN.2021040573
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
14. Риттер М.Л., Пирофски Л. Мофетил микофенолята: влияние на субпопуляции клеточного иммунитета, инфекционные осложнения и антимикробная активность. Transpl Infect Dis. (2009) 11:290–7. doi: 10.1111/j.1399-3062.2009.00407.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
15. Jonsson CA, Carlsten H. Микофеноловая кислота ингибирует инозин-5′-монофосфатдегидрогеназу и подавляет продукцию иммуноглобулинов и цитокинов В-лимфоцитами. Int Immunopharmacol. (2003) 3:31–7. doi: 10.1016/S1567-5769(02)00210-2
Int Immunopharmacol. (2003) 3:31–7. doi: 10.1016/S1567-5769(02)00210-2
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
16. Змонарски С.С., Боратынска М., Мадзярска К., Клингер М., Куштель М., Патрзалек Д. и соавт. Микофенолата мофетил сильно подавляет гуморальный ответ на ЦМВ-инфекцию в раннем посттрансплантационном периоде. Процесс трансплантации. (2003) 35:2205–6. doi: 10.1016/S0041-1345(03)00764-4
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
17. Struijk GH, Minnee RC, Koch SD, Zwinderman AH, van Donselaar-van der Pant KA, Idu MM, et al. Поддерживающая иммуносупрессивная терапия эверолимусом сохраняет гуморальный иммунный ответ. Почки, внутр. (2010) 78:934–40. doi: 10.1038/ki.2010.269
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Купить Втулка монтажная алюминиевая 6мм M3 — 2шт. — Ботланд
Индекс: ПЛЛ-01838 EAN: 52362652
- Описание
- Доставка
- Вложения
- Отзывы
- Две монтажные втулки
- Шестигранный ключ
- Винты для сжатия элемента на валу двигателя
Подробные размеры указаны на техническом чертеже.
Переходник предназначен для валов диаметром 6 мм, круглых или в форме буквы «D». В концентраторе есть шесть отверстий с резьбой M3 для винтов, которые позволяют устанавливать элементы. Работает с колесами Pololu 90×10 и 80×10 мм любого цвета.
Черные диски от Pololu 90×10 мм, устанавливаются с помощью адаптера
для двигателя с редуктором 37Dx129L:1.
Полезные ссылки
|
Доставка в тот же день
- Зачисление оплаты заказа на наш счет в рабочий день до 10:00 означает отправку товара в тот же день.
- Все посылки доставляются курьером GLS Group и застрахованы до 1200 евро.
- Вы получите ссылку для отслеживания вашей посылки и отслеживания хода доставки, как только она будет отправлена.

Условия поставки
GLS — зона 1Австрия, Бельгия, Хорватия, Чехия, Дания, Германия, Нидерланды, Польша, Словакия
- Срок доставки: 2-4 дня
- Стоимость доставки: от 4.18 евро
- Страховка: 1200 евро
Условия обслуживания
GLS — зона 2Болгария, Эстония, Франция, Венгрия, Италия, Латвия, Литва, Люксембург, Португалия, Румыния, Сан-Марино, Словения
- Срок доставки: 2-5 дней
- Стоимость доставки: от 5,35 EUR
- Страховка: 1200 евро
Условия обслуживания
GLS — зона 3Финляндия, Греция, Ирландия, Испания, Швеция
- Срок доставки: 2-7 дней
- Стоимость доставки: от 7,67 евро
- Страховка: 1200 евро
Условия обслуживания
Способы оплаты
PayPal- Botland является проверенным продавцом PayPal.